名校
解题方法
1 . 回答下列问题:
(1)②元素原子的电子式是:_______ 。
(2)硅元素在周期表中的位置是:第_______ 周期_______ 族。
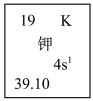
(3)如图所示钾元素的部分信息,“30.97”数值表示_______ 。______ (填元素符号)。③和⑧两种元素形成的气态氢化物稳定性强的是_______ (填化学式)。写出④的最高价氧化物对应水合物和⑧的最高价氧化物对应水合物相互反应的化学方程式_______ 。
(5)Cl元素比S元素的非金属性强,请从原子结构角度解释原因_______ 。能证明这一事实的化学反应为_______ (写一个化学方程式)。
(6)能证明O元素的非金属性强于S元素的依据是_______ 。
A.热稳定性:H2O>H2S B.SO2中O显负价 C.沸点:S>O2
(7)氧元素有三种核素:16O、17O、18O,对这三种核素的描述错误的是_______ 。
(8)元素周期表可以用于寻找新元素、发现物质的新用途。下列说法正确的是_______ 。
(9)元素周期表中,某些主族元素与右下方的主族元素(如图)的性质具有相似性,这种规律被称为“对角线规则”。下列叙述错误的是_______ 。
族 周期 | ⅠA | 0 | |||||||
| 1 | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |||
| 2 | ① | ② | ③ | ||||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ||||
(1)②元素原子的电子式是:
(2)硅元素在周期表中的位置是:第
(3)如图所示钾元素的部分信息,“30.97”数值表示
(5)Cl元素比S元素的非金属性强,请从原子结构角度解释原因
(6)能证明O元素的非金属性强于S元素的依据是
A.热稳定性:H2O>H2S B.SO2中O显负价 C.沸点:S>O2
(7)氧元素有三种核素:16O、17O、18O,对这三种核素的描述错误的是
| A.质子数相同 | B.质量相同 |
| C.化学性质相同 | D.位置相同(周期表中) |
(8)元素周期表可以用于寻找新元素、发现物质的新用途。下列说法正确的是
| A.在周期表中金属与非金属的分界处可以找到催化剂材料 |
| B.对氟、氯、硫、磷、砷等元素的研究,有助于制造出新品种的农药 |
| C.在过渡元素中可寻找制造半导体的元素 |
| D.可在第IA、IIA族元素中寻找制造耐高温、耐腐蚀合金的元素 |
(9)元素周期表中,某些主族元素与右下方的主族元素(如图)的性质具有相似性,这种规律被称为“对角线规则”。下列叙述错误的是
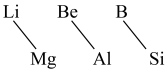
| A.Li在空气中燃烧生成Li2O、Li3N | B.硼酸是弱酸 |
| C.Be不与水反应 | D.Be(OH)2是两性氢氧化物 |
您最近一年使用:0次
名校
2 . 类推的思维方法在化学学习中应用广泛,但类推出的结论需经过实践的检验才能确定其正确与否。下列几种类推结论错误的是
| A.Al(OH)3能与NaOH溶液反应,则Be(OH)2也能与NaOH溶液反应 |
| B.SO2是“V形”分子,则O3是“V形”分子 |
| C.第二周期元素氢化物稳定性:H2O>HF>NH3,则第三周期元素氢化物稳定性:H2S>HCl>PH3 |
| D.工业制Mg采用电解熔融MgCl2的方法,则工业制Al也可采用电解熔融AlCl3的方法 |
您最近一年使用:0次
名校
3 . 已知周期表中金属与非金属分界线方向对角的两主族元素性质相似,如Li与Mg、Be与Al、B和Si 相似,这一规律被称为“对角线规则”,下列叙述正确的是
| A.Be能和氨水反应产生H2 | B.BeO为两性氧化物 |
| C.Li 在空气中的燃烧产物为Li2O2 | D.H3BO3是一种强酸 |
您最近一年使用:0次
2024-01-25更新
|
111次组卷
|
2卷引用:陕西省汉中市九校联盟2023-2024学年高一上学期1月期末化学试题
名校
4 . 如图所示为元素周期表的一部分,其中的编号代表对应的元素。

请回答下列问题:
(1)表中属于d区的元素是___________ (填编号);④⑤⑥⑦⑧五种元素形成的稳定离子中,离子半径最小的是___________ (填离子符号)。
(2)某元素原子的价层电子排布式为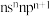 ,该元素原子的最外层电子的孤电子对数为
,该元素原子的最外层电子的孤电子对数为___________ ,该元素的第一电离能___________ (填“大于”“等于”或“小于”)原子的价层电子排布式为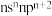 的元素。
的元素。
(3)某些不同族元素的性质也有一定的相似性,如上表中元素⑤与元素②的氢氧化物有相似的性质。请写出元素②的氢氧化物与 溶液反应的化学方程式:
溶液反应的化学方程式:___________ 。
(4)上述10种元素形成的最高价氧化物对应水化物中,酸性最强的是___________ (填化学式)。
(5)下列各组微粒的空间结构相同的是___________ (填序号)。
① 和
和 ②
② 和
和 ③
③ 和
和 ④
④ 和
和 ⑤
⑤ 和
和 ⑥
⑥ 和
和 ⑦
⑦ 和
和

请回答下列问题:
(1)表中属于d区的元素是
(2)某元素原子的价层电子排布式为
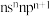 ,该元素原子的最外层电子的孤电子对数为
,该元素原子的最外层电子的孤电子对数为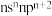 的元素。
的元素。(3)某些不同族元素的性质也有一定的相似性,如上表中元素⑤与元素②的氢氧化物有相似的性质。请写出元素②的氢氧化物与
 溶液反应的化学方程式:
溶液反应的化学方程式:(4)上述10种元素形成的最高价氧化物对应水化物中,酸性最强的是
(5)下列各组微粒的空间结构相同的是
①
 和
和 ②
② 和
和 ③
③ 和
和 ④
④ 和
和 ⑤
⑤ 和
和 ⑥
⑥ 和
和 ⑦
⑦ 和
和
您最近一年使用:0次
名校
5 . “类比”是预测物质性质与化学反应的重要方法之一,但“类比”不能违背客观事实,下列“类比”合理的是
| A.Na2O2与CO2反应生成Na2CO3和O2,则Na2O2与SO2反应生成Na2SO3和O2 |
| B.Na在空气中燃烧生成Na2O2,则同族的Li在空气中燃烧也生成Li2O2 |
| C.Al(OH)3溶于NaOH溶液生成Na[Al(OH)4],则Be(OH)2也能溶于NaOH溶液生成Na2[Be(OH)4] |
| D.Al3+与S2﹣在水溶液中因水解无法大量共存,则Fe3+与S2﹣在水溶液中也因水解无法大量共存 |
您最近一年使用:0次
2023-07-24更新
|
261次组卷
|
4卷引用:浙江省宁波市九校2022-2023学年高二上学期期末联考化学试题
21-22高二下·全国·单元测试
解题方法
6 . 元素的对角线规则
(1)在元素周期表中,某些_______ 族元素与其右下方的_______ 族元素(如图)的有些性质是相似的(如锂和镁在过量的氧气中燃烧均生成正常氧化物,而不是过氧化物),这种相似性被称为“_______ ”。

(2)处于“对角线”位置的元素,它们的_______ 具有相似性。
实例分析:
①锂和镁的相似性
A.锂与镁的沸点较为接近:
B.锂和镁在氧气中_______ 时只生成对应的氧化物,并且Li2O和MgO与水反应都十分缓慢。
4Li+O2 2Li2O、2Mg+O2
2Li2O、2Mg+O2 2MgO。
2MgO。
C.锂和镁与水的反应都十分缓慢,并且生成的氢氧化物_______ 溶于水,附着于金属表面阻碍反应的进行。
D.锂和镁都能直接与氮气反应生成相应的氮化物Li3N和Mg3N2。
E.锂和镁的氢氧化物在加热时,可分解为Li2O、H2O和MgO、H2O。
F.在碱金属的氟化物、碳酸盐和磷酸盐中,只有锂盐是_______ 溶于水的,相应的镁盐也_______ 溶于水。
②铍和铝的相似性
A.铍与铝都可与酸、碱反应放出_______ ,并且铍在浓硝酸中也发生_______ 化。
B.二者的氧化物和氢氧化物都既能溶于强酸又能溶于强碱溶液:
Al(OH)3+3HCl=_______ ,Al(OH)3+NaOH=_______ ;
Be(OH)2+2HCl=_______ ,Be(OH)2+2NaOH=_______ 。
C.二者的氧化物Al2O3和BeO的熔点和硬度都很高。
D.BeCl2和AlCl3都是共价化合物,易_______ 。
③硼和硅的相似性
A.自然界中B与Si均以化合物的形式存在。
B.B与Si的单质都易与强碱反应,且不与稀酸反应:
2B+2KOH+2H2O=_______ ,Si+2KOH+H2O=_______ 。
C.硼烷和硅烷的稳定性都比较差,且都易_______ 。
D.硼和硅的卤化物的熔、沸点比较低,易挥发,易水解。
(1)在元素周期表中,某些

(2)处于“对角线”位置的元素,它们的
实例分析:
①锂和镁的相似性
A.锂与镁的沸点较为接近:
| 元素 | Li | Na | Be | Mg |
| 沸点/℃ | 1 341 | 881.4 | 2 467 | 1 100 |
B.锂和镁在氧气中
4Li+O2
 2Li2O、2Mg+O2
2Li2O、2Mg+O2 2MgO。
2MgO。C.锂和镁与水的反应都十分缓慢,并且生成的氢氧化物
D.锂和镁都能直接与氮气反应生成相应的氮化物Li3N和Mg3N2。
E.锂和镁的氢氧化物在加热时,可分解为Li2O、H2O和MgO、H2O。
F.在碱金属的氟化物、碳酸盐和磷酸盐中,只有锂盐是
②铍和铝的相似性
A.铍与铝都可与酸、碱反应放出
B.二者的氧化物和氢氧化物都既能溶于强酸又能溶于强碱溶液:
Al(OH)3+3HCl=
Be(OH)2+2HCl=
C.二者的氧化物Al2O3和BeO的熔点和硬度都很高。
D.BeCl2和AlCl3都是共价化合物,易
③硼和硅的相似性
A.自然界中B与Si均以化合物的形式存在。
B.B与Si的单质都易与强碱反应,且不与稀酸反应:
2B+2KOH+2H2O=
C.硼烷和硅烷的稳定性都比较差,且都易
D.硼和硅的卤化物的熔、沸点比较低,易挥发,易水解。
您最近一年使用:0次
名校
解题方法
7 . 元素周期表中,某些主族元素与右下方的主族元素(如图)的性质具有相似性,这种规律被称为“对角线规则”。则下列叙述错误的是
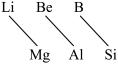

A. 受热分解生成 受热分解生成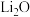 和 和 |
B.氧化铍的化学式为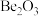 |
C.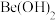 既能溶于强酸又能溶于强碱溶液 既能溶于强酸又能溶于强碱溶液 |
| D.类似硅酸钠溶液显碱性一样,硼酸钠溶液显碱性 |
您最近一年使用:0次
2022-12-24更新
|
375次组卷
|
4卷引用:吉林省长春市东北师范大学附属中学2022-2023学年高一上学期阶段考试化学试题
吉林省长春市东北师范大学附属中学2022-2023学年高一上学期阶段考试化学试题(已下线)【2023】【高一上】【源清中学】【期末考】【高中化学】【赵优萍收集】第2课时 元素周期表和元素周期律的应用(已下线)课时2 元素周期表和元素周期律的应用
8 . 按要求填空:
(1)基态K原子中,核外电子占据最高能层的符号是_______ ,占据该能层电子的电子云轮廓图形状为_______ 。
(2)在周期表中,与Li的化学性质最相似的邻族元素是_______ ,该元素基态原子核外M层电子的自旋状态_______ (填“相同”或“相反”)。
(1)基态K原子中,核外电子占据最高能层的符号是
(2)在周期表中,与Li的化学性质最相似的邻族元素是
您最近一年使用:0次
名校
解题方法
9 . “类推”是一种重要的学习方法。下列类推的结论与事实不相符的是
A.由 微溶于水,推知 微溶于水,推知 微溶于水 微溶于水 |
B.由 有两性,推知 有两性,推知 有两性 有两性 |
C.由 与水反应生成HCl和HClO,推知 与水反应生成HCl和HClO,推知 与水反应生成HF和HFO 与水反应生成HF和HFO |
| D.由N元素的最高正价是+5,推知P元素的最高正价是+5 |
您最近一年使用:0次
2022-04-27更新
|
413次组卷
|
4卷引用:四川省成都市蓉城名校联盟2021-2022学年高一下学期期中联考化学试题
10 . 回答下列问题
(1)为什么副族元素又称为过渡元素?_______
(2)为什么在元素周期表中非金属元素主要集中在右上角三角区内?处于非金属三角区边缘的元素常被称为半金属或准金属。为什么?_______
(3)在周期表里找出Cr和Cu的价层电子,它们的电子排布符合构造原理吗?此外还有哪些元素的基态原子电子排布不符合构造原理?_______
(4)预言119号元素基态原子最外层电子排布;预言第八周期有多少种元素?_______
(5)对角线规则:元素周期表中的某些主族元素其某些性质与_______ 元素相似。
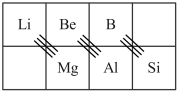
如铍、铝两元素的性质相似性
(1)为什么副族元素又称为过渡元素?
(2)为什么在元素周期表中非金属元素主要集中在右上角三角区内?处于非金属三角区边缘的元素常被称为半金属或准金属。为什么?
(3)在周期表里找出Cr和Cu的价层电子,它们的电子排布符合构造原理吗?此外还有哪些元素的基态原子电子排布不符合构造原理?
(4)预言119号元素基态原子最外层电子排布;预言第八周期有多少种元素?
(5)对角线规则:元素周期表中的某些主族元素其某些性质与

如铍、铝两元素的性质相似性
| 与酸反应 | 与碱反应 | |
| 单质 | ||
| 氧化物 | ||
| 氢氧化物 |
您最近一年使用:0次



