名校
解题方法
1 . X、Y、Z、W为原子序数依次增大的短周期主族元素,Y、W同族,常温下Z的单质遇Y的最高价氧化物对应的水化物的浓溶液会发生钝化反应,由X、Y、Z三种原子构成的一种特殊离子化合物如图所示,下列说法正确的是
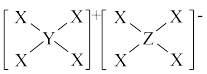
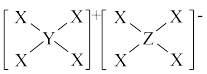
| A.在元素周期表中,113号元素与Z元素不同族 |
| B.Y的非金属性比W的强,所以单质的还原性:Y>W |
| C.X、Y形成的二元化合物只含有极性共价键 |
| D.X、Z、Y、W四种元素的简单离子半径依次增大 |
您最近一年使用:0次
2021-04-24更新
|
1299次组卷
|
10卷引用:安徽省皖南八校2021届高三4月第三次联考理综化学试题
安徽省皖南八校2021届高三4月第三次联考理综化学试题安徽省六校教育研究会2022届高三第一次素质测试化学试题安徽省合肥市第六中学2022届高三上学期开学考试化学试题(已下线)考点08 分子间作用力 氢键-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点08 微粒间作用力-备战2022年高考化学一轮复习考点帮(浙江专用)(已下线)专题05 物质结构和元素周期律-备战2022年高考化学学霸纠错(全国通用)辽宁省协作体2021-2022学年下学期高三第一次模拟考试化学试题四川省成都市树德中学2021-2022学年高二下学期4月阶段性测试化学试题辽宁省阜新市实验中学2021-2022学年高三下学期第一次模拟考试化学试题辽宁省葫芦岛市四校2022-2023学年高三上学期期中联考化学试题
名校
2 . 短周期主族元素X、Y、M、W、Q的原子序数依次增大。X-的电子层结构与氦相同,Y元素的某种单质可用作自来水消毒剂,Q和Y同族,M、W、Y三种元素组成的盐M2WY3的溶液通入过量CO2后产生白色胶状沉淀。下列说法不正确的是
| A.M和Y形成的化合物M2Y2中,阴阳离子的个数比为1:2 |
| B.WY2可用于制作计算机芯片 |
| C.化合物MX具有很强的还原性,能与水反应 |
| D.最简单气态氢化物的热稳定性:Q>W |
您最近一年使用:0次
2022-02-02更新
|
600次组卷
|
2卷引用:安徽省马鞍山市 2021-2022学年高三第一次教学质量监测理综化学试题
名校
3 . 我国科学家最近在锂电池研究方面取得新进展,其电解质阴离子结构如图所示。已知:短周期元素X、Y、Z、R、W的原子序数依次递增且X、Y、Z、R位于同周期。下列叙述正确的是
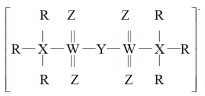
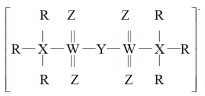
A.原子的第一电离能: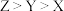 | B.简单氢化物的还原性: |
| C.Y的氧化物对应的水化物一定是强酸 | D.简单氢化物的沸点: |
您最近一年使用:0次
名校
解题方法
4 . X、Y、Z、W是原子序数依次增大的前20号元素,常温下只有一种元素的单质为气态。基态X原子s轨道上的电子数是p轨道上的2倍,Y的简单氢化物与其最高价含氧酸反应会产生白烟,Z与X形成的某种化合物常温下为液体,基态W原子有1个未成对电子。下列说法错误的是
| A.氢化物的沸点:Y>Z>X |
| B.电负性:Y>Z>X>W |
| C.原子半径:W>Z>X>Y |
| D.上述元素形成的某种化合物的溶液可用于检测Fe3+ |
您最近一年使用:0次
名校
5 . 短周期主族元素a、b、c、d的原子序数依次增大。四种元素形成的单质依次为m、n、p、q,x、y、z是这些元素组成的二元化合物,其中z为形成酸雨的主要物质之一,w溶液可使酚酞溶液显红色。上述物质的转化关系如图所示。下列说法正确的是( )
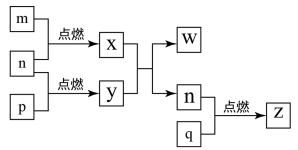

A.原子半径的大小: |
B.x的电子式一定是 |
C.简单氢化物的沸点: |
| D.y、w含有的化学键类型完全相同 |
您最近一年使用:0次
2020-09-03更新
|
1980次组卷
|
6卷引用:【全国百强校】安徽省六安市第一中学2017-2018学年高一下学期第二次阶段性考试化学试题
【全国百强校】安徽省六安市第一中学2017-2018学年高一下学期第二次阶段性考试化学试题苏教版(2020)高一必修第一册专题5 总结检测人教版(2019)高一必修第一册 第四章素养检测(已下线)第15练 第四章章末质量检测-2022年【寒假分层作业】高一化学(人教版2019)江西宜春市铜鼓中学2022-2023学年高一下学期第一次段考化学试题湖南省长沙市明德中学2022-2023学年高一下学期5月月考化学试题
名校
解题方法
6 . 一种由短周期主族元素组成的化合物,其阴离子结构如图所示。W、X、Y、Z原子序数之和为20。下列有关叙述正确的是


| A.由Y、Z、W三种元素组成的化合物都属于有机物 |
| B.原子半径:W<X<Z<Y |
| C.X的最高价氧化物对应的水化物是强酸 |
| D.还原性:ZW4>W2Y |
您最近一年使用:0次
2022-05-27更新
|
579次组卷
|
4卷引用:安徽省安庆市桐城中学2022-2023学年高一上学期期末考试化学试题
安徽省安庆市桐城中学2022-2023学年高一上学期期末考试化学试题广东省广州市广大附中、广外、铁一中学三校2022届高三三模联考化学试题(已下线)专题06 物质结构元素周期律-三年(2020-2022)高考真题分项汇编福建永春一中、培元中学、季延中学、石光中学2022-2023学年高三上学期期中考联考化学试题
名校
解题方法
7 . 已知:a、b、c、d为四种短周期主族元素。其中a元素存在一种没有中子的原子,b原子的L层电子数为4, 的密度是相同状况下氢气密度的16倍,d与c同主族。下列说法中正确的是
的密度是相同状况下氢气密度的16倍,d与c同主族。下列说法中正确的是
 的密度是相同状况下氢气密度的16倍,d与c同主族。下列说法中正确的是
的密度是相同状况下氢气密度的16倍,d与c同主族。下列说法中正确的是| A.c的最高正价为+6价 | B.原子半径: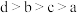 |
C.最简单氢化物的沸点: | D.a、c、d形成的化合物属于强酸 |
您最近一年使用:0次
2023-12-31更新
|
377次组卷
|
2卷引用:安徽省阜阳市第三中学2023-2024学年高一上学期1月期末化学试题
名校
8 . 短周期元素W、R、X、Y、Z原子序数依次增大,可形成甲、乙(结构如图)两种具有强还原性的物质,且X、Z同主族。下列说法错误的是
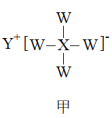
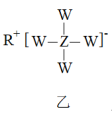
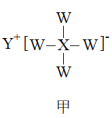
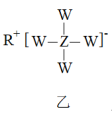
| A.W、X分别是氢元素和硼元素 |
| B.五种元素中,Y原子半径最大 |
| C.Z元素最高价氧化物对应的水化物具有两性 |
| D.单质Y和R在空气中均可燃烧,燃烧产物所含化学键类型完全相同 |
您最近一年使用:0次
2021-09-18更新
|
872次组卷
|
9卷引用:安徽师范大学附属中学2022届高三下学期第十八次综合测试理综化学试题
安徽师范大学附属中学2022届高三下学期第十八次综合测试理综化学试题河北省唐山市2021-2022学年高三上学期开学摸底考试化学试题河北省石家庄市第二十二中学2022届高三10月月考化学试题浙江省嘉兴市2021-2022学年高三上学期选考模拟测试化学试题(已下线)解密05 物质结构 元素周期律(分层训练)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(浙江专用)(已下线)化学-2022年高考押题预测卷03(浙江卷)(已下线)押新高考卷06题 元素周期表元素周期律-备战2022年高考化学临考题号押题(新高考通版)浙江省2022届高三考前第三次模拟考试化学试题(已下线)专题12 元素周期律推断-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)
名校
解题方法
9 . X、Y、Z、W是原子序数依次增大的四种短周期元素,X氢化物的水溶液可用于刻蚀玻璃,Y是地壳中含量最高的金属元素,Z原子的核外电子数是X最外层电子数的2倍,W的单质是制作黑火药的原料之一。下列结论正确的是( )
| A.工业上通过电解法获取Y的单质 |
| B.简单氢化物的沸点:X<W |
| C.简单离子半径大小:X>Y>W |
| D.最高价氧化物水化物的酸性:Z>W |
您最近一年使用:0次
2022-04-11更新
|
877次组卷
|
6卷引用:安徽省合肥市2022届高三第二次教学质量检测理综化学试题
安徽省合肥市2022届高三第二次教学质量检测理综化学试题(已下线)押全国卷理综第10题 元素周期表 元素周期律-备战2022年高考化学临考题号押题(课标全国卷)四川省南充市2022届高三适应性考试(三诊)理综化学试题四川省内江市第六中学2022-2023学年高二下学期第一次月考(创新班)化学试题2024届四川省南充市高三下学期适应性考试(二诊)理综试题-高中化学2024届四川省成都石室中学高三下学期5月高考适应性考试(一)理科综合试卷-高中化学
名校
10 . 已知a、b、d、e、 f、g、 h为原子序数依次增大的六种短周期主族元素, 非金属元素a最外层电子数与其周期数相同,b原子的最外层电子数是其所在周期数的2倍。d的一种单质可杀菌消毒,g的最高正价与最低负价代数和为4, f的最高价氧化物可分别与e和h的最高价氧化物的水化物反应,a单质在h单质中燃烧,产物溶于水得到一种强酸甲。请用化学用语回答下列问题:
(1)f在元素周期表中的位置___ 画出与h同族的第四周期元素的原子结构示意图____________ 。
(2)d、e、f、h的简单离子的半径由大到小的顺序_________ 。
(3)下列说法正确的是 。
(4)设计一个简单的实验证明d和g的非金属性强弱: _________ (用化学方程式表示)。
(5)为降低水源中NO 对人体的危害,可在强碱性条件下用f的单质将溶液中的NO
对人体的危害,可在强碱性条件下用f的单质将溶液中的NO 还原为N2,该反应的离子方程式为
还原为N2,该反应的离子方程式为______________ 。
(6)将e和f单质各1mol投入足量水中,充分反应后,所得溶液体积为500mL,则该过程可得标况下气体体积_______ L。最终获得溶液的物质的量浓度为_____ mol∙L−1。
(1)f在元素周期表中的位置
(2)d、e、f、h的简单离子的半径由大到小的顺序
(3)下列说法正确的是 。
| A.氢化物的稳定性d>b |
| B.含氧酸的酸性h>g>b>f |
| C.bg2中b为+4价;g为−2价可说明g的非金属性强于b |
| D.g阴离子能与Fe3+反应而h的阴离子不能,可说明g的非金属性弱于h |
(5)为降低水源中NO
 对人体的危害,可在强碱性条件下用f的单质将溶液中的NO
对人体的危害,可在强碱性条件下用f的单质将溶液中的NO 还原为N2,该反应的离子方程式为
还原为N2,该反应的离子方程式为(6)将e和f单质各1mol投入足量水中,充分反应后,所得溶液体积为500mL,则该过程可得标况下气体体积
您最近一年使用:0次



