名校
1 . 已知a、b、d、e、 f、g、 h为原子序数依次增大的六种短周期主族元素, 非金属元素a最外层电子数与其周期数相同,b原子的最外层电子数是其所在周期数的2倍。d的一种单质可杀菌消毒,g的最高正价与最低负价代数和为4, f的最高价氧化物可分别与e和h的最高价氧化物的水化物反应,a单质在h单质中燃烧,产物溶于水得到一种强酸甲。请用化学用语回答下列问题:
(1)f在元素周期表中的位置___ 画出与h同族的第四周期元素的原子结构示意图____________ 。
(2)d、e、f、h的简单离子的半径由大到小的顺序_________ 。
(3)下列说法正确的是 。
(4)设计一个简单的实验证明d和g的非金属性强弱: _________ (用化学方程式表示)。
(5)为降低水源中NO 对人体的危害,可在强碱性条件下用f的单质将溶液中的NO
对人体的危害,可在强碱性条件下用f的单质将溶液中的NO 还原为N2,该反应的离子方程式为
还原为N2,该反应的离子方程式为______________ 。
(6)将e和f单质各1mol投入足量水中,充分反应后,所得溶液体积为500mL,则该过程可得标况下气体体积_______ L。最终获得溶液的物质的量浓度为_____ mol∙L−1。
(1)f在元素周期表中的位置
(2)d、e、f、h的简单离子的半径由大到小的顺序
(3)下列说法正确的是 。
| A.氢化物的稳定性d>b |
| B.含氧酸的酸性h>g>b>f |
| C.bg2中b为+4价;g为−2价可说明g的非金属性强于b |
| D.g阴离子能与Fe3+反应而h的阴离子不能,可说明g的非金属性弱于h |
(5)为降低水源中NO
 对人体的危害,可在强碱性条件下用f的单质将溶液中的NO
对人体的危害,可在强碱性条件下用f的单质将溶液中的NO 还原为N2,该反应的离子方程式为
还原为N2,该反应的离子方程式为(6)将e和f单质各1mol投入足量水中,充分反应后,所得溶液体积为500mL,则该过程可得标况下气体体积
您最近一年使用:0次
解题方法
2 . 现有部分短周期元素的性质或原子结构如表:
根据上述信息进行判断,并回答下列问题:
(1)元素W在元素周期表中的位置是第_____ 周期第_____ 族。
(2)元素X的一种同位素可测定文物的年代,这种同位素的符号是________ 。
(3)元素Y与氢元素形成一种离子YH4+,写出该微粒的电子式_____ ,如何检验某溶液中含该离子_____ 。
(4)元素Z与元素W相比,金属性较强的是_____ (用元素符号表示),下列表述中能证明这一事实的是_____ (填字母序号)。
A.Z单质的熔点比W单质的低
B.Z的化合价比W的低
C.常温下Z单质与水反应的程度很剧烈,而W单质在加热条件下才能与水反应
D.Z最高价氧化物对应的水化物的碱性比W的强
(5)由上述元素中的X、Y、Z组成的某剧毒化合物XYZ不慎泄漏时,消防人员通常采用喷洒过氧化氢溶液的方式处理,以减少污染。反应生成一种酸式盐和一种气体,二者的水溶液均呈碱性,该反应的化学方程式为______ 。
| T | 地壳中含量最多的元素 |
| X | 最外层电子数是次外层电子数的2倍 |
| Y | 常温下,单质为双原子分子,其氢化物的水溶液呈碱性 |
| Z | M层比K层少1个电子 |
| W | 其离子是第三周期金属元素的离子中半径最小的 |
(1)元素W在元素周期表中的位置是第
(2)元素X的一种同位素可测定文物的年代,这种同位素的符号是
(3)元素Y与氢元素形成一种离子YH4+,写出该微粒的电子式
(4)元素Z与元素W相比,金属性较强的是
A.Z单质的熔点比W单质的低
B.Z的化合价比W的低
C.常温下Z单质与水反应的程度很剧烈,而W单质在加热条件下才能与水反应
D.Z最高价氧化物对应的水化物的碱性比W的强
(5)由上述元素中的X、Y、Z组成的某剧毒化合物XYZ不慎泄漏时,消防人员通常采用喷洒过氧化氢溶液的方式处理,以减少污染。反应生成一种酸式盐和一种气体,二者的水溶液均呈碱性,该反应的化学方程式为
您最近一年使用:0次
2020-08-06更新
|
28次组卷
|
2卷引用:安徽师范大学附属外国语学校2020-2021学年高一4月月考化学试题
名校
解题方法
3 . X、Y、Z、M、R、Q是短周期主族元素,部分信息如下表所示:
(1)R在元素周期表中的位置是 ______ ;R在自然界中有质量数为35和37的两种核素,它们之间的关系互为 ______ .
(2)Z的单质与水反应的化学方程式是______ .
(3)Y与R相比,非金属性较强的是______ (用元素符号表示),下列事实能证明这一结论的是 ______ (选填字母序号).
a.常温下Y的单质呈固态,R的单质呈气态
b.还原性XR<YX4
c.Y与R形成的化合物中Y呈正价
(4)根据表中数据推测,Y的原子半径的最小范围是______ .
(5)甲、乙是上述部分元素的最高价氧化物的水化物,且甲+乙→丙+水.若丙的水溶液呈碱性,则丙的化学式是______ .
| X | Y | Z | M | R | Q | |
| 原子半径/nm | 0.186 | 0.074 | 0.099 | 0.143 | ||
| 主要化合价 | -4,+4 | -2 | -1,+7 | +3 | ||
| 其它 | 阳离子核外无电子 | 无机非金属材料的主角 | 焰色反应呈黄色 |
(2)Z的单质与水反应的化学方程式是
(3)Y与R相比,非金属性较强的是
a.常温下Y的单质呈固态,R的单质呈气态
b.还原性XR<YX4
c.Y与R形成的化合物中Y呈正价
(4)根据表中数据推测,Y的原子半径的最小范围是
(5)甲、乙是上述部分元素的最高价氧化物的水化物,且甲+乙→丙+水.若丙的水溶液呈碱性,则丙的化学式是
您最近一年使用:0次
名校
解题方法
4 . 已知:a、b、c、d为四种短周期主族元素。其中a元素存在一种没有中子的原子,b原子的L层电子数为4, 的密度是相同状况下氢气密度的16倍,d与c同主族。下列说法中正确的是
的密度是相同状况下氢气密度的16倍,d与c同主族。下列说法中正确的是
 的密度是相同状况下氢气密度的16倍,d与c同主族。下列说法中正确的是
的密度是相同状况下氢气密度的16倍,d与c同主族。下列说法中正确的是| A.c的最高正价为+6价 | B.原子半径: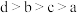 |
C.最简单氢化物的沸点: | D.a、c、d形成的化合物属于强酸 |
您最近一年使用:0次
2023-12-31更新
|
377次组卷
|
2卷引用:安徽省阜阳市第三中学2023-2024学年高一上学期1月期末化学试题
解题方法
5 . X、Y、Z、P、Q是原子序数依次增大的短周期主族元素,其中X的一种核素中没有中子,Y的单质和Z的单质是空气的主要成分,Z和Q同主族。做焰色试验时P元素的焰色为黄色。下列说法错误的是
A.原子半径: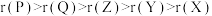 |
B. 中含有的化学键类型为离子键、共价键 中含有的化学键类型为离子键、共价键 |
| C.Q的简单气态氢化物的热稳定性比Z的弱 |
| D.X与Y或Z可形成的核外电子总数为10的微粒 |
您最近一年使用:0次
6 . X、Y、Z、W、R五种元素,原子序数依次增大,元素X有一种同位素无中子,Y的简单气态氢化物溶于水呈碱性,Z的2p轨道有两个未成对电子,W的离子是同周期离子半径最小的,R为第四周期基态原子未成对电子数最多的元素,下列说法错误的是
A. 性质较稳定是由于含有氢键的缘故 性质较稳定是由于含有氢键的缘故 |
| B.X、Y、Z组成的化合物可能是离子化合物 |
C.工业上常用电解熔融的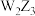 来制备单质W 来制备单质W |
| D.R位于周期表的d区 |
您最近一年使用:0次
2023-04-23更新
|
118次组卷
|
3卷引用:安徽省十联盟2022-2023学年高二下学期期中考试化学(B卷)试题
名校
解题方法
7 . X、Y、Z、W是原子序数依次增大的前20号元素,常温下只有一种元素的单质为气态。基态X原子s轨道上的电子数是p轨道上的2倍,Y的简单氢化物与其最高价含氧酸反应会产生白烟,Z与X形成的某种化合物常温下为液体,基态W原子有1个未成对电子。下列说法错误的是
| A.氢化物的沸点:Y>Z>X |
| B.电负性:Y>Z>X>W |
| C.原子半径:W>Z>X>Y |
| D.上述元素形成的某种化合物的溶液可用于检测Fe3+ |
您最近一年使用:0次
8 . 已知W、X、Y、Z四种元素分别属于三个短周期,且原子序数依次增大,由它们组成的化合物E、Q可以发生如下图的反应。化合物M是有机合成重要的中间体,M中阴离子为48电子微粒,下列说法错误的是
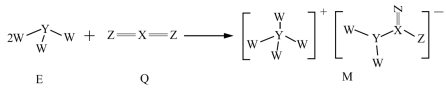
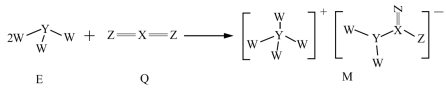
| A.E易液化,是因为可形成分子间氢键 | B.Q是导致温室效应的成分之一 |
| C.简单离子的半径:Y<Z | D.M的阴阳离子中均含有极性共价键 |
您最近一年使用:0次
名校
解题方法
9 . 短周期主族元素A、B、C、D、E的原子序数依次增大,A、B、C三种元素组成的化合物为强碱;化合物D2E2是一种具有难闻气味的黄红色液体,与其他元素组成的物质有如下转化关系:2D2E2+2A2B=DB2↑+□↓+4AE(方框代表一种生成物)。下列说法不正确的是
| A.DB2能使紫色石蕊变色 |
| B.简单阴离子还原性:D>E>A |
| C.D2E2分子中既存在极性键又存在非极性键 |
| D.上述方程式所涉物质中的□存在多种同素异形体 |
您最近一年使用:0次
解题方法
10 . 如图转化关系中,A、B、C、D是二元化合物,A与C均含有10个电子。甲、乙、丙是三种常见的非金属单质,下列说法不正确的是


| A.化合物A与丙可直接生成D |
| B.单质乙有多种同素异形体,均具有高熔点、高沸点、硬度大的性质 |
| C.稳定性:A<C |
| D.组成上述转化关系中的物质的元素种类共有三种 |
您最近一年使用:0次



