名校
解题方法
1 . 元素 、
、 、
、 、
、 、
、 均为原子序数依次增大的短周期主族元素,
均为原子序数依次增大的短周期主族元素, 在地壳金属元素中的含量仅次于
在地壳金属元素中的含量仅次于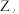 已知
已知 原子最外层电子数与核外电子总数之比为
原子最外层电子数与核外电子总数之比为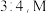 原子的最外层电子数与次外层电子数之比为3:4、N-、Z3+、X+离子半径逐渐减小;化合物
原子的最外层电子数与次外层电子数之比为3:4、N-、Z3+、X+离子半径逐渐减小;化合物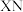 常温下为气体,请回答下列问题:
常温下为气体,请回答下列问题:
(1)写出 、
、 、
、 按原子个数之比
按原子个数之比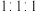 形成的化合物的化学式
形成的化合物的化学式_______ ; 和
和 气态氢化物的稳定性大小比较为
气态氢化物的稳定性大小比较为_______ (用化学式和“ ”“
”“ ”或“
”或“ ”表示)。
”表示)。
(2)X与 可分别形成
可分别形成 电子和
电子和 电子的分子,写出该
电子的分子,写出该 电子分子转化成
电子分子转化成 电子分子的化学方程式
电子分子的化学方程式_______ 。
(3)Z元素的单质能与 和
和 形成的化合物在一定条件下发生反应,同时放出大量的热,其反应的化学方程式为
形成的化合物在一定条件下发生反应,同时放出大量的热,其反应的化学方程式为_______ 。
(4)如图表示由上述元素中的某两种元素组成的气体分子在一定条件下的密闭容器中充分反应前后的转化关系,示意图中转移电子的数目为_______ 。
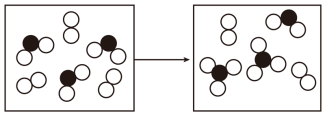
(5)由 、
、 、
、 三种元素组成的离子,在水溶液中与
三种元素组成的离子,在水溶液中与 和
和 均不能大量共存,还能和氯水反应,写出其与新制氯水反应的离子方程式
均不能大量共存,还能和氯水反应,写出其与新制氯水反应的离子方程式_______ 。
 、
、 、
、 、
、 、
、 均为原子序数依次增大的短周期主族元素,
均为原子序数依次增大的短周期主族元素, 在地壳金属元素中的含量仅次于
在地壳金属元素中的含量仅次于 已知
已知 原子最外层电子数与核外电子总数之比为
原子最外层电子数与核外电子总数之比为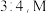 原子的最外层电子数与次外层电子数之比为3:4、N-、Z3+、X+离子半径逐渐减小;化合物
原子的最外层电子数与次外层电子数之比为3:4、N-、Z3+、X+离子半径逐渐减小;化合物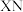 常温下为气体,请回答下列问题:
常温下为气体,请回答下列问题:(1)写出
 、
、 、
、 按原子个数之比
按原子个数之比 形成的化合物的化学式
形成的化合物的化学式 和
和 气态氢化物的稳定性大小比较为
气态氢化物的稳定性大小比较为 ”“
”“ ”或“
”或“ ”表示)。
”表示)。(2)X与
 可分别形成
可分别形成 电子和
电子和 电子的分子,写出该
电子的分子,写出该 电子分子转化成
电子分子转化成 电子分子的化学方程式
电子分子的化学方程式(3)Z元素的单质能与
 和
和 形成的化合物在一定条件下发生反应,同时放出大量的热,其反应的化学方程式为
形成的化合物在一定条件下发生反应,同时放出大量的热,其反应的化学方程式为(4)如图表示由上述元素中的某两种元素组成的气体分子在一定条件下的密闭容器中充分反应前后的转化关系,示意图中转移电子的数目为

(5)由
 、
、 、
、 三种元素组成的离子,在水溶液中与
三种元素组成的离子,在水溶液中与 和
和 均不能大量共存,还能和氯水反应,写出其与新制氯水反应的离子方程式
均不能大量共存,还能和氯水反应,写出其与新制氯水反应的离子方程式
您最近一年使用:0次
名校
解题方法
2 . 元素周期表是化学知识的宝库,它的内涵十分丰富。如表是a~m九种元素在周期表中的位置,请回答下列问题:
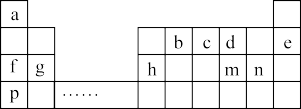
(1)m的阴离子结构示意图为____ 。
(2)d与a元素的原子按1:1结合的化合物的电子式____ 。
(3)b的最高价氧化物的结构式为____ 。
(4)d、g、n形成的简单离子的半径由大到小的顺序为____ (用离子符号填写)。
(5)f、g、p的最高价氧化物的水化物碱性从强到弱的顺序为____ (填化学式)。
(6)p和n两种元素最高价氧化物的水化物相互反应的离子反应方程式为____ 。
(7)c的氢化物和c的最高价氧化物对应水化物之间反应能生成盐M,M中含有的化学键类型有____ 。
(8)“类铝”在门捷列夫预言4年后,被布瓦博德朗在一种矿石中发现,命名为镓(Ga)。由镓的性质推知,镓与铝同主族,且位于h的下一周期。镓在周期表中的位置____ 。冶炼金属镓通常采用的方法是____ 。

(1)m的阴离子结构示意图为
(2)d与a元素的原子按1:1结合的化合物的电子式
(3)b的最高价氧化物的结构式为
(4)d、g、n形成的简单离子的半径由大到小的顺序为
(5)f、g、p的最高价氧化物的水化物碱性从强到弱的顺序为
(6)p和n两种元素最高价氧化物的水化物相互反应的离子反应方程式为
(7)c的氢化物和c的最高价氧化物对应水化物之间反应能生成盐M,M中含有的化学键类型有
(8)“类铝”在门捷列夫预言4年后,被布瓦博德朗在一种矿石中发现,命名为镓(Ga)。由镓的性质推知,镓与铝同主族,且位于h的下一周期。镓在周期表中的位置
您最近一年使用:0次
名校
3 . 短周期主族元素W、X、Y、Z的原子序数依次增大,X的原子半径是所有短周期主族元素中最大的,Y组成的单质是一种良好的半导体材料,Y的原子序数是Z的最外层电子数的2倍,由W、X、Y三种元素形成的化合物M的结构如图所示.下列叙述错误 的是


| A.Z的单质在H2中燃烧呈现苍白色火焰 |
| B.X2W2中阴阳离子个数比为1:2 |
| C.简单气态氢化物的稳定性:Y<Z |
| D.W、X、Z的简单离子半径依次增大 |
您最近一年使用:0次
2022-04-30更新
|
119次组卷
|
2卷引用:宁夏回族自治区银川一中2021-2022学年高一下学期期中考试化学试题
名校
4 . 某元素甲气态氢化物与该元素最高价氧化物的水化物反应生成盐,乙元素的简单离子半径在第三周期中最小,丙元素和丁元素同主族且原子序数丙是丁的两倍,下列说法正确的是
| A.食品包装袋中可以用甲的气态氢化物做保护气 |
B. 乙的单质在标准状况下和浓硝酸反应后,生成的气体约为 乙的单质在标准状况下和浓硝酸反应后,生成的气体约为 |
| C.丙和丁的常见单质的沸点,丙的高 |
D.乙和丁形成的化合物做的坩埚可以用来熔融 |
您最近一年使用:0次
2022-03-18更新
|
108次组卷
|
2卷引用:宁夏石嘴山市平罗中学2021-2022学年高一下学期第一次月考化学试题
名校
解题方法
5 . 已知短周期元素X、Y、Z、M、Q和R在周期表中的相对位置如图所示,其中X的最高化合价为+3。下列说法错误的是
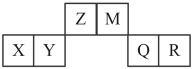

| A.最高价含氧酸酸性:Z>Y |
| B.X的氧化物可与Q的氢化物水溶液反应 |
| C.M的单质与Na反应时反应条件不同产物相同 |
| D.X、Y、Q、R的电子层数相同 |
您最近一年使用:0次
2022-03-05更新
|
479次组卷
|
2卷引用:宁夏青铜峡市宁朔中学2021-2022学年高一3月月考化学试题
名校
解题方法
6 . A、B、C、D为高氯酸铵中的元素,B元素原子的最外层电子数是内层电子数的3倍,D元素最高价氧化物的分子式为D2O7,C元素最高价氧化物对应的水化物能与其简单氢化物发生化合反应;E元素与D元素同周期,且E为碱金属元素。
(1)写出A、B、C的元素符号:A___ ,B___ ,C___ 。
(2)D元素在周期表中的位置为___ 。
(3)Al与E元素的最高价氧化物对应的水化物的溶液反应的化学方程式为___ 。
(1)写出A、B、C的元素符号:A
(2)D元素在周期表中的位置为
(3)Al与E元素的最高价氧化物对应的水化物的溶液反应的化学方程式为
您最近一年使用:0次
名校
7 . 现有部分短周期元素的性质或原子结构如下表:
(1)元素X位于周期表中的位置___ ,它的一种核素可测定文物的年代,这种核素的符号___
(2)元素Y的原子结构示意图为____ ,写出YH3和Y的最高价氧化物对应的水化物反应的化学方程式___ 。
(3)元素Z与元素T相比,非金属性较强的是__ (填元素符号),下列表述能证明这一事实的是__ 。
a.常温下Z的单质和T的单质状态不同
b.Z的氢化物比T的氢化物稳定
c.一定条件下Z和T的单质都能与NaOH溶液反应
(4)T、X、Y、Z四种元素的最高价氧化物对应水化物中酸性最强的是__ (填酸的化学式,下同),酸性最弱的是___ 。
| 元素编号 | 元素性质或原子结构 |
| T | M层上电子数是K层电子数的3倍 |
| X | 最外层电子数是次外层电子数的2倍 |
| Y | 常温下单质为双原子分子,其氢化物水溶液呈碱性 |
| Z | 元素最高正价是+7 |
(2)元素Y的原子结构示意图为
(3)元素Z与元素T相比,非金属性较强的是
a.常温下Z的单质和T的单质状态不同
b.Z的氢化物比T的氢化物稳定
c.一定条件下Z和T的单质都能与NaOH溶液反应
(4)T、X、Y、Z四种元素的最高价氧化物对应水化物中酸性最强的是
您最近一年使用:0次
名校
解题方法
8 . 已知X、Y为短周期元素,两元素形成化合物XY2,已知其原子序数分别为a和b,则a不可能为
| A.b-4 | B.b-5 | C.b+6 | D.b+8 |
您最近一年使用:0次
2021-04-11更新
|
90次组卷
|
3卷引用:宁夏回族自治区银川市北方民族大学附属中学2021-2022年高一下学期3月月考化学试题
名校
解题方法
9 . 有A、B、C、D四种短周期元素,它们的原子序数由A到D依次增大,已知A和B原子有相同的电子层数,且A的L层电子数是K层电子数的两倍,C燃烧时呈现黄色火焰,C的单质在点燃条件下与B的单质充分反应,可以得到与D单质颜色相同的淡黄色固态化合物,试根据以上叙述回答:
(1)元素A的名称_______ B的元素符号_______ D2-的离子结构示意图_______ 。
(2)分别写出AB2的结构式是_______ ,C2B2的电子式为_______ 。
(3)用电子式表示化合物C2D的形成过程_______ 。
(1)元素A的名称
(2)分别写出AB2的结构式是
(3)用电子式表示化合物C2D的形成过程
您最近一年使用:0次
名校
10 . 表中列出了①~⑨九种元素在周期表中的位置:
请按要求回答下列问题。
(1)元素④的名称是_______ ,元素④在周期表中所处位置是_______ ,从元素原子得失电子的角度看,元素④具有_______ 性;(填“氧化性”或“还原性”)。
(2)气态氢化物的④⑥⑦的稳定性由弱到强的顺序排列是_______ ;(用化学式和“<”表示)。
(3)元素⑦的原子结构示意图是_______ ;
(4)写出元素⑤形成的单质在与水反应的化学方程式_______ ,这一反应是_______ (填“吸热”或“放热”)反应。
(5)用电子式表示①与⑨反应得到的化合物的形成过程_______ 。
(6)⑥⑦⑨的最高价氧化物对应水化物的酸性由强到弱的顺序是_______ (用化学式和“>”表示)
| ⅠA | ||||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ② | ③ | ④ | ⑧ | ||||
| 3 | ⑤ | ⑥ | ⑦ | ⑨ |
(1)元素④的名称是
(2)气态氢化物的④⑥⑦的稳定性由弱到强的顺序排列是
(3)元素⑦的原子结构示意图是
(4)写出元素⑤形成的单质在与水反应的化学方程式
(5)用电子式表示①与⑨反应得到的化合物的形成过程
(6)⑥⑦⑨的最高价氧化物对应水化物的酸性由强到弱的顺序是
您最近一年使用:0次



