名校
1 . X、Y、Z、W、M五种元素的原子序数依次增大。已知X、Y、Z、W是短周期元素中的四种非金属元素,X元素的原子形成的离子就是一个质子;Y 原子的最外层电子数是内层电子数的2倍;Z、W在元素周期表中处于相邻的位置,它们的单质在常温下均为无色气体;M是地壳中含量最高的金属元素。下列说法正确的是
| A.X、Z、W三元素所形成的化合物一定为共价化合 物 |
| B.原子半径:r(M)>r(Y) >r(Z) >r(W) >r(X) |
| C.W和M形成的化合物不能与强碱反应 |
| D.Y、Z的最高价含氧酸的酸性:Y>Z |
您最近一年使用:0次
2019-05-28更新
|
237次组卷
|
6卷引用:宁夏回族自治区吴忠市吴忠中学2019-2020学年高一下学期4月第一次在线考试化学试题
名校
2 . 已知几种元素的性质或原子结构的相关叙述如表所示。
回答下列问题:
(1)写出工业上用X的单质来制备粗硅的化学方程式_________________________ 。
(2)Y形成的另一种单质主要存在于地球的平流层中,被称作地球生物的保护伞,该单质的化学式是________ 。
(3)元素Z在海水中含量非常高,海水中含Z元素的化合物主要是__________ (写化学式)。
(4)画出T原子的结构示意图:____________ 。
(5)T元素组成的单质在Y元素组成的常见单质中燃烧,得到的产物的化学式是________ ,电子式是____________ 。
| 元素 | 元素性质或原子结构的相关叙述 |
| T | 失去1个电子后,形成与Ne相同的核外电子排布 |
| X | 最外层电子数是次外层电子数的2倍 |
| Y | 其某种单质是空气的主要成分,也是最常见的助燃剂 |
| Z | 原子核外有3个电子层,最外层比次外层少1个电子 |
(1)写出工业上用X的单质来制备粗硅的化学方程式
(2)Y形成的另一种单质主要存在于地球的平流层中,被称作地球生物的保护伞,该单质的化学式是
(3)元素Z在海水中含量非常高,海水中含Z元素的化合物主要是
(4)画出T原子的结构示意图:
(5)T元素组成的单质在Y元素组成的常见单质中燃烧,得到的产物的化学式是
您最近一年使用:0次
9-10高一下·河南许昌·期末
名校
解题方法
3 . W、X、Y、Z是原子序数依次增大的同一短周期元素,W、X是金属元素,Y、Z是非金属元素。
(1)W和X的最高价氧化物的水化物之间可以相互反应生盐和水,该反应的离子方程式为___ 。
(2)W与Y可形成化合物W2Y,该化合物的电子式为___ 。
(3)比较Y、Z气态氢化物的稳定性 > (用化学式表示)___ 。
(4)Y的低价氧化物通入Z单质的水溶液中,发生反应的化学方程式为___ 。
(5)W、X、Y、Z四种元素简单离子的离子半径由大到小的顺序是: > > > (用离子符号表示)___ 。
(1)W和X的最高价氧化物的水化物之间可以相互反应生盐和水,该反应的离子方程式为
(2)W与Y可形成化合物W2Y,该化合物的电子式为
(3)比较Y、Z气态氢化物的稳定性 > (用化学式表示)
(4)Y的低价氧化物通入Z单质的水溶液中,发生反应的化学方程式为
(5)W、X、Y、Z四种元素简单离子的离子半径由大到小的顺序是: > > > (用离子符号表示)
您最近一年使用:0次
2020-06-03更新
|
54次组卷
|
10卷引用:宁夏贺兰景博中学2021-2022学年高一下学期第一次月考化学试题
宁夏贺兰景博中学2021-2022学年高一下学期第一次月考化学试题(已下线)2010年河南省许昌市六校联考高一下学期期末考试化学试题(已下线)2011-2012学年福建省四地六校高一下学期第二次联考化学试卷2015-2016学年河北省唐山市开滦二中高一下期中化学试卷云南省文山州马关县第一中学2018-2019学年高一6月份考试化学试题云南省澜沧一中2018-2019学年高一下学期期末考试化学试题河南省信阳市商城县上石桥高中2019-2020学年高一下学期期中考试化学试题江西省抚州市第一中学2022-2023学年高一下学期3月月考化学试题(已下线)2012-2013学年四川省双流中学高二入学考试化学试卷2015-2016学年安徽省淮北市第一中学新高二暑假返校提能化学试卷
11-12高一下·四川成都·期中
名校
4 . X、Y、Z、W、R是5种短周期元素,其原子序数依次增大。X是周期表中原子半径最小的元素,Y原子最外层电子数是次外层电子数的3倍,Z、W、R处于同一周期,R与Y处于同一族,Z、W原子的核外电子数之和与Y、R原子的核外电子数之和相等。下列说法正确的是 ( )
| A.元素Y、Z、W具有相同电子层结构的离子,其半径依次增大 |
| B.元素X不能与元素Y形成化合物X2Y2 |
| C.元素Y、R分别与元素X形成的化合物的沸点:XmY>XmR |
| D.元素W、R的最高价氧化物的水化物都是强酸 |
您最近一年使用:0次
2020-05-21更新
|
269次组卷
|
21卷引用:宁夏银川市宁夏大学附属中学2019-2020学年高一下学期期中考试化学试题
宁夏银川市宁夏大学附属中学2019-2020学年高一下学期期中考试化学试题(已下线)2011-2012学年四川成都外国语学校高一下学期期中考试化学试卷2015-2016学年黑龙江省哈尔滨六中高一下期中化学试卷云南省普洱市普洱第二中学2019—2020学年高一上学期期末考试化学试题2020年春季人教版高中化学必修2第一章《物质结构 元素周期律》测试卷湖南省常德市桃花源一中2019-2020学年高一下学期期中考试化学试题甘肃省会宁县第一中学2019-2020学年高一下学期第一次月考化学试题吉林省辽源市辽县第一高级中学2019-2020高一下学期期中考试化学试题安徽省安庆市第二中学2019-2020学年高一下学期期中考试化学试题吉林省四平市公主岭范家屯镇第一中学2019-2020学年高一期中考试化学试题河南省新乡市辉县市第二高级中学2019-2020学年高一下学期第一次月考试化学试题(A部)(已下线)2013届北京市通州区高三年级上学期期末摸底考试化学试卷2015届山东省淄博七中高三上学期期中考试化学试卷2014-2015江苏省启东中学高二下学期期中考试化学试卷2016-2017学年辽宁省盘锦中学高二上期初考试化学卷四川省威远中学2019-2020学年高二上学期第二次月考化学试题山西省大同市天镇一中2019-2020学年高二上学期期中考试化学试题广西靖西市第二中学2019-2020学年高二下学期开学考试化学试题广东省执信中学2021届高三上学期第二次月考化学试题广东省河源中学2021届高三上学期第二次质量检测化学试题(已下线)模块同步卷02 原子结构与元素的性质-《灯塔金卷系列》2020-2021学年高二化学模块同步卷(人教版选修3)
名校
5 . 短周期元素X、Y、Z、W、Q在周期表中的位置如表所示,其中W的气态氢化物摩尔质量为34 g/mol,Y的最低价氢化物为非电解质.则下列说法中正确的是( )
| X | Y | ||
| Z | W | Q |
| A.X的最低价氢化物水溶液显酸性 |
| B.Q单质能溶于水,且水溶液须用棕色细口瓶盛装 |
| C.Na与Y能形成化合物Na2Y2,且与水反应后溶液呈碱性 |
| D.阴离子还原性:W>Q |
您最近一年使用:0次
2018-05-09更新
|
454次组卷
|
6卷引用:宁夏银川一中2017-2018学年高一下学期期中考试化学试题
名校
解题方法
6 . 现有A、B、C、D、E五种短周期元素,已知A、B、C、D四种元素的核内质子数之和为56,在元素周期表中的位置如图所示,1 mol E的单质可与足量酸反应,能产生33.6 L H2(在标准状况下);E的阳离子与A的阴离子核外电子层结构相同。
回答下列问题:
(1)写出下列元素名称A__________ ,B___________ ,E____________
(2)C的简单离子结构示意图为_____________
(3)B单质在A单质中燃烧,反应现象是__________________________________ ,生成物的化学式为___________
(4)A与E形成的化合物的化学式为__________ ,它的性质决定了它在物质的分类中应属于__________________
(5)向D与E形成的化合物的水溶液中滴入烧碱溶液至过量,此过程中观察到的现象是_______________________ ,写出有关化学反应方程式______________________________ 。
| A | ||
| B | C | D |
(1)写出下列元素名称A
(2)C的简单离子结构示意图为
(3)B单质在A单质中燃烧,反应现象是
(4)A与E形成的化合物的化学式为
(5)向D与E形成的化合物的水溶液中滴入烧碱溶液至过量,此过程中观察到的现象是
您最近一年使用:0次
2018-05-09更新
|
249次组卷
|
3卷引用:宁夏银川一中2017-2018学年高一下学期期中考试化学试题
名校
7 . 短周期元素X、Y、W、Q在元素周期表中的相对位置如图所示。常温下,Al能溶于W的最高价氧化物对应水化物的稀溶液,却不溶于其浓溶液。下列说法正确的是
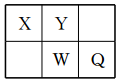

| A.Y的最高化合价为+6 |
| B.简单氢化物的稳定性:Y>W |
| C.简单离子半径:W>Q>Y>X |
| D.X、Y、W不可能同时存在于一种离子化合物中 |
您最近一年使用:0次
2018-05-05更新
|
154次组卷
|
3卷引用:宁夏育才中学2017-2018学年高一下学期期中考试化学试题
名校
解题方法
8 . 根据下表中几种短周期元素的原子半径及主要化合价,回答下列问题:
(1)元素D组成的常见单质有两种,分别是_______ 、________ (写名称)。
(2)用电子式表示IE2的形成过程:_________________________ 。
(3)A、H、J的离子半径由大到小顺序是_________ (用离子符号表示)。
(4)78 g J2B2与足量的水反应生成_______ L(标准状况下)气体。
(5)元素E的单质与水反应的离子方程式为_______________ 。
| 元素代号 | A | B | D | E | G | H | I | J |
| 化合价 | -1 | -2 | +4、-4 | -1 | +5、-3 | +3 | +2 | +1 |
| 原子半径 | 0.071 | 0.074 | 0.077 | 0.099 | 0.110 | 0.143 | 0.160 | 0.186 |
(2)用电子式表示IE2的形成过程:
(3)A、H、J的离子半径由大到小顺序是
(4)78 g J2B2与足量的水反应生成
(5)元素E的单质与水反应的离子方程式为
您最近一年使用:0次
13-14高一下·云南昆明·期中
名校
9 . 下列各元素的氧化物中,既能与盐酸反应,又能够与NaOH溶液反应的是( )
| A.元素X:它的原子中M层比L层少2个电子 |
| B.元素Y:它的二价阳离子核外电子总数与氩原子相同 |
| C.元素Z:位于元素周期表中的第三周期,ⅢA族 |
| D.元素W:它的焰色反应颜色呈黄色 |
您最近一年使用:0次
2019-04-26更新
|
139次组卷
|
9卷引用:宁夏长庆高级中学2020-2021学年高一上学期期中考试化学试题2
宁夏长庆高级中学2020-2021学年高一上学期期中考试化学试题2(已下线)2014届云南省昆明滇池中学高一下学期期中考试化学试卷【校级联考】湖北省宜昌市部分示范高中教学协作体2018-2019学年高一第二学期期中联考化学试题广东省北京师范大学东莞石竹附属学校2018-2019学年高一下学期期中考试化学试题甘肃省靖远县第四中学2018-2019学年高一下学期期中考试化学试题陕西省咸阳市乾县第二中学2019-2020学年高一下学期期中测试化学试题河南省焦作市沁阳市第一中学2019-2020学年高一下学期第一次月考化学试题甘肃省静宁县第一中学2020-2021学年高一下学期第三次月考化学(普通班)试题上海市崇明区民本中学2020-2021学年高二上学期期中考试化学试题
名校
10 . A、B、C、D、E五种短周期主族元素的原子序数依次增大,已知:
①其原子半径大小关系是D>E>B>C>A;
②A、D同主族,B、C、E分处三个连续的主族,且最外层电子数依次增加;
③C是地壳中含量最多的元素,D与C可形成原子个数比为1∶1或2∶1的化合物。
请填写以下空白:
(1)单质B的电子式为____________ ,结构式为____________ 。
(2)化合物D2C2的电子式为________________ 。用电子式表示D2C的形成过程:__________________________ 。
(3)单质A和单质B在一定条件下发生反应的化学方程式为_________________ 。
(4)单质E与A、C、D三种元素形成的化合物发生反应的化学方程式为___________ 。
①其原子半径大小关系是D>E>B>C>A;
②A、D同主族,B、C、E分处三个连续的主族,且最外层电子数依次增加;
③C是地壳中含量最多的元素,D与C可形成原子个数比为1∶1或2∶1的化合物。
请填写以下空白:
(1)单质B的电子式为
(2)化合物D2C2的电子式为
(3)单质A和单质B在一定条件下发生反应的化学方程式为
(4)单质E与A、C、D三种元素形成的化合物发生反应的化学方程式为
您最近一年使用:0次
2018-02-11更新
|
635次组卷
|
2卷引用:宁夏银川唐徕回民中学2017-2018学年高一4月月考化学试题



