名校
1 . 下表为对部分短周期元素的性质或原子结构的描述。
下列有关说法中正确的是
| 元素编号 | 元素性质或原子结构 |
| T | M层上的电子数是原子核外电子层数的2倍 |
| X | 最外层电子数是次外层电子数的2倍 |
| Y | 常温下单质为双原子分子,其氢化物的水溶液呈碱性 |
| Z | 元素最高正价是+7价 |
| A.元素的非金属性:Z>T |
| B.最高价氧化物对应水化物的酸性:X>T |
| C.气态氢化物的热稳定性:X>Y |
| D.Z、T两种元素的原子半径:Z>T |
您最近一年使用:0次
2021-06-21更新
|
782次组卷
|
8卷引用:第二节 元素周期律 第2课时 元素周期表和元素周期律的应用
2 . 短周期元素 、
、 、
、 、
、 的原子序数依次增大,
的原子序数依次增大, 的原子在元素周期表中半径最小;
的原子在元素周期表中半径最小; 的次外层电子数是其最外层电子数的
的次外层电子数是其最外层电子数的 ;
; 的单质可与冷水剧烈反应,产生
的单质可与冷水剧烈反应,产生 的单质;
的单质; 与
与 属于同一主族。下列叙述正确的是
属于同一主族。下列叙述正确的是
 、
、 、
、 、
、 的原子序数依次增大,
的原子序数依次增大, 的原子在元素周期表中半径最小;
的原子在元素周期表中半径最小; 的次外层电子数是其最外层电子数的
的次外层电子数是其最外层电子数的 ;
; 的单质可与冷水剧烈反应,产生
的单质可与冷水剧烈反应,产生 的单质;
的单质; 与
与 属于同一主族。下列叙述正确的是
属于同一主族。下列叙述正确的是A. 元素形成的简单离子与 元素形成的简单离子与 元素形成的简单离子的核外电子总数相同 元素形成的简单离子的核外电子总数相同 |
B.单质的氧化性: |
C.化合物 、 、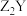 、 、 中化学键的类型完全相同 中化学键的类型完全相同 |
D.原子半径: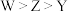 |
您最近一年使用:0次
2020-09-06更新
|
871次组卷
|
4卷引用:人教版(2019)高一必修第一册第四章 物质结构 元素周期律 素养拓展区
人教版(2019)高一必修第一册第四章 物质结构 元素周期律 素养拓展区高一必修第一册(苏教2019版)专题5 素养拓展区(已下线)第15练 第四章章末质量检测-2022年【寒假分层作业】高一化学(人教版2019)云南省昆明市四川师范大学昆明实验学校安宁校区2020-2021学年高一下学期开学考试化学试题
3 .  、
、 、
、 、
、 、
、 、
、 六种短周期元素的原子序数依次增大,
六种短周期元素的原子序数依次增大, 元素形成的单质是自然界中最轻的气体,
元素形成的单质是自然界中最轻的气体, 元素原子的半径是同周期元素原子中半径最大的。如图所示为元素周期表的一部分,
元素原子的半径是同周期元素原子中半径最大的。如图所示为元素周期表的一部分, 、
、 、
、 、
、 的原子序数之和为37。下列判断错误的是( )
的原子序数之和为37。下列判断错误的是( )
 、
、 、
、 、
、 、
、 、
、 六种短周期元素的原子序数依次增大,
六种短周期元素的原子序数依次增大, 元素形成的单质是自然界中最轻的气体,
元素形成的单质是自然界中最轻的气体, 元素原子的半径是同周期元素原子中半径最大的。如图所示为元素周期表的一部分,
元素原子的半径是同周期元素原子中半径最大的。如图所示为元素周期表的一部分, 、
、 、
、 、
、 的原子序数之和为37。下列判断错误的是( )
的原子序数之和为37。下列判断错误的是( )| A | B | D |
| E |
A. 、 、 都是第Ⅰ 都是第Ⅰ 族的金属元素 族的金属元素 |
B. 离子的氧化性小于 离子的氧化性小于 的氧化性 的氧化性 |
C. 元素的简单氢化物比 元素的简单氢化物比 元素的简单氢化物稳定 元素的简单氢化物稳定 |
D. 的一种氧化物 的一种氧化物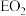 通入品红溶液中可使品红溶液褪色 通入品红溶液中可使品红溶液褪色 |
您最近一年使用:0次
名校
4 . 现有短周期元素X、Y、Z、M,X、Y位于同主族,Z、M位于同主族,Y、Z位于同周期,X与Z、M都不在同一周期,Z的核电荷数是M的2倍。下列说法正确的是
A.简单阳离子的氧化性: |
B.气态氢化物的沸点: |
| C.X、Z与M不可能存在同一离子化合物中 |
| D.Y2Z的溶液:c(Y+):c(Z2-) > 2:1 |
您最近一年使用:0次
2020-02-14更新
|
134次组卷
|
2卷引用:人教版高一化学必修2同步练习:第一章第二节第二课时《元素周期律的应用》
解题方法
5 . 已知X、Y、Z、W四种主族元素,X的阳离子与Y的阴离子具有相同的电子层结构;W的阳离子的氧化性强于等电荷数的X的阳离子的氧化性;Z的阴离子半径大于等电荷数的Y的阴离子半径,则四种元素的原子序数由大到小的顺序是( )
| A.Z>X>Y>W | B.W>X>Y>Z |
| C.X>Y>Z>W | D.Z>Y>X>W |
您最近一年使用:0次
解题方法
6 . 通常状况下, 、
、 和
和 是三种气态单质。
是三种气态单质。 的组成元素是第3周期原子半径最小的元素(稀有气体元素除外);
的组成元素是第3周期原子半径最小的元素(稀有气体元素除外); 和
和 均由元素
均由元素 组成,
组成, 能氧化
能氧化 ,反应的离子方程式为
,反应的离子方程式为 。
。
(1)写出物质的分子式:
______ ,
______ ,
______ 。
(2) 与
与 的关系是
的关系是______ (填序号)。
a.互为同位素 b.属于同一物质
c.互为同素异形体 d.互为同分异构体
(3)导致大气中 减少的主要物质是
减少的主要物质是______ 。
(4)将 和二氧化硫分别通入品红溶液中,都能使品红溶液褪色。利用褪色的溶液区别二者的实验方法是
和二氧化硫分别通入品红溶液中,都能使品红溶液褪色。利用褪色的溶液区别二者的实验方法是________________________ 。
(5)举例说明 的氧化性比硫单质的氧化性强:
的氧化性比硫单质的氧化性强:________________________ (用化学方程式表示)。
 、
、 和
和 是三种气态单质。
是三种气态单质。 的组成元素是第3周期原子半径最小的元素(稀有气体元素除外);
的组成元素是第3周期原子半径最小的元素(稀有气体元素除外); 和
和 均由元素
均由元素 组成,
组成, 能氧化
能氧化 ,反应的离子方程式为
,反应的离子方程式为 。
。(1)写出物质的分子式:



(2)
 与
与 的关系是
的关系是a.互为同位素 b.属于同一物质
c.互为同素异形体 d.互为同分异构体
(3)导致大气中
 减少的主要物质是
减少的主要物质是(4)将
 和二氧化硫分别通入品红溶液中,都能使品红溶液褪色。利用褪色的溶液区别二者的实验方法是
和二氧化硫分别通入品红溶液中,都能使品红溶液褪色。利用褪色的溶液区别二者的实验方法是(5)举例说明
 的氧化性比硫单质的氧化性强:
的氧化性比硫单质的氧化性强:
您最近一年使用:0次
2020-03-02更新
|
220次组卷
|
2卷引用:高一必修第一册(苏教2019版)专题5 易错疑难集训(二)
名校
7 . X、Y、Z、M、W为五种短周期元素。X、Y、Z是原子序数依次递增的同周期元素,且最外层电子数之和为15,X与Z可形成XZ2分子;Y与M形成的气态化合物在标准状况下的密度为0.76g·L-1;W的质子数是X、Y、Z、M四种元素质子数之和的 。下列说法正确的是( )。
。下列说法正确的是( )。
 。下列说法正确的是( )。
。下列说法正确的是( )。| A.原子半径:W>Z>Y>X>M |
| B.XZ2、X2M2、W2Z2均为共价化合物 |
| C.M2Z2有强氧化性,分子中只有共价键 |
| D.由X、Y、Z、M四种元素形成的化合物可能既有离子键,又有共价键 |
您最近一年使用:0次
名校
8 . 如表是元素周期表主族元素的一部分,短周期元素X的最高正价是+5价,Y单质可在空气中燃烧。
(1)Z的元素符号是________ ,原子结构示意图是_________ 。
(2)W的最高价氧化物不溶于水,但能溶于烧碱溶液,反应的化学方程式为_________ 。
(3)探寻同一族元素性质的一些共同规律,是学习化学的重要方法之一。在下表中列出对H2ZO3各种不同化学性质的推测,举例并写出相应的化学方程式。
| W | X | Y |
| Z |
(1)Z的元素符号是
(2)W的最高价氧化物不溶于水,但能溶于烧碱溶液,反应的化学方程式为
(3)探寻同一族元素性质的一些共同规律,是学习化学的重要方法之一。在下表中列出对H2ZO3各种不同化学性质的推测,举例并写出相应的化学方程式。
| 编号 | 性质推测 | 化学方程式 |
| 示例 | 氧化性 | H2ZO3+4HI=Z↓+2I2+3H2O |
| 1 | ||
| 2 |
您最近一年使用:0次
9 . A、B、C、D、E是前20号元素,其原子序数依次增大。A、C两元素原子的电子层数相同,A元素原子的最外层电子数和次外层电子数分别与E元素原子的相同。A和C可形成化合物AC,D和E可形成化合物ED2,B元素原子最外层电子数比最内层电子数多1。
(1)这五种元素的名称和符号分别是_________________________________ 。
(2)AC、ED2的化学式分别是______________________________________ 。
(3)写出这五种元素最高价氧化物对应水化物的化学式,并分析其酸性、碱性强弱的变化情况______________________________________ 。
(4)C元素位于周期表第_________ 周期_________ 族。D元素的最高正化合价是_________________ 。
(1)这五种元素的名称和符号分别是
(2)AC、ED2的化学式分别是
(3)写出这五种元素最高价氧化物对应水化物的化学式,并分析其酸性、碱性强弱的变化情况
(4)C元素位于周期表第
您最近一年使用:0次
解题方法
10 . W、X、Y、Z、R是原子序数依次增大的短周期元素。a、b、c、d、e、f是由这些元素组成的化合物,气体a的水溶液呈碱性,c为红棕色气体,f是由W、Z、R元素形成的化合物。m为元素Z形成的单质,W与X能形成化合物XW4。上述物质的转化关系如图所示,下列说法正确的是( )
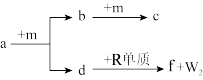
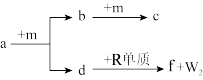
| A.简单离子半径: R>Z |
| B.最高价氧化物对应水化物的酸性:X>Y |
C. 为离子化合物,含有离子键和共价键 为离子化合物,含有离子键和共价键 |
| D.符合通式XnWn的化合物均能使溴的CCl4溶液因发生反应而褪色 |
您最近一年使用:0次



