1 . 国家卫生健康委员会发布公告称,富硒酵母、二氧化硅、硫黄等6种食品添加剂新品种安全性已通过审查,这些食品添加剂包括食品营养强化剂、风味改良剂、结构改善剂、防腐剂,用于食品生产中,将更好地满足吃货们的心愿,丰富舌尖上的营养和美味。请回答下列问题:
(1)富硒酵母是一种新型添加剂,其中硒元素在周期表中的位置为____ 。
(2)下列说法正确的是____ 。
A.热稳定性: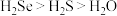 B.
B.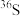 与
与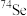 的中子数之和为60
的中子数之和为60
C.酸性: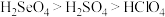 D.还原性:
D.还原性: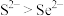
(3)短周期元素 、
、 、
、 、
、 、
、 、
、 都可能存在于某些食品添加剂中,其最高正化气价或最低负化合价与原子序数的关系如图所示:
都可能存在于某些食品添加剂中,其最高正化气价或最低负化合价与原子序数的关系如图所示:
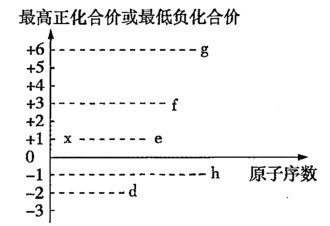
①由 、
、 、
、 三种元素组成的化合物的电子式为
三种元素组成的化合物的电子式为____ 。
② 、
、 、
、 、
、 、
、 元素形成的简单离子中半径最大的是
元素形成的简单离子中半径最大的是___ (用化学式表示),其结构示意图为___ 。
③ 和
和 组成的化合物中,既含有极性共价键又含有非极性共价键的是
组成的化合物中,既含有极性共价键又含有非极性共价键的是____ (填化学式),此化合物可将碱性工业废水中的 氧化,生成碳酸盐和氨气,相应的离子方程式为
氧化,生成碳酸盐和氨气,相应的离子方程式为____ 。
(1)富硒酵母是一种新型添加剂,其中硒元素在周期表中的位置为
(2)下列说法正确的是
A.热稳定性:
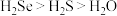 B.
B.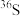 与
与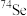 的中子数之和为60
的中子数之和为60C.酸性:
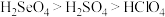 D.还原性:
D.还原性: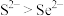
(3)短周期元素
 、
、 、
、 、
、 、
、 、
、 都可能存在于某些食品添加剂中,其最高正化气价或最低负化合价与原子序数的关系如图所示:
都可能存在于某些食品添加剂中,其最高正化气价或最低负化合价与原子序数的关系如图所示:
①由
 、
、 、
、 三种元素组成的化合物的电子式为
三种元素组成的化合物的电子式为②
 、
、 、
、 、
、 、
、 元素形成的简单离子中半径最大的是
元素形成的简单离子中半径最大的是③
 和
和 组成的化合物中,既含有极性共价键又含有非极性共价键的是
组成的化合物中,既含有极性共价键又含有非极性共价键的是 氧化,生成碳酸盐和氨气,相应的离子方程式为
氧化,生成碳酸盐和氨气,相应的离子方程式为
您最近一年使用:0次
2 . 元素周期表与元素周期律在化学学习研究中有很重要的作用。如表所示是五种元素的相关信息,W、X都位于第三周期。
(1)Q在元素周期表中的位置是________ 。
(2)W的最高价氧化物对应的水化物的化学式是_________ 。
(3)X单质与水反应的离子方程式是__________ 。
(4)金属性 ,用原子结构解释原因:
,用原子结构解释原因:_________ ,失电子能力 ,金属性
,金属性 。
。
(5)下列对于Z及其化合物的推断正确的是________ (填字母)。
A.Z的最低负化合价与W的最低负化合价相同
B.Z的氢化物的稳定性弱于W的氢化物的稳定性
C.Z的单质的氧化性强于W的单质的氧化性
元素 | 信息 |
Q | 地壳中含量最高 |
W | 最高化合价为+7 |
X | 最高价氧化物对应的水化物在第三周期中碱性最强 |
Y | 焰色试验(透过蓝色钴玻璃)火焰呈紫色 |
Z | 原子结构示意图为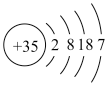 |
(2)W的最高价氧化物对应的水化物的化学式是
(3)X单质与水反应的离子方程式是
(4)金属性
 ,用原子结构解释原因:
,用原子结构解释原因: ,金属性
,金属性 。
。(5)下列对于Z及其化合物的推断正确的是
A.Z的最低负化合价与W的最低负化合价相同
B.Z的氢化物的稳定性弱于W的氢化物的稳定性
C.Z的单质的氧化性强于W的单质的氧化性
您最近一年使用:0次
解题方法
3 . 下列有关金属元素特征的叙述正确的是( )
| A.金属元素的原子只有还原性,离子只有氧化性 |
| B.金属元素在一般化合物中只显正价 |
| C.金属元素在不同的化合物中的化合价均不同 |
| D.金属元素的单质在常温下均为金属晶体 |
您最近一年使用:0次
2020-01-08更新
|
218次组卷
|
2卷引用:课时1 金属晶体——A学习区 夯实基础(鲁科版选修3)
解题方法
4 . 现有下列短周期元素的数据(已知 的原子半径为
的原子半径为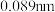 ):
):
(1)③号元素在周期表中的位置是______ ;上述元素处于同一主族的有______ (用元素符号表示)。
(2)元素①和⑥能形成两种化合物,写出其中较稳定的化合物与水反应的离子方程式:__________________ 。
(3)含锂材料在社会中广泛应用,如各种储氢材料(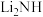 等)、便携式电源材料(
等)、便携式电源材料( 等)。根据下列要求回答问题:
等)。根据下列要求回答问题:
① 和
和 作核反应堆最佳热载体,
作核反应堆最佳热载体,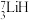 和
和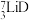 用作高温堆减速剂。下列说法正确的是
用作高温堆减速剂。下列说法正确的是______ (填序号)。
A. 和
和 互为同位素 B.
互为同位素 B. 和
和 属于同种核素
属于同种核素
C.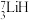 和
和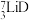 的化学性质不同 D.
的化学性质不同 D.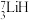 和
和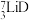 是同种物质
是同种物质
②下列说法不正确的是______ (填序号)。
A.碱性:
B.微粒半径: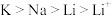
C.氧化性: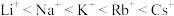
D.金属性:
 的原子半径为
的原子半径为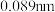 ):
):| ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |
原子半径/ | 0.074 | 0.160 | 0.152 | 0.110 | 0.099 | 0.186 | 0.075 | 0.082 |
| 最高化合价 |  | 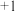 |  | 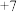 | 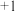 |  |  | |
| 最低化合价 |  |  |  |  |
(1)③号元素在周期表中的位置是
(2)元素①和⑥能形成两种化合物,写出其中较稳定的化合物与水反应的离子方程式:
(3)含锂材料在社会中广泛应用,如各种储氢材料(
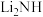 等)、便携式电源材料(
等)、便携式电源材料( 等)。根据下列要求回答问题:
等)。根据下列要求回答问题:①
 和
和 作核反应堆最佳热载体,
作核反应堆最佳热载体,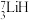 和
和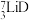 用作高温堆减速剂。下列说法正确的是
用作高温堆减速剂。下列说法正确的是A.
 和
和 互为同位素 B.
互为同位素 B. 和
和 属于同种核素
属于同种核素C.
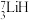 和
和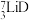 的化学性质不同 D.
的化学性质不同 D.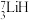 和
和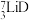 是同种物质
是同种物质②下列说法不正确的是
A.碱性:

B.微粒半径:
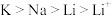
C.氧化性:
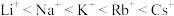
D.金属性:

您最近一年使用:0次
15-16高二下·重庆·阶段练习
名校
5 . 前四周期元素X、Y、Z、W核电荷数依次增大,核电荷数之和为58;Y原子的M层p轨道有3个未成对电子;Z与Y同周期,且在该周期中电负性最大;W原子的L层电子数与最外层电子数之比为4:1,其d轨道中的电子数与最外层电子数之比为5:2。
(1)写出Z元素在元素周期表中的位置:___________ 。
(2) 与X形成共价化合物A,Z与X形成共价化合物B,A与B还原性较强的是
与X形成共价化合物A,Z与X形成共价化合物B,A与B还原性较强的是___________  写分子式
写分子式 。
。
(3) 的最高价氧化物的水化物的化学式为
的最高价氧化物的水化物的化学式为___________ ;
(4) 单质
单质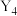 与
与 在一定条件下恰好完全反应生成
在一定条件下恰好完全反应生成 化合物C,一个C分子中所含有的σ键数目为
化合物C,一个C分子中所含有的σ键数目为___________ ;
(5)含W元素的最高化合价的含氧酸根离子是___________ ,该含氧酸根离子在分析化学中有重要作用,在酸性条件下该含氧酸根离子可将 氧化成
氧化成 ,请写出该反应的离子方程式
,请写出该反应的离子方程式___________ 。
(1)写出Z元素在元素周期表中的位置:
(2)
 与X形成共价化合物A,Z与X形成共价化合物B,A与B还原性较强的是
与X形成共价化合物A,Z与X形成共价化合物B,A与B还原性较强的是 写分子式
写分子式 。
。(3)
 的最高价氧化物的水化物的化学式为
的最高价氧化物的水化物的化学式为(4)
 单质
单质 与
与 在一定条件下恰好完全反应生成
在一定条件下恰好完全反应生成 化合物C,一个C分子中所含有的σ键数目为
化合物C,一个C分子中所含有的σ键数目为(5)含W元素的最高化合价的含氧酸根离子是
 氧化成
氧化成 ,请写出该反应的离子方程式
,请写出该反应的离子方程式
您最近一年使用:0次
2021-04-21更新
|
553次组卷
|
5卷引用:4.3化学键-同步学习必备知识
20-21高三·广东茂名·阶段练习
6 . 短周期主族元素W、X、Y、Z的原子序数依次增大,Z最高价氧化物的水化物酸性在短周期主族元素最高价氧化物的水化物中最强,X为ⅠA元素,W的核外电子数与X、Z的最外层电子数之和相等,Y的原子序数是Z的最外层电子数的2倍。下列叙述正确的是
| A.元素最高化合价的顺序为Z>W>Y>X |
| B.氢化物的稳定性的顺序为W>Y>Z |
| C.X、Y分别与W形成的二元化合物的熔点比较:Y>X |
| D.W、X、Z形成的化合物只具氧化性 |
您最近一年使用:0次
15-16高三下·福建泉州·阶段练习
7 . X、Y、Z、W均为短周期元素,原子序数依次增大。Y原子的M电子层有1个电子,同周期的简单离子的半径中Z最小。W与X同主族,其最高化合价是最低负化合价绝对值的3倍。下列说法正确的是( )
| A.最高价氧化物水化物的碱性:Y<Z |
| B.简单气态氢化物的热稳定性:X<W |
| C.X分别与Z、W形成化合物的熔点:Z<W |
| D.简单离子的还原性:X<W |
您最近一年使用:0次
2016-12-09更新
|
140次组卷
|
5卷引用:4.2.2 元素周期表和元素周期律的应用(精练)-2020-2021学年上学期高一化学同步精品课堂(人教版必修第一册)
(已下线)4.2.2 元素周期表和元素周期律的应用(精练)-2020-2021学年上学期高一化学同步精品课堂(人教版必修第一册)2016届福建省泉州市高中毕业班3月质量检查理综化学试卷2015-2016学年河南师大附中高二下期末理综化学试卷2016-2017学年河北省唐山一中高一下学期3月月考化学试卷内蒙古包头稀土高新区第二中学2019-2020高一下学期月考化学试题
解题方法
8 . 短周期主族元素X、Y、Z、W的原子序数依次增大,K、L、M均是由这些元素组成的氧化物;甲、乙分别是元素Y、W的单质,甲是常见的固体,乙是常见的气体;K是红棕色气体;丙的浓溶液具有强氧化性。上述物质的转化关系如图所示。下列说法不正确的是
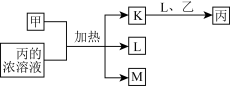

| A.K、L、M形成的晶体都是分子晶体 |
| B.X和Z形成的分子晶体中一定不存在非极性键 |
| C.L的沸点一定比X、Y组成的化合物沸点高 |
| D.由X、Y、Z、W构成的化合物中可能只含有共价键 |
您最近一年使用:0次
名校
解题方法
9 . X、Y、Z、W四种主族元素,原子序数依次增大,且均不大于20,四种元素核电荷数之和为46,X、Y两种元素能够形成两种化合物,其中一种化合物被称为生命的源泉。Z元素是一种重要的“成盐元素”,其形成的一种盐在海水中含量最高,其单质通过电解该盐溶液获得。下列关于四种元素说法错误的是( )
| A.X2Y2、ZY2、W(ZY)2均是常见的杀菌消毒剂,三者作用原理相同 |
| B.WX2中X元素的检验方法可以将WX2固体置于氧气流中灼烧并将产物通过无水硫酸铜 |
| C.WZ2、WY2两种化合物中阴阳离子个数比均为2:1 |
| D.XZY属于弱电解质,且具有强氧化性 |
您最近一年使用:0次
2022-12-15更新
|
507次组卷
|
4卷引用:模块检测卷2
名校
解题方法
10 . X、Y、Z、W、R、Q为原子序数依次增大的六种短周期主族元素。X是原子半径最小的元素;Y原子最外层电子数是核外电子层数的3倍;Z是短周期中金属性最强的元素;W是地壳中含量最多的金属元素;R的最高正价与最低负价代数和为4。请回答下列问题:
(1)Y的元素名称是______ 。
(2)W在周期表中的位置是______ 。
(3)写出化合物Z2R的电子式______ 。
(4)写出化合物X2Y2的结构式______ 。
(5)Y、Z、W三种元素对应的简单离子半径由大到小的顺序是______ (用元素的离子符号表示)。
(6)下列说法能证明非金属性Q强于R的是______ (填序号)。
a.简单阴离子的还原性:Q>R
b.简单氢化物热稳定性:Q>R
c.氧化物对应的水化物的酸性: Q>R
(7)W的单质与Z的最高价氧化物对应的水化物反应的化学方程式是______ 。
(1)Y的元素名称是
(2)W在周期表中的位置是
(3)写出化合物Z2R的电子式
(4)写出化合物X2Y2的结构式
(5)Y、Z、W三种元素对应的简单离子半径由大到小的顺序是
(6)下列说法能证明非金属性Q强于R的是
a.简单阴离子的还原性:Q>R
b.简单氢化物热稳定性:Q>R
c.氧化物对应的水化物的酸性: Q>R
(7)W的单质与Z的最高价氧化物对应的水化物反应的化学方程式是
您最近一年使用:0次
2021-01-19更新
|
590次组卷
|
5卷引用:第四章 物质结构 元素周期律 综合拔高练



