广东省茂名市长坡中学2022届高三8月模拟化学试题
广东
高三
阶段练习
2021-09-11
216次
整体难度:
适中
考查范围:
认识化学科学、有机化学基础、化学与STSE、常见无机物及其应用、化学反应原理、物质结构与性质、化学实验基础
广东省茂名市长坡中学2022届高三8月模拟化学试题
广东
高三
阶段练习
2021-09-11
216次
整体难度:
适中
考查范围:
认识化学科学、有机化学基础、化学与STSE、常见无机物及其应用、化学反应原理、物质结构与性质、化学实验基础
一、单选题 添加题型下试题
单选题
|
适中(0.65)
名校
解题方法
1. 2020年全球爆发了新冠肺炎疫情,2020年1月30日晚,世界卫生组织(WHO)宣布,将新型冠状病毒疫情列为国际关注的突发公共卫生事件(PHEIC)。世界卫生组织3月11日表示,新冠肺炎疫情的爆发已经构成一次全球性“大流行”。下列说法正确 的是
| A.人们用乙醇、次氯酸钠溶液均可以将病毒氧化而达到消毒的目的 |
| B.卫生防疫专家强调,目前可以确定的新冠肺炎传播途径主要为直接传播、气溶胶传播和接触传播。气溶胶是一种胶体,属于胶体分散系,分散剂是空气中的水珠,气溶胶能发生丁达尔现象 |
| C.抗体的化学本质是维生素 |
| D.2019年6月25日,生活垃圾分类制度将入法。上海成为第一个中国垃圾分类试点城市。垃圾一般可分为:可回收物、厨余垃圾、有害垃圾、其它垃圾。废弃口罩属于有害垃圾 |
您最近一年使用:0次
2021-09-09更新
|
314次组卷
|
3卷引用:广东省茂名市长坡中学2022届高三8月模拟化学试题
广东省茂名市长坡中学2022届高三8月模拟化学试题(已下线)第二单元 化学物质及其变化(B卷 真题滚动练)-2022年高考化学一轮复习单元滚动双测卷(新高考地区专用)江西省新余市第一中学2021-2022学年高三上学期第二次模拟考试化学试题
单选题
|
适中(0.65)
2. 疫情当前,春耕在即。各级人民政府坚持疫情防控和农业农村工作“两手硬”,全面推进复耕备耕助农抗疫增收工作。己唑醇(结构如图)属唑类杀菌剂,对真菌(尤其是担子菌纲和子囊菌纲)引起的病害有广谱性的保护和铲除作用。适宜作物与安全性果树如苹果、葡萄、香蕉,蔬菜(瓜果、辣椒等),花生,咖啡,禾谷类作物和观赏植物等。下列有关“己唑醇”的说法正确的是


| A.它的分子式为C14H20Cl2N3O |
| B.它含有羟基、氯原子、碳碳双键等官能团 |
| C.1mol己唑醇最多能和2molH2发生加成反应 |
| D.一定条件下它能发生水解反应、酯化反应、消去反应、氧化反应、加成反应等 |
您最近一年使用:0次
单选题
|
适中(0.65)
3. 二氧化硫是最常见、最简单、有刺激性的硫氧化物。大气主要污染物之一。火山爆发时会喷出该气体,在许多工业过程中也会产生二氧化硫。由于煤和石油通常都含有硫元素,因此燃烧时会生成二氧化硫。当二氧化硫溶于水中,会形成亚硫酸。若把亚硫酸进一步在PM2.5存在的条件下氧化,便会迅速高效生成硫酸(酸雨的主要成分)。某学校化学兴趣小组对SO2的化学性质进行如图的探究。
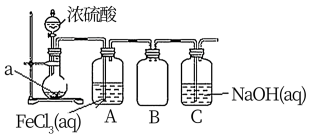
下列说法错误的是

下列说法错误的是
A.A瓶反应后的离子方程式:2Fe3++SO2+2H2O=2Fe2++SO +4H+ +4H+ |
| B.B瓶的作用为防倒吸 |
| C.C瓶用于吸收未反应的SO2 |
| D.烧瓶中放入的药品a为Cu |
您最近一年使用:0次
单选题
|
适中(0.65)
4. NA为阿伏加德罗常数的值,下列说法正确的是
| A.1L0.5mol/L的KMnO4溶液中,氧原子的总数为2NA |
| B.1mol熔融状态的NH4HSO4中含1NA个H+ |
| C.1L5mol/L的浓盐酸与足量MnO2共热,完全反应可生成1.25NA个Cl2分子 |
| D.NaBH4燃料电池正极消耗22.4L(标准状况)气体时,电路中通过的电子数目为4NA |
您最近一年使用:0次
单选题
|
适中(0.65)
5. 短周期主族元素W、X、Y、Z的原子序数依次增大,Z最高价氧化物的水化物酸性在短周期主族元素最高价氧化物的水化物中最强,X为ⅠA元素,W的核外电子数与X、Z的最外层电子数之和相等,Y的原子序数是Z的最外层电子数的2倍。下列叙述正确的是
| A.元素最高化合价的顺序为Z>W>Y>X |
| B.氢化物的稳定性的顺序为W>Y>Z |
| C.X、Y分别与W形成的二元化合物的熔点比较:Y>X |
| D.W、X、Z形成的化合物只具氧化性 |
您最近一年使用:0次
单选题
|
适中(0.65)
解题方法
6. 25℃,Ksp[Fe(OH)3]=4.0×10-38,向10mL0.1mol/L的FeCl3溶液中加入30mL0.1mol/L的NaOH溶液发生反应,混合溶液中c(Fe3+)与时间(t)的变化如图所示。

下列说法正确的是

下列说法正确的是
| A.A点Fe3+的浓度0.1mol/L |
| B.25℃,Fe3+发生水解常数为2.5×10-5 |
| C.C点存在的平衡主要为Fe3+的水解平衡 |
| D.t4时向溶液中加入10mL0.1mol/LNaCl溶液,平衡不移动 |
【知识点】 沉淀溶解平衡的应用
您最近一年使用:0次
2021-09-09更新
|
166次组卷
|
3卷引用:广东省茂名市长坡中学2022届高三8月模拟化学试题
单选题
|
适中(0.65)
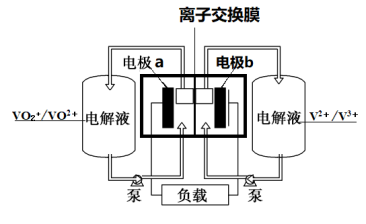
7. 全钒液流电池(VanadiumRedoxFlowBattery,VRB),是一种以钒为活性物质呈循环流动液态的氧化还原电池。钒电池电能以化学能的方式存储在不同价态钒离子的硫酸电解液中,通过外接泵把电解液压入电池堆体内,在机械动力作用下,使其在不同的储液罐和半电池的闭合回路中循环流动,采用质子交换膜作为电池组的隔膜,电解质溶液平行流过电极表面并发生电化学反应,通过双电极板收集和传导电流,从而使得储存在溶液中的化学能转换成电能。全钒液流电池:VO +2H++V2+
+2H++V2+ V3++VO2++H2O
V3++VO2++H2O
 +2H++V2+
+2H++V2+ V3++VO2++H2O
V3++VO2++H2O
| A.放电时该装置中b电极发生氧化反应 |
B.放电时正极反应式为VO +2H++e-=VO2++H2O +2H++e-=VO2++H2O |
| C.理论上,充电时当电路中通过3mole-时,必有6molH+由b极区向a极区迁移 |
| D.充电时阴极反应式为:V3++e-=V2+ |
您最近一年使用:0次
二、解答题 添加题型下试题
解答题-实验探究题
|
适中(0.65)
解题方法
8. 乙酸正丁酯,简称乙酸丁酯。无色透明有愉快果香气味的液体。较低级同系物难溶于水;与醇、醚、酮等有机溶剂混溶。易燃。急性毒性较小,但对眼鼻有较强的刺激性,而且在高浓度下会引起麻醉。乙酸正丁酯是一种优良的有机溶剂,对乙基纤维素、醋酸丁酸纤维素、聚苯乙烯、甲基丙烯酸树脂、氯化橡胶以及多种天然树胶均有较好的溶解性能。实验室制备乙酸正丁酯的化学方程式CH3COOH+CH3CH2CH2CH2OH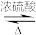 CH3COOCH2CH2CH2CH3+H2O。
CH3COOCH2CH2CH2CH3+H2O。
主要实验步骤如下:
①干燥的圆底烧瓶中加12.0mL正丁醇、16.0mL冰醋酸(过量)和3~4滴浓H2SO4,摇匀后,加几粒沸石,再如图1装置安装好分水器(作用:实验过程中不断分离除去反应生成的水)、冷凝管。然后小火加热。

②将烧瓶中反应后的混后物冷却与分水器中的酯层合并,转入分液漏斗,
③依次用10mL水,10mL10%碳酸钠溶液洗至无酸性(pH=7),再水洗一次,用少许无水硫酸镁干燥。
④将干燥后的乙酸正丁酯转入50mL蒸馏烧瓶中,加几粒沸石进行常压蒸馏,收集产品。主要试剂及产物的物理常数:
根据以上信息回答下列问题。
(1)图Ⅰ装置中冷水应从___ (填a或b)管口通入,反应混合物冷凝回流,通过分水器不断分离除去反应生成的水的目的是___ 。
(2)在洗涤、分液操作中,应充分振荡,然后静置,待分层后___ (填标号)。
(3)在步骤③分液时,应选择图Ⅱ装置中___ 形分液漏斗,其原因是___ 。

(4)在提纯粗产品的过程中,用碳酸钠溶液洗涤主要除去___ 的杂质。若改用氢氧化钠溶液是否可以___ (填“可以”或“不可以”),其原因___ 。
(5)计算产率
测量分水器内由乙酸与丁醇反应生成的水体积为1.8mL,假设在制取乙酸丁酯过程中反应物和生成物没有损失,且忽略副反应,乙酸丁酯的产率为___ 。
 CH3COOCH2CH2CH2CH3+H2O。
CH3COOCH2CH2CH2CH3+H2O。主要实验步骤如下:
①干燥的圆底烧瓶中加12.0mL正丁醇、16.0mL冰醋酸(过量)和3~4滴浓H2SO4,摇匀后,加几粒沸石,再如图1装置安装好分水器(作用:实验过程中不断分离除去反应生成的水)、冷凝管。然后小火加热。

②将烧瓶中反应后的混后物冷却与分水器中的酯层合并,转入分液漏斗,
③依次用10mL水,10mL10%碳酸钠溶液洗至无酸性(pH=7),再水洗一次,用少许无水硫酸镁干燥。
④将干燥后的乙酸正丁酯转入50mL蒸馏烧瓶中,加几粒沸石进行常压蒸馏,收集产品。主要试剂及产物的物理常数:
| 乙酸 | 正丁醇 | 乙酸丁酯 | |
| 熔点/℃ | 16.6 | -89.5 | -73.5 |
| 沸点/℃ | 117.9 | 117 | 126.0 |
| 密度/g·cm-3 | 1.1 | 0.80 | 0.88 |
(1)图Ⅰ装置中冷水应从
(2)在洗涤、分液操作中,应充分振荡,然后静置,待分层后
| A.直接将乙酸丁酯从分液漏斗的上口倒出 |
| B.直接将乙酸丁酯从分液漏斗的下口放出 |
| C.先将水层从分液漏斗的下口放出,再将乙酸丁酯从下口放出 |
| D.先将水层从分液漏斗的下口放出,再将乙酸丁酯从上口倒出 |

(4)在提纯粗产品的过程中,用碳酸钠溶液洗涤主要除去
(5)计算产率
测量分水器内由乙酸与丁醇反应生成的水体积为1.8mL,假设在制取乙酸丁酯过程中反应物和生成物没有损失,且忽略副反应,乙酸丁酯的产率为
您最近一年使用:0次
解答题-工业流程题
|
适中(0.65)
9. 以电石渣为主要原料,实现了废物的资源化利用,有较高的应用价值,电石渣呈灰色,并伴有刺鼻的气味,以电石渣[主要成分为Ca(OH)2,含少量MgO,SiO2,Al2O3,碳渣等杂质]为原料制备高纯活性纳米CaCO3的流程如图:
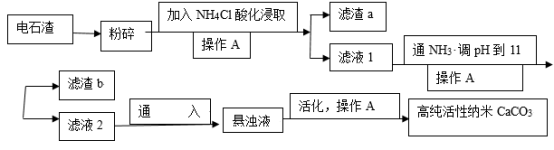
(1)操作A的名称是____ ,加入NH4Cl可以酸化溶液,请用离子方程式来表示可以酸化的原因___
(2)滤渣a中含有___ ,向滤液1中通入NH3调节溶液pH,主要目的是:①使滤液2能吸收更多CO2,②___ 。写出通入CO2生成悬浊液的化学方程式____ 。
(3)流程中可循环利用的物质是___ 和___ 。
(4)电石渣在运输、贮存过程中避免与___ 物质接触。高纯活性纳米CaCO3在生产生活中可用于油墨和造纸等工业的填料,也可用于化妆品、儿童牙膏等日化产品。请写出你知道的CaCO3的其他用途__ (任写两点)。

| 物质 | 开始沉淀pH | 完全沉淀pH |
| Mg(OH)2 | 9.8 | 10.8 |
| Al(OH)3 | 3.2 | 4.7 |
(1)操作A的名称是
(2)滤渣a中含有
(3)流程中可循环利用的物质是
(4)电石渣在运输、贮存过程中避免与
您最近一年使用:0次
解答题-原理综合题
|
适中(0.65)
10. 由H、C、N、O、S等元素形成多种化合物在生产生活中有着重要应用。
(1)以CO2与NH3为原料可合成化肥尿素[化学式为CO(NH2)2]。
已知:①2NH3(g)+CO2(g)=NH2CO2NH4(s) ΔH=-159.5kJ/mol
②NH2CO2NH4(s)=CO(NH2)2(s)+H2O(g) ΔH=+116.5kJ/mol
③H2O(l)=H2O(g) ΔH=+44.0kJ/mol
写出CO2与NH3合成尿素同时生成液态水的热化学反应方程式:___ 。
(2)某密闭容器中存在反应:CO(g)+2H2(g) CH3OH(g),起始时容器中只有amol/LCO和bmol/LH2,平衡时测得混合气体中CH3OH的物质的量分数[φ(CH3OH)]与温度(T)、压强(p)之间的关系如图所示。
CH3OH(g),起始时容器中只有amol/LCO和bmol/LH2,平衡时测得混合气体中CH3OH的物质的量分数[φ(CH3OH)]与温度(T)、压强(p)之间的关系如图所示。

①温度T1和T2时对应的平衡常数分别为K1、K2,则K1___ K2(填“>”“<”或“=”);若恒温(T1)恒容条件下,起始时a=1、b=2,测得平衡时混合气体的压强为p1kPa,则T1时该反应的压强平衡常数Kp=___ 。(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数,用含p1的代数式表示)
②若恒温恒容条件下,起始时充入1molCO和2molH2,达平衡后,CO的转化率为α1,此时,若再充入1molCO和2molH2,再次达平衡后,CO的转化率为α2,则α1___ α2(填“>”“<”“=”或“无法确定”)。
(3)最近有人尝试用H2还原工业尾气中SO2,该反应分两步完成,如图1所示,该过程中相关物质的物质的量浓度随时间的变化关系如图2所示:


①分析可知X为__ (写化学式),0~t1时间段的温度为__ ,0~t1时间段用SO2表示的化学反应速率为___ 。
②总反应的化学方程式为__ 。
(1)以CO2与NH3为原料可合成化肥尿素[化学式为CO(NH2)2]。
已知:①2NH3(g)+CO2(g)=NH2CO2NH4(s) ΔH=-159.5kJ/mol
②NH2CO2NH4(s)=CO(NH2)2(s)+H2O(g) ΔH=+116.5kJ/mol
③H2O(l)=H2O(g) ΔH=+44.0kJ/mol
写出CO2与NH3合成尿素同时生成液态水的热化学反应方程式:
(2)某密闭容器中存在反应:CO(g)+2H2(g)
 CH3OH(g),起始时容器中只有amol/LCO和bmol/LH2,平衡时测得混合气体中CH3OH的物质的量分数[φ(CH3OH)]与温度(T)、压强(p)之间的关系如图所示。
CH3OH(g),起始时容器中只有amol/LCO和bmol/LH2,平衡时测得混合气体中CH3OH的物质的量分数[φ(CH3OH)]与温度(T)、压强(p)之间的关系如图所示。
①温度T1和T2时对应的平衡常数分别为K1、K2,则K1
②若恒温恒容条件下,起始时充入1molCO和2molH2,达平衡后,CO的转化率为α1,此时,若再充入1molCO和2molH2,再次达平衡后,CO的转化率为α2,则α1
(3)最近有人尝试用H2还原工业尾气中SO2,该反应分两步完成,如图1所示,该过程中相关物质的物质的量浓度随时间的变化关系如图2所示:


①分析可知X为
②总反应的化学方程式为
您最近一年使用:0次
解答题-有机推断题
|
适中(0.65)
11. 盐酸阿比朵尔是一种广谱抗病毒药物。在新冠肺炎疫情爆发初期就有医生表示在尝试给患者使用。中国工程院院士李兰娟团队的研究称,该药在体外实验中对新冠病毒有抑制作用。盐酸阿比朵尔的合成过程如图:

已知:①Ac2O为乙酸酐(CH3COOCOCH3)
苯酚与乙酸酐反应:CH6CH5OH+CH3COOCOCH3→CH6CH5OCOCH3+CH3COOH
②CH3COOC2H5+CH3COOC2H5 CH3COCH2COOC2H5+C2H5OH
CH3COCH2COOC2H5+C2H5OH
(1)有机物A的名称是:___ ;E→F的反应类型为:___ 。
(2)写出G含氧官能团名称:___ 。
(3)B→C反应的化学方程式为___ 。
(4)与B互为同分异构体且苯环上有两个取代基、能发生银镜反应、含硝基的同分异构体有___ 种;其中核磁共振氢谱图中峰面积比为1∶2∶2∶2的同分异构体的结构简式为:___ 。
(5)请设计以乙醇和 为主要原料(其它试剂自选)合成
为主要原料(其它试剂自选)合成 化合物的合成路线流程图:
化合物的合成路线流程图:___ 。

已知:①Ac2O为乙酸酐(CH3COOCOCH3)
苯酚与乙酸酐反应:CH6CH5OH+CH3COOCOCH3→CH6CH5OCOCH3+CH3COOH
②CH3COOC2H5+CH3COOC2H5
 CH3COCH2COOC2H5+C2H5OH
CH3COCH2COOC2H5+C2H5OH(1)有机物A的名称是:
(2)写出G含氧官能团名称:
(3)B→C反应的化学方程式为
(4)与B互为同分异构体且苯环上有两个取代基、能发生银镜反应、含硝基的同分异构体有
(5)请设计以乙醇和
 为主要原料(其它试剂自选)合成
为主要原料(其它试剂自选)合成 化合物的合成路线流程图:
化合物的合成路线流程图:【知识点】 有机反应类型 同分异构体的数目的确定解读 酯的化学性质 有机物的推断
您最近一年使用:0次
试卷分析
整体难度:适中
考查范围:认识化学科学、有机化学基础、化学与STSE、常见无机物及其应用、化学反应原理、物质结构与性质、化学实验基础
试卷题型(共 11题)
题型
数量
单选题
7
解答题
4
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.65 | 胶体的性质和应用 乙醇的物理性质 蛋白质的变性 化学科学对人类文明发展的意义 | |
| 2 | 0.65 | 有机反应类型 加成反应 多官能团有机物的结构与性质 胺的性质与应用 | |
| 3 | 0.65 | 二氧化硫的化学性质 二氧化硫的制备 浓硫酸的强氧化性 | |
| 4 | 0.65 | 22.4L/mol适用条件 结合氧化还原反应知识与NA相关推算 氯气的实验室制法 原电池有关计算 | |
| 5 | 0.65 | 元素周期律的应用 元素金属性与非金属性递变规律的理解及应用 由元素性质的递变规律进行相关推断 根据物质性质进行元素种类推断 | |
| 6 | 0.65 | 沉淀溶解平衡的应用 | |
| 7 | 0.65 | 原电池正负极判断 原电池电极反应式书写 电解池电极反应式及化学方程式的书写与判断 原电池有关计算 | |
| 二、解答题 | |||
| 8 | 0.65 | 羧酸酯化反应 常见有机物的制备 | 实验探究题 |
| 9 | 0.65 | 水解的离子方程式书写 沉淀的溶解与生成 物质分离、提纯综合应用 物质制备的探究 | 工业流程题 |
| 10 | 0.65 | 盖斯定律的应用 化学反应速率计算 化学平衡的移动及其影响因素 化学平衡常数的有关计算 | 原理综合题 |
| 11 | 0.65 | 有机反应类型 同分异构体的数目的确定 酯的化学性质 有机物的推断 | 有机推断题 |



