1 . 已知X、W、Z、Y为原子半径依次增大的短周期元素,其形成的生活中常见的一种化合物结构如图所示。下列叙述正确的是
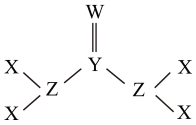

| A.W的单质一定属于非极性分子 |
| B.电负性: W>Z>Y |
| C.该化合物中Y、Z的杂化方式为sp3 |
D.-ZX2、 ZX3、 均为10电子粒子 均为10电子粒子 |
您最近一年使用:0次
2 . 短周期主族元素A、B、C、D、E常见稳定结构、相关信息、性质如表:
下列说法一定正确的是
| A+ | B2- | C | D的简单氢化物 | E的氢化物的水溶液 |
| 电子数为0 | 离子半径140pm | 常见化合价-2、+4、+6 | 正四面体 | 强酸溶液 |
| A.简单阴离子还原性:E>C |
| B.D与A形成的化合物的沸点低于B与A形成的化合物的沸点 |
| C.B和E形成的其中一种化合物具有强氧化性 |
| D.C的简单离子半径小于140pm |
您最近一年使用:0次
名校
解题方法
3 . W、X、Y、Z为原子序数依次增大的短周期主族元素,W、X处于不同周期,原子的最外层电子数X比Y多一个但比Z少一个。下列说法正确的是( )
| A.原子半径的大小:Z>Y>X>W |
| B.若X的单质为常见的非金属导体,则Y的简单离子能破坏水的电离平衡 |
| C.元素的非金属性:Y>Z |
| D.若Y、Z的核电荷数之和为X的4倍,则X、Z的气态氢化物的沸点:前者低于后者 |
您最近一年使用:0次
2020-07-16更新
|
189次组卷
|
4卷引用:四川省成都市第七中学2019-2020学年高二下学期零诊模拟考试化学
名校
解题方法
4 . 如图是元素周期表的一部分:
(1)元素⑩原子结构示意图为__________ 。
(2)元素③④的第一电离能大小关系为_______ (填化学用语,下同),原因是__________________ ,④-⑧中最高价氧化物对应水化物酸性最强的是_______ 。
(3)写出元素⑦的最高价氧化物与NaOH溶液反应的离子方程式_________ 。
(4)元素⑤ 与⑧ 元素相比,非金属性较强的是__________ (用元素符号表示),下列表述中能证明这一事实的是__________ 。
A.气态氢化物的挥发性和稳定性 B.两元素的电负性
C.单质分子中的键能 D.含氧酸的酸性
E.氢化物中X—H键的键长 F.两单质在自然界中的存在形式
(5)根据下列五种元素的第一至第四电离能数据(单位:KJ·mol﹣1),回答下面各题:
①T元素最可能是________ (填“s”、“p”、“d”、“ds”等)区元素;在周期表中,最可能处于同一主族的是_________ 。(填元素代号 );
②下列离子的氧化性最弱的是______________ 。
A.S2+ B.R2+ C.U+ D.T3+

(1)元素⑩原子结构示意图为
(2)元素③④的第一电离能大小关系为
(3)写出元素⑦的最高价氧化物与NaOH溶液反应的离子方程式
(4)元素⑤ 与⑧ 元素相比,非金属性较强的是
A.气态氢化物的挥发性和稳定性 B.两元素的电负性
C.单质分子中的键能 D.含氧酸的酸性
E.氢化物中X—H键的键长 F.两单质在自然界中的存在形式
(5)根据下列五种元素的第一至第四电离能数据(单位:KJ·mol﹣1),回答下面各题:
| 元素代号 | I1 | I2 | I3 | I4 |
| Q | 2080 | 4000 | 6100 | 9400 |
| R | 500 | 4600 | 6900 | 9500 |
| S | 740 | 1500 | 7700 | 10500 |
| T | 580 | 1800 | 2700 | 11600 |
| U | 420 | 3100 | 4400 | 5900 |
②下列离子的氧化性最弱的是
A.S2+ B.R2+ C.U+ D.T3+
您最近一年使用:0次
2018-04-19更新
|
197次组卷
|
2卷引用:福建省华安一中、长泰一中等四校2017-2018学年高二下学期第一次(4月)联考化学试题
5 . W、X、Y、Z是原子半径依次增大的四种短周期主族元素,已知25℃时,W、Z形成的0.01mol.L-1化合物的水溶液pH=2,X3-电子层结构与氖元素相同,Y的最外层电子数是电子层数的2倍。
(1)Z在元素周期表中位置是_____________ 。
(2)(YX)2结构与卤素单质相似,组成原子均满足8电子稳定结构,(YX)2的结构式为
________ (元素符号表示)。
(3)W、X、Z组成的一种常见化合物可用作焊接金属的除锈剂,该化合物的水溶液与Mg反应有两种气体产生,其中一种气体有刺激性气味,该反应的离子方程式为____________ 。该化合物的稀溶液与稀NaOH溶液混合(不考虑含X微粒的分解和挥发等),所得溶液呈中性,则含X的分子的浓度_________ c(Na+)(填“大于”、“小于”或“等于”)。
(4)XZ3在湿气中易水解生成一种常见的漂白剂,且反应为非氧化还原反应,该反应的化学方程式为__________________________ 。
(1)Z在元素周期表中位置是
(2)(YX)2结构与卤素单质相似,组成原子均满足8电子稳定结构,(YX)2的结构式为
(3)W、X、Z组成的一种常见化合物可用作焊接金属的除锈剂,该化合物的水溶液与Mg反应有两种气体产生,其中一种气体有刺激性气味,该反应的离子方程式为
(4)XZ3在湿气中易水解生成一种常见的漂白剂,且反应为非氧化还原反应,该反应的化学方程式为
您最近一年使用:0次
2018-03-26更新
|
159次组卷
|
2卷引用:湖北孝感高中等五校2017-2018学年高二上学期期末联考化学试题
解题方法
6 . 有关物质的转化关系如下图所示。常温下,B、E呈气态,其中B呈黄绿色。D是最常见的无色液体,E常用作制冷剂,F是一种不溶于水的碱,G是厨房中的常见调味品,H由两种元素组成,其摩尔质量为32 g·mol-1。
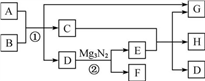
(1) E的电子式为____ 。
(2) H的化学式为____ 。
(3) 写出反应①的离子方程式:_________________ 。
(4) 写出反应②的化学方程式:_________________ 。

(1) E的电子式为
(2) H的化学式为
(3) 写出反应①的离子方程式:
(4) 写出反应②的化学方程式:
您最近一年使用:0次
名校
7 . 甲~辛等元素在周期表中的位置如下表所示。下列说法正确的是


| A.甲、丁、戊的单质都是金属 |
| B.乙、丙、辛都是非金属元素 |
| C.乙、庚、辛都能形成氧化物 |
| D.已的氧化物既可溶于KOH溶液又可溶于H2SO4溶液 |
您最近一年使用:0次
2016-07-12更新
|
150次组卷
|
6卷引用:广东省汕头市达濠华侨中学2017-2018学年高二下学期阶段联考(一)化学试题



