1 . 元素周期表是学习化学的重要工具,它隐含着许多信息和规律。下表列出了七种元素在元素周期表中的位置,回答下列问题:
(1)表中C在周期表的位置是___________ 。
(2)元素E与元素H相比,金属性较强的是___________ (用元素符号表示),下列表述中能证明这一事实的是___________ (填字母序号)。
a.H的最高价氧化物对应的水化物的碱性比E的强
b.E的化合价比H的低
c.常温下E的单质与水反应的程度很剧烈,而H的单质在加热条件下才能与水反应
(3)画出硫的原子结构示意图:___________ ;画出氧离子的结构示意图:___________ 。
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 1 | A | |||||||
| 2 | B | C | D | |||||
| 3 | E | F | ||||||
| 4 | H |
(2)元素E与元素H相比,金属性较强的是
a.H的最高价氧化物对应的水化物的碱性比E的强
b.E的化合价比H的低
c.常温下E的单质与水反应的程度很剧烈,而H的单质在加热条件下才能与水反应
(3)画出硫的原子结构示意图:
您最近半年使用:0次
解题方法
2 . 如表是元素周期表的一部分,表中的每个编号代表一种短周期主族元素,请回答下列问题:
(1)表中金属性最强的是___________ (用元素符号表示),写出该元素的单质与水的反应离子方程式___________ 。
(2)表中⑤元素最高价氧化物对应水化物是___________ (填化学式),写出其电离方程式___________ 。
(3)元素③在元素周期表中的位置___________ 。
(4)元素①的单质在元素⑥的单质中燃烧产物的化学式___________ 。
(5)元素⑤和元素⑥可组成原子个数比为1:1的化合物的化学式为___________ 。
| 族 周期 | ⅠA | 0 | ||||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |||
| 2 | ② | ③ | ④ | |||||||
| 3 | ⑤ | ⑥ |
(2)表中⑤元素最高价氧化物对应水化物是
(3)元素③在元素周期表中的位置
(4)元素①的单质在元素⑥的单质中燃烧产物的化学式
(5)元素⑤和元素⑥可组成原子个数比为1:1的化合物的化学式为
您最近半年使用:0次
2024·广东·一模
解题方法
3 . 2024年是元素周期表诞生的第155周年。已知短周期主族元素X、Y、Z、M、N,其原子序数与其对应的0.1mol/L最高价氧化物的水化物溶液,在常温下的pH关系如图所示。下列说法中正确的是

| A.X和Y元素均在p区 | B.元素的电负性:Z>M>N |
| C.M的含氧酸根离子的中心原子为sp2杂化 | D.XN3和ZN3的空间构型均为三角锥形 |
您最近半年使用:0次
4 . 四种短周期主族元素W、X、Y、Z的原子序数依次增大。W与Y同族,且Y的原子序数是W的2倍;X的原子核外电子层数是其最外层电子数的3倍。回答下列问题:
(1)W在周期表中的位置为___________ 。
(2)W、X、Y的简单离子半径由大到小的顺序为___________ (用离子符号表示)。
(3)W、X形成的两种化合物的化学式为___________ 。
(4)元素Y、Z中非金属性较强的是___________ (用元素符号表示),下列说法能说明这一事实的是___________ (填字母)。
a.常温时两种元素的单质状态不同
b.气态氢化物的稳定性:Z>Y
c.氧化物对应水化物的酸性:Z>Y
d.简单离子的还原性:Y>Z
(1)W在周期表中的位置为
(2)W、X、Y的简单离子半径由大到小的顺序为
(3)W、X形成的两种化合物的化学式为
(4)元素Y、Z中非金属性较强的是
a.常温时两种元素的单质状态不同
b.气态氢化物的稳定性:Z>Y
c.氧化物对应水化物的酸性:Z>Y
d.简单离子的还原性:Y>Z
您最近半年使用:0次
名校
解题方法
5 . X、Y、Z、W均为短周期元素,它们在周期表中相对位置如图所示。若Y原子的最外层电子数是内层电子数的3倍,下列说法错误的是
| X | Y | |
| Z | W |
| A.四种元素的单质中,Z的单质熔点、沸点最高 |
B. 和 和 均具有漂白性,漂白原理不同 均具有漂白性,漂白原理不同 |
C.氧化物对应水化物的酸性: |
| D.X、Z的简单氢化物均能与各自某种氧化物对应的水化物发生反应 |
您最近半年使用:0次
2024-03-01更新
|
171次组卷
|
2卷引用:山东省威海市2023-2024学年高一上学期期末考试化学试题
名校
解题方法
6 . 短周期主族元素W、X、Y、Z的原子序数依次增大,X的原子半径是所有短周期主族元素中最大的,W的核外电子数与X、Z的最外层电子数之和相等,Y的原子序数是Z的最外层电子数的2倍,由W、X、Y三种元素形成的化合物M的结构如图所示。下列叙述正确的是
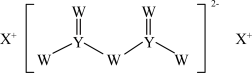

A.元素非金属性强弱的顺序为 |
B.离子半径关系 |
| C.W的简单氢化物稳定性比Y的简单氢化物稳定性低 |
| D.化合物M中W不都满足8电子稳定结构 |
您最近半年使用:0次
2024-02-27更新
|
272次组卷
|
3卷引用:山东省济宁市育才中学2023-2024学年高一下学期开学化学试题
解题方法
7 . W、X、Y、Z均为短周期元素,W的最外层电子数与核外电子总数之比为7∶17;X与W同主族;Y的原子序数是W和X的原子序数之和的一半;含Z元素的物质焰色试验为黄色。下列判断正确的是
| A.金属性:Y>Z | B.氢化物的沸点:X>W |
| C.离子的还原性:X>W | D.离子半径:Z>Y>X |
您最近半年使用:0次
2024-02-26更新
|
81次组卷
|
2卷引用:山东省德州市万隆中英文高级中学2023-2024学年高一下学期3月月考化学试题
名校
8 . 甲~辛等主族元素在周期表中的相对位置如下表。甲与戊的原子序数相差3,己是地壳中元素含量第二多的元素,丙与庚属同周期元素。下列判断正确的是
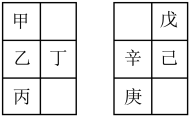
A.乙为K元素,庚元素为 元素 元素 |
| B.丙的焰色试验为黄色 |
| C.丙与庚的原子核外电子数相差12 |
| D.丁的最高价氧化物对应的水化物能与碱发生反应 |
您最近半年使用:0次
2024-02-26更新
|
53次组卷
|
2卷引用:山东省德州市万隆中英文高级中学2023-2024学年高一下学期3月月考化学试题
9 . 某同学根据元素的原子结构特点,将前18号元素排列成如图所示的蜗牛形状,图中每个点代表一种元素。下列说法中正确的是
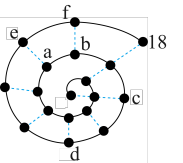

| A.a和e元素均属于第ⅣA |
B.原子核对最外层电子的吸引力: |
C.非金属性: |
D.原子半径: |
您最近半年使用:0次
解题方法
10 . 元素周期表已成为化学家的得力工具,为研究物质结构、发现新元素、合成新物质、寻找新材料提供了许多有价值的指导。下列说法正确的是
| A.在过渡元素中可以找到优良的半导体材料 |
| B.在元素周期表中随着原子序数的递增,原子最外层电子数总是从1到8重复出现 |
C.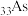 与 与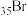 位于同一周期,则推测酸性: 位于同一周期,则推测酸性: 。 。 |
| D.根据元素周期表推测,单质铍能与冷水剧烈反应 |
您最近半年使用:0次



