1 . Se元素是人体必需的微量元素之一。下列说法正确的是
A. 不可以被氧化 不可以被氧化 | B. 的分子构型为V型 的分子构型为V型 |
C. 不能和碱溶液反应 不能和碱溶液反应 | D. 的热稳定性强于 的热稳定性强于 |
您最近半年使用:0次
名校
2 . 下表为截取的元素周期表前4周期的一部分,且X、Y、Z、R和W均为主族元素。下列说法不正确的是
| X | ||
| Y | Z | R |
| W |
| A.五种元素原子最外层电子数一定都大于2 |
| B.Y与W原子序数一定相差18 |
| C.R的最高价氧化物的水化物一定是强酸 |
| D.简单气态氢化物沸点:X可能高于Z |
您最近半年使用:0次
3 . 元素周期表是学习化学的重要工具,它隐含着许多信息和规律。下表列出了七种元素在元素周期表中的位置,回答下列问题:
(1)表中C在周期表的位置是___________ 。
(2)元素E与元素H相比,金属性较强的是___________ (用元素符号表示),下列表述中能证明这一事实的是___________ (填字母序号)。
a.H的最高价氧化物对应的水化物的碱性比E的强
b.E的化合价比H的低
c.常温下E的单质与水反应的程度很剧烈,而H的单质在加热条件下才能与水反应
(3)画出硫的原子结构示意图:___________ ;画出氧离子的结构示意图:___________ 。
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 1 | A | |||||||
| 2 | B | C | D | |||||
| 3 | E | F | ||||||
| 4 | H |
(2)元素E与元素H相比,金属性较强的是
a.H的最高价氧化物对应的水化物的碱性比E的强
b.E的化合价比H的低
c.常温下E的单质与水反应的程度很剧烈,而H的单质在加热条件下才能与水反应
(3)画出硫的原子结构示意图:
您最近半年使用:0次
解题方法
4 . 如表是元素周期表的一部分,表中的每个编号代表一种短周期主族元素,请回答下列问题:
(1)表中金属性最强的是___________ (用元素符号表示),写出该元素的单质与水的反应离子方程式___________ 。
(2)表中⑤元素最高价氧化物对应水化物是___________ (填化学式),写出其电离方程式___________ 。
(3)元素③在元素周期表中的位置___________ 。
(4)元素①的单质在元素⑥的单质中燃烧产物的化学式___________ 。
(5)元素⑤和元素⑥可组成原子个数比为1:1的化合物的化学式为___________ 。
| 族 周期 | ⅠA | 0 | ||||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |||
| 2 | ② | ③ | ④ | |||||||
| 3 | ⑤ | ⑥ |
(2)表中⑤元素最高价氧化物对应水化物是
(3)元素③在元素周期表中的位置
(4)元素①的单质在元素⑥的单质中燃烧产物的化学式
(5)元素⑤和元素⑥可组成原子个数比为1:1的化合物的化学式为
您最近半年使用:0次
名校
5 . 八角形元素周期表的每个顶角对应一种元素,下列说法正确的是
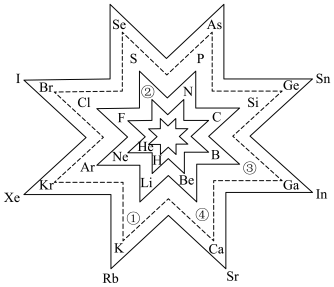
| A.虚线八角形顶角排列了第四周期所有元素 |
| B.等物质的量的①和③的单质混合能完全溶于足量水 |
| C.元素②的最高正化合价=主族序数 |
| D.金属性强弱:④>Sr |
您最近半年使用:0次
6 . 已知  是原子序数依次递增的短周期元素,已知 A和
是原子序数依次递增的短周期元素,已知 A和 和
和  为同一主族元素,A与
为同一主族元素,A与  与
与  形成共价化合物,B原子的最外层电子数比次外层多3,
形成共价化合物,B原子的最外层电子数比次外层多3, 元素的最高正化合价与最低负化合价的代数和为6,
元素的最高正化合价与最低负化合价的代数和为6, 是同周期中离子半径最小的元素,
是同周期中离子半径最小的元素, 形成的化合物是造成酸雨的主要原因。请回答下列问题:
形成的化合物是造成酸雨的主要原因。请回答下列问题:
(1)七种元素中,非金属性最强的元素在周期表中的位置是_____________ ,画出其原子结构示意图:_________________ .
(2)元素 的简单离子的半径由小到大的顺序为
的简单离子的半径由小到大的顺序为_____________________________ 。
(3)元素B的最低价氢化物的电子式为_____________________ 。
(4)由 所形成的常见离子化合物是
所形成的常见离子化合物是_____________ (写化学式),其所含化学键类型为_____________ 。
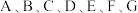 是原子序数依次递增的短周期元素,已知 A和
是原子序数依次递增的短周期元素,已知 A和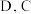 和
和  为同一主族元素,A与
为同一主族元素,A与 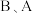 与
与  形成共价化合物,B原子的最外层电子数比次外层多3,
形成共价化合物,B原子的最外层电子数比次外层多3, 元素的最高正化合价与最低负化合价的代数和为6,
元素的最高正化合价与最低负化合价的代数和为6, 是同周期中离子半径最小的元素,
是同周期中离子半径最小的元素, 形成的化合物是造成酸雨的主要原因。请回答下列问题:
形成的化合物是造成酸雨的主要原因。请回答下列问题:(1)七种元素中,非金属性最强的元素在周期表中的位置是
(2)元素
 的简单离子的半径由小到大的顺序为
的简单离子的半径由小到大的顺序为(3)元素B的最低价氢化物的电子式为
(4)由
 所形成的常见离子化合物是
所形成的常见离子化合物是
您最近半年使用:0次
解题方法
7 . 如图是部分短周期主族元素化合价与原子序数的关系图,下列说法错误的是


A.气态氢化物的稳定性: |
B.由  五种元素形成的简单离子中半径最小的是 五种元素形成的简单离子中半径最小的是  |
C. 和 和  的最高价氧化物对应的水化物能发生反应 的最高价氧化物对应的水化物能发生反应 |
D. 的一种氧化物可做供氧剂 的一种氧化物可做供氧剂 |
您最近半年使用:0次
解题方法
8 . 2022年诺贝尔化学奖颁给了在“点击化学”领域做出贡献的科学家。我国科研人员发现了一种安全、高效的点击化学试剂  。下列关于元素
。下列关于元素 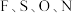 的说法正确的是
的说法正确的是
 。下列关于元素
。下列关于元素 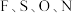 的说法正确的是
的说法正确的是A.简单气态氢化物中最稳定的是  | B.元素非金属性最强的是  |
C. 原子半径比 原子半径比  原子半径大 原子半径大 | D. 元素在周期表中的位置是第2周期 元素在周期表中的位置是第2周期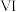 族 族 |
您最近半年使用:0次
9 . A、B、W、D、E为短周期元素,且原子序数依次增大,质子数之和为39,A形成的单质为密度最小的气体,B、W同周期,A、D同主族,A与W能形成两种液态化合物A2W和A2W2,E元素的周期序数与主族序数相等。回答下列问题:
(1)E元素在周期表中的位置为_______ 。
(2)D的一种氧化物可与B的最高价氧化物反应生成W的单质,试写出反应的化学方程式:_______ 。
(3)D形成的单质在一定条件下能与A形成的单质化合生成一种化合物DA,DA能与水反应放出氢气,写出该反应的化学方程式:_______ 。
(4)若要比较D和E的失电子能力强弱,下列实验方法可行的是_______ (填字母)。
a.将D形成的单质置于E的盐溶液中,若D形成的单质不能置换出E形成的单质,说明D的失电子能力比E的弱
b.在常温下,将少量D、E形成的单质分别投入到水中,若D形成的单质和水反应而E形成的单质不和水反应,说明D的失电子能力比E的强
c.比较相同条件下D和E的最高价氧化物对应的水化物的溶解性,若前者比后者的溶解度大,说明D的失电子能力比E的强
(1)E元素在周期表中的位置为
(2)D的一种氧化物可与B的最高价氧化物反应生成W的单质,试写出反应的化学方程式:
(3)D形成的单质在一定条件下能与A形成的单质化合生成一种化合物DA,DA能与水反应放出氢气,写出该反应的化学方程式:
(4)若要比较D和E的失电子能力强弱,下列实验方法可行的是
a.将D形成的单质置于E的盐溶液中,若D形成的单质不能置换出E形成的单质,说明D的失电子能力比E的弱
b.在常温下,将少量D、E形成的单质分别投入到水中,若D形成的单质和水反应而E形成的单质不和水反应,说明D的失电子能力比E的强
c.比较相同条件下D和E的最高价氧化物对应的水化物的溶解性,若前者比后者的溶解度大,说明D的失电子能力比E的强
您最近半年使用:0次
10 . 几种主族元素在周期表中的位置如下:

根据上表回答下列问题:
(1)⑥元素的氢化物是_______ (填化学式)。
(2)①③⑦三种元素原子半径由大到小的顺序是_______ (填元素符号)。
(3)表中某元素原子的核外电子层数是最外层电子数的3倍,该元素在周期表中的位置是_______ 。
(4)①②③三种元素最高价氧化物对应水化物的碱性最强的是_______ (填化学式),①与水反应的化学方程式为_______ 。
(5)⑦的非金属性强于⑧,从原子结构的角度解释其原因:_______ 。下列表述中能证明这一事实的是_______ (填字母)。
a.⑦的氢化物比⑧的氢化物稳定
b.⑦的最高价氧化物对应水化物的酸性强于⑧的最高价氧化物对应水化物的酸性
c.⑦能将⑧从其钠盐溶液中置换出来

根据上表回答下列问题:
(1)⑥元素的氢化物是
(2)①③⑦三种元素原子半径由大到小的顺序是
(3)表中某元素原子的核外电子层数是最外层电子数的3倍,该元素在周期表中的位置是
(4)①②③三种元素最高价氧化物对应水化物的碱性最强的是
(5)⑦的非金属性强于⑧,从原子结构的角度解释其原因:
a.⑦的氢化物比⑧的氢化物稳定
b.⑦的最高价氧化物对应水化物的酸性强于⑧的最高价氧化物对应水化物的酸性
c.⑦能将⑧从其钠盐溶液中置换出来
您最近半年使用:0次



