名校
1 . 元素周期表与元素周期律在化学学习研究中有很重要的作用。下表是元素周期表的一部分,请用对应的化学用语作答
(1)上述除①②外的元素中,离子半径最小的是______ (填离子符号),简单气态氢化物还原性最强的是______ (填化学式),最高价氧化物水化物酸性最强的是______ (填化学式)。
(2)某元素最高价氧化物水化物与其简单气态氢化物化合成盐,该盐的化学式为______ ,②④元素形成的三原子化合物的电子式为______ ,①③元素形成的简单气态氢化物分子的空间构型为______ 。
(3)A、B、C、D分别是上述元素形成的不同微粒,存在以下转化关系

若A、B、C、D均为10电子微粒,则A和B反应生成C和D的离子方程式为______ 。
②若A、C为18电子微粒,B、D为10电子微粒,则A和B反应生成C和D的离子方程式为______ 。
(4)元素⑥的最高价氧化物对应的水化物与元素⑦的最高价氧化物之间反应的离子方程式为______ 。
(5)下列事实不能说明元素⑩的非金属性比元素⑨强的是______(填字母)。
主族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA |
1 | ① | ||||||
2 | ② | ③ | ④ | ⑤ | |||
3 | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
(1)上述除①②外的元素中,离子半径最小的是
(2)某元素最高价氧化物水化物与其简单气态氢化物化合成盐,该盐的化学式为
(3)A、B、C、D分别是上述元素形成的不同微粒,存在以下转化关系

若A、B、C、D均为10电子微粒,则A和B反应生成C和D的离子方程式为
②若A、C为18电子微粒,B、D为10电子微粒,则A和B反应生成C和D的离子方程式为
(4)元素⑥的最高价氧化物对应的水化物与元素⑦的最高价氧化物之间反应的离子方程式为
(5)下列事实不能说明元素⑩的非金属性比元素⑨强的是______(填字母)。
| A.⑩的单质与⑨的简单氢化物溶液反应,溶液变浑浊 |
| B.⑩的单质可以将铁氧化为正三价,而的单质将铁氧化为正二价 |
| C.⑩的氢化物为强酸,而⑨的氢化物为弱酸 |
| D.⑩和⑨两元素的简单氢化物受热分解,前者的分解温度高 |
您最近半年使用:0次
2024-04-08更新
|
97次组卷
|
2卷引用:山东省济南市山东省实验中学2023-2024学年高一下学期3月月考化学试题
名校
2 . 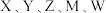 为五种短周期元素,
为五种短周期元素, 是原子序数依次递增的同周期元素,且最外层电子数之和为15;
是原子序数依次递增的同周期元素,且最外层电子数之和为15; 与
与 可形成XZ2分子;
可形成XZ2分子; 与
与 形成的气态化合物在标准状态下的密度为
形成的气态化合物在标准状态下的密度为 的质子数是
的质子数是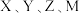 四种元素质子数之和的
四种元素质子数之和的 。下列说法正确的是
。下列说法正确的是
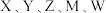 为五种短周期元素,
为五种短周期元素, 是原子序数依次递增的同周期元素,且最外层电子数之和为15;
是原子序数依次递增的同周期元素,且最外层电子数之和为15; 与
与 可形成XZ2分子;
可形成XZ2分子; 与
与 形成的气态化合物在标准状态下的密度为
形成的气态化合物在标准状态下的密度为 的质子数是
的质子数是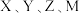 四种元素质子数之和的
四种元素质子数之和的 。下列说法正确的是
。下列说法正确的是A.离子半径: |
B.简单气态氢化物的稳定性: |
C.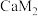 和 和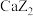 两种化合物中,阳离子与阴离子个数比均为 两种化合物中,阳离子与阴离子个数比均为 |
D.由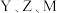 三种元素所组成的化合物的水溶液均显酸性 三种元素所组成的化合物的水溶液均显酸性 |
您最近半年使用:0次
2024-04-08更新
|
61次组卷
|
2卷引用:山东省济南市山东省实验中学2023-2024学年高一下学期3月月考化学试题
名校
解题方法
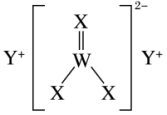
3 . 已知 均为短周期主族元素,在周期表中的相对位置如图所示,下列说法正确的是
均为短周期主族元素,在周期表中的相对位置如图所示,下列说法正确的是
 均为短周期主族元素,在周期表中的相对位置如图所示,下列说法正确的是
均为短周期主族元素,在周期表中的相对位置如图所示,下列说法正确的是X | Y |
Z | W |
A.若 为强酸, 为强酸, 的最高正价为 的最高正价为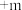 ,则 ,则 的最高正价也为 的最高正价也为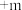 |
B.若四种元素均为金属元素,则 的最高价氧化物对应的水化物一定为强碱 的最高价氧化物对应的水化物一定为强碱 |
C.若四种元素均为非金属元素,则 的最高价氧化物对应的水化物一定为强酸 的最高价氧化物对应的水化物一定为强酸 |
D.若四种元素中只有一种为金属元素,则 与 与 二者的最高价氧化物对应的水化物能反应 二者的最高价氧化物对应的水化物能反应 |
您最近半年使用:0次
2024-04-08更新
|
50次组卷
|
2卷引用:山东省济南市山东省实验中学2023-2024学年高一下学期3月月考化学试题
名校
解题方法
4 . 为纪念元素周期表诞生150周年,IUPAC等向世界介绍118位优秀青年化学家,并形成一张“青年化学家元素周期表”。中国学者雷晓光、姜雪峰、刘庄分别成为“N、S、Hg”元素的代言人。回答下列问题:
(1)汞的原子结构示意图 ,写出汞在周期表中的位置
,写出汞在周期表中的位置___________ 。
(2)下列有关性质的比较能用元素周期律解释的是___________。
(3)硒(Se)与硫位于同一主族,均是生命必需元素。下列推断错误的是___________ 。
A.硒元素的最低负化合价为-2价
B.二氧化硒(SeO2)具有还原性
C.硒的氧化物对应的水化物属于强酸
(4)某种化合物是工业洗涤剂的中间体,其结构如图所示。其中X、Y、Z、Q、W为原子序数依次增大的五种短周期元素,Q最外层电子数与Y核外电子总数相同,X的原子半径是元素周期表中最小的。回答下列问题:
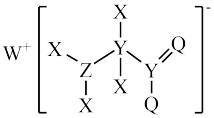
①Z单质的结构式为___________ 。
②Y、Z、Q三种元素所形成的简单气态氢化物中,稳定性最强的是___________ (填化学式);X、Y、Z、Q四种元素组成的化合物中,既含离子键又含共价键的是___________ (填化学式,一种即可)。
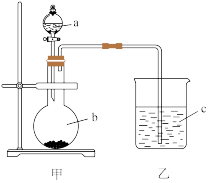
③利用如图装置可比较Y、Z两元素原子的得电子能力,b中发生反应的化学方程式为___________ 。
(1)汞的原子结构示意图
 ,写出汞在周期表中的位置
,写出汞在周期表中的位置(2)下列有关性质的比较能用元素周期律解释的是___________。
| A.酸性:HCl>H2SO3 | B.非金属性:O>S |
| C.碱性:NaOH>Mg(OH)2 | D.热稳定性:Na2CO3>NaHCO3 |
A.硒元素的最低负化合价为-2价
B.二氧化硒(SeO2)具有还原性
C.硒的氧化物对应的水化物属于强酸
(4)某种化合物是工业洗涤剂的中间体,其结构如图所示。其中X、Y、Z、Q、W为原子序数依次增大的五种短周期元素,Q最外层电子数与Y核外电子总数相同,X的原子半径是元素周期表中最小的。回答下列问题:

①Z单质的结构式为
②Y、Z、Q三种元素所形成的简单气态氢化物中,稳定性最强的是
③利用如图装置可比较Y、Z两元素原子的得电子能力,b中发生反应的化学方程式为

您最近半年使用:0次
名校
5 . 2023年4月15日,我国神舟十五号航天员顺利完成第四次出舱任务,安全返回天问实验舱。载人飞船的材料中含有的主族元素W、X、Y、Z,分布在三个短周期中,其原子序数依次增大,X、Z同主族,X的最外层电子数是W和Y的最外层电子数之和,其中只有Y的单质为金属,能与NaOH溶液反应。下列叙述正确的是
| A.原子半径:Y>Z>X>W |
| B.Z的氧化物为酸性氧化物,能与水反应生成对应的酸 |
| C.X与W形成的最简单化合物的热稳定性比Z与W形成的最简单化合物的热稳定性差 |
| D.Z单质可广泛应用于制造光电池、芯片等 |
您最近半年使用:0次
2023-08-10更新
|
278次组卷
|
2卷引用:山东省济南市2022-2023学年高一下学期期中考试化学试题
名校
6 . X、Y、Z、W、R、Q为原子序数依次增大的六种短周期主族元素。X是原子半径最小的元素;Y原子最外层电子数是核外电子层数的3倍;Z是短周期中金属性最强的元素;W是地壳中含量最多的金属元素;R的最高正价与最低负价代数和为4,请回答下列问题:
(1)W在周期表中的位置是_______ 。
(2)ZYX的电子式为_______ , 中含有的化学键类型为
中含有的化学键类型为_______ 。
(3)Y、Z、W三种元素对应的简单离子半径由大到小的顺序是_______ (用元素的离子符号表示)。
(4)下列说法能证明非金属性Q强于R的是_______ (填字母)。
a.简单阴离子的还原性:
b.简单氢化物热稳定性:
c.氧化物对应的水化物的酸性:
(5)W的最高价氧化物对应水化物与Z的最高价氧化物对应水化物反应的离子方程式是_______ 。
(6)X和Y组成的化合物中,既含有极性共价键又含有非极性共价键的是_______ (填化学式),此化合物可将碱性工业废水中的CN-氧化,生成碳酸盐和氨气,相应的离子方程式为_______ 。
(1)W在周期表中的位置是
(2)ZYX的电子式为
 中含有的化学键类型为
中含有的化学键类型为(3)Y、Z、W三种元素对应的简单离子半径由大到小的顺序是
(4)下列说法能证明非金属性Q强于R的是
a.简单阴离子的还原性:

b.简单氢化物热稳定性:

c.氧化物对应的水化物的酸性:

(5)W的最高价氧化物对应水化物与Z的最高价氧化物对应水化物反应的离子方程式是
(6)X和Y组成的化合物中,既含有极性共价键又含有非极性共价键的是
您最近半年使用:0次
名校
解题方法
7 . 应用元素周期律的有关知识,可以预测我们不熟悉的一些元素的单质及其化合物的性质。下列预测中正确的是
①第2周期非金属元素的气态氢化物溶于水后,水溶液均为酸性
②碳酸锶(SrCO3)是难溶于水的白色固体,受热能发生分解反应
③Tl(铊)与盐酸和NaOH溶液作用均能产生氢气
④铍 的氧化物的水化物可能具有两性
的氧化物的水化物可能具有两性
⑤非金属性F>Cl,故将F2通入NaCl溶液中,发生反应为F2+2Cl−=Cl2+2F−
①第2周期非金属元素的气态氢化物溶于水后,水溶液均为酸性
②碳酸锶(SrCO3)是难溶于水的白色固体,受热能发生分解反应
③Tl(铊)与盐酸和NaOH溶液作用均能产生氢气
④铍
 的氧化物的水化物可能具有两性
的氧化物的水化物可能具有两性⑤非金属性F>Cl,故将F2通入NaCl溶液中,发生反应为F2+2Cl−=Cl2+2F−
| A.②④ | B.①②③④ | C.①③⑤ | D.②④⑤ |
您最近半年使用:0次
名校
解题方法
8 . (I)俄美科学家联合小组宣布合成出114号元素(Fl)的一种同位素,该原子的质量数是289,试回答下列问题:
(1)该元素在周期表中的位置为:_______ ,属于_______ 元素(填“金属”或“非金属”)。
(II)下表为元素周期表的部分,列出了10种元素在元素周期表中的位置,试回答下列问题:
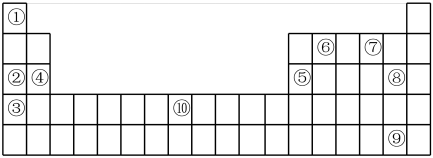
(2)②③④三种元素最高价氧化物的水化物碱性由强到弱的顺序是_______ (填化学式)。
(3)元素⑦的简单氢化物与③的单质反应的离子方程式为_______ ;
(4)元素②和⑤的最高价氧化物的水化物反应的离子方程式为_______ ;
(5)元素⑩的名称为_______ ,其单质与⑧的单质反应的化学方程式为_______ ;
(6)部分短周期元素的原子半径及主要化合价如下表,判断以下叙述不正确的是_______
A.L2+、R2-的核外电子数相等
B.单质与稀盐酸反应的速率L<Q
C.M与T形成的化合物具有两性
D.简单氢化物的沸点为HnT>HnR
E.T与R可形成的化合物TR2、TR3
F.Q与M的单质均能与盐酸、NaOH溶液反应放出氢气
(1)该元素在周期表中的位置为:
(II)下表为元素周期表的部分,列出了10种元素在元素周期表中的位置,试回答下列问题:

(2)②③④三种元素最高价氧化物的水化物碱性由强到弱的顺序是
(3)元素⑦的简单氢化物与③的单质反应的离子方程式为
(4)元素②和⑤的最高价氧化物的水化物反应的离子方程式为
(5)元素⑩的名称为
(6)部分短周期元素的原子半径及主要化合价如下表,判断以下叙述不正确的是
| 元素代号 | L | M | Q | R | T |
| 原子半径/nm | 0.160 | 0.143 | 0.112 | 0.104 | 0.066 |
| 主要化合价 | +2 | +3 | +2 | +6、-2 | -2 |
B.单质与稀盐酸反应的速率L<Q
C.M与T形成的化合物具有两性
D.简单氢化物的沸点为HnT>HnR
E.T与R可形成的化合物TR2、TR3
F.Q与M的单质均能与盐酸、NaOH溶液反应放出氢气
您最近半年使用:0次
名校
解题方法
9 . 几种短周期元素的原子半径及主要化合价如下表所示,下列叙述正确的是
| 元素代号 | X | Y | Z | W |
| 原子半径/pm | 160 | 143 | 70 | 66 |
| 主要化合价 | +2 | +3 | +5、+3、-3 | -2 |
| 元素化合物的性质 | 形成常见的两性氧化物 | Z2是常见保护气 | W3可用于杀菌消毒 |
| A.W的简单氢化物比Z的简单氢化物稳定 |
| B.X、Y元素的金属性X<Y |
| C.Y的最高价氧化物对应的水化物能溶于稀氨水 |
| D.一定条件下,Z单质与W的常见单质直接生成ZW2 |
您最近半年使用:0次
22-23高三上·河北邢台·期末
名校
10 . 短周期主族元素W、X、Y、Z的原子序数依次增大,W的最高正价与最低负价绝对值之差为0,W、X、Y形成的化合物甲的结构如图所示,Z原子M层上有2个未成对电子且此能级无空轨道。下列说法正确的是

| A.电负性大小:X>W>Z |
| B.简单氢化物的沸点:X>Z |
| C.X、Y形成的化合物只含离子键 |
| D.W和Z最高价氧化物中心原子的杂化方式相同 |
您最近半年使用:0次



