名校
1 . 科学家在嫦娥五号取回的月壤中发现了水及大量玻璃性质的物质,经分析,月壤中含有原子序数依次增大的短周期主族元素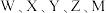 ,其中
,其中 分别位于不同周期,
分别位于不同周期,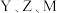 为同周期相邻的元素且最外层电子数之和为9,X最外层电子数是
为同周期相邻的元素且最外层电子数之和为9,X最外层电子数是 最外层电子数的2倍。下列说法正确的是
最外层电子数的2倍。下列说法正确的是
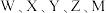 ,其中
,其中 分别位于不同周期,
分别位于不同周期,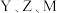 为同周期相邻的元素且最外层电子数之和为9,X最外层电子数是
为同周期相邻的元素且最外层电子数之和为9,X最外层电子数是 最外层电子数的2倍。下列说法正确的是
最外层电子数的2倍。下列说法正确的是A. 元素形成的化合物中的化学键为离子键 元素形成的化合物中的化学键为离子键 |
B. 的简单离子半径: 的简单离子半径: |
C.非金属性: |
D. 与 与 只能形成一种化合物 只能形成一种化合物 |
您最近半年使用:0次
名校
解题方法
2 . 国家卫生健康委员会发布公告称,富硒酵母、二氧化硅、硫黄等6种食品添加剂新品种安全性已通过审查,这些食品添加剂包括食品营养强化剂、风味改良剂、结构改善剂、防腐剂,用于食品生产中,丰富舌尖上的营养和美味。氧、硫、硒为同一主族元素,请回答下列问题:
(1)硒(Se)是一种生命元素,有抗癌、抗衰老等重要功能。富硒酵母是一种新型添加剂,其中硒元素在周期表中的位置为______ 。工业上用浓H2SO4焙烧CuSe的方法提取硒(其中Cu转化为CuSO4),且有SO2、H2O和SeO2(固体)生成,写出发生反应的化学方程式:_____ 。理论上该反应每转移1mol电子,得到的SeO2的质量为_____ 。
(2)下列说法正确的是______。
(3)短周期元素d、e、f、g、h、x都可能存在于某些食品添加剂中,其最高正化合价或最低负化合价与原子序数的关系如图所示:___________ 。
②d、e、f、g、h元素形成的简单离子中,半径最大的离子结构示意图为___________ 。
③x和d组成的化合物中,既含有极性共价键又含有非极性共价键,此化合物可将碱性工业废水中的 氧化,生成碳酸盐和氨气,相应的离子方程式为
氧化,生成碳酸盐和氨气,相应的离子方程式为___________ 。
④e和d组成的某化合物,可做呼吸面具的供氧剂,用电子式表示其形成过程___________ 。
(1)硒(Se)是一种生命元素,有抗癌、抗衰老等重要功能。富硒酵母是一种新型添加剂,其中硒元素在周期表中的位置为
(2)下列说法正确的是______。
A.热稳定性: | B.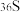 与 与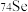 的中子数之和为60 的中子数之和为60 |
C.酸性: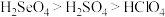 | D.还原性:Se2- < S2- |
(3)短周期元素d、e、f、g、h、x都可能存在于某些食品添加剂中,其最高正化合价或最低负化合价与原子序数的关系如图所示:
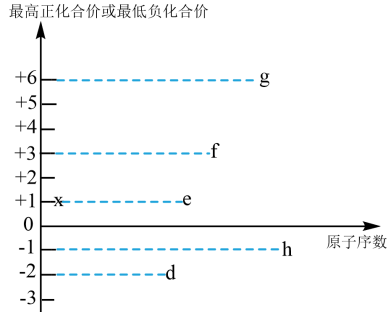
②d、e、f、g、h元素形成的简单离子中,半径最大的离子结构示意图为
③x和d组成的化合物中,既含有极性共价键又含有非极性共价键,此化合物可将碱性工业废水中的
 氧化,生成碳酸盐和氨气,相应的离子方程式为
氧化,生成碳酸盐和氨气,相应的离子方程式为④e和d组成的某化合物,可做呼吸面具的供氧剂,用电子式表示其形成过程
您最近半年使用:0次
2023-08-31更新
|
267次组卷
|
3卷引用:山东省东明县第一中学2022-2023学年高一下学期3月月考化学试题
名校
3 . 随原子序数递增,八种短周期元素(用字母x、y等表示)原子半径的相对大小、最高正价或最低负价的变化如图所示。回答下列问题:

(1)d在元素周期表中的位置位于_____ ;写出z、d、e的简单离子半径由大到小的顺序______ (用离子符号表示)。
(2)金属 单质及其化合物的性质与
单质及其化合物的性质与 单质及其化合物的性质相似,写出鉴别
单质及其化合物的性质相似,写出鉴别 和
和 反应的化学方程式
反应的化学方程式_________ 。
(3)写出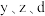 的最简单氢化物的稳定性由强到弱的顺序
的最简单氢化物的稳定性由强到弱的顺序_____ (用化学式表示)。
(4) 与g相比,非金属性较强的是
与g相比,非金属性较强的是___ (用元素符号表示);得出该结论所依据的实验事实是_______ (只答一条)。
(5)用电子式表示 的最高价氧化物的形成过程:
的最高价氧化物的形成过程:________ 。
(6) 的一种氢化物分子
的一种氢化物分子 中既含非极性键又含极性键,其结构式为
中既含非极性键又含极性键,其结构式为____ 。

(1)d在元素周期表中的位置位于
(2)金属
 单质及其化合物的性质与
单质及其化合物的性质与 单质及其化合物的性质相似,写出鉴别
单质及其化合物的性质相似,写出鉴别 和
和 反应的化学方程式
反应的化学方程式(3)写出
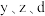 的最简单氢化物的稳定性由强到弱的顺序
的最简单氢化物的稳定性由强到弱的顺序(4)
 与g相比,非金属性较强的是
与g相比,非金属性较强的是(5)用电子式表示
 的最高价氧化物的形成过程:
的最高价氧化物的形成过程:(6)
 的一种氢化物分子
的一种氢化物分子 中既含非极性键又含极性键,其结构式为
中既含非极性键又含极性键,其结构式为
您最近半年使用:0次
名校
解题方法
4 . Q、X、Y、Z是原子序数逐渐增大的短周期主族元素,其最外层电子数之和为15。X、Y、Z为同周期相邻元素,且均不与Q同族。下列说法正确的是
| A.非金属性:Z>Q | B.单质的导电性:Y<Z |
| C.原子半径半径:X<Z | D.最高价氧化物水化物的碱性:X>Y |
您最近半年使用:0次
名校
5 . 一种麻醉剂的结构式如图所示。元素X的原子核只有1个质子,元素Y、Z、W的原子序数增大,且均位于X的下一周期,元素E的原子比元素W的原子多8个电子。下列说法错误的是

A.离子半径: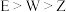 | B.非金属性: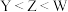 |
C.ZW2中, 的化合价为 的化合价为 价 价 | D.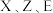 能形成具有漂白性的化合物 能形成具有漂白性的化合物 |
您最近半年使用:0次
2023-08-22更新
|
482次组卷
|
3卷引用: 山东省淄博实验中学2022-2023学年高一上学期期末考试化学试题
6 . 短周期主族元素W、X、Y、Z的原子序数依次增大,W与X的原子序数之和是Y的一半,Y、Z的基态原子中单电子数之比为2:1,甲、乙、丙分别为元素X、Y、Z的单质,m、n、p均是这些元素组成的常见二元气态物质,其中常温下,0.01mol·L-1p溶液的pH为2,他们之间的转化关系如图所示。下列说法错误的是


| A.第一电离能:X<Y |
| B.沸点:n>m |
| C.氧化性:丙>乙 |
| D.m、q的水溶液均显酸性 |
您最近半年使用:0次
名校
7 . 1869年俄国化学家门捷列夫制出第一张元素周期表,元素周期表体现了元素位置、结构和性质的关系。短周期元素A、B、C、D、E原子序数递增,由它们组成的新型化合物CA4B5D8·4A2D可用于电讯器材、高级玻璃的制造,其受热分解产物中有两种常见的10电子分子,二者反应生成一种弱碱,B、E同主族,E是同周期离子半径最小的。
(1)画出E的离子结构示意图______ ,在元素周期表中的位置为______ 。
(2)100—200℃时只生成一种气体,该气体电子式为______ 。
(3)试比较B、C、E元素所形成最高价氧化物对应水化物的酸性由强到弱的顺序为(写化学式)______ ,并从原子结构角度解释其原因__ 。
(4)请依据推断比较D、E两种元素离子半径的大小______ 。
(5)C的最高价氧化物对应的水化物与E的最高价氧化物对应的水化物反应的离子方程式为______ 。
(6)该化合物500℃热分解后生成的固体氧化物可与Mg单质发生置换反应,写出化学方程式______ 。
(1)画出E的离子结构示意图
(2)100—200℃时只生成一种气体,该气体电子式为
(3)试比较B、C、E元素所形成最高价氧化物对应水化物的酸性由强到弱的顺序为(写化学式)
(4)请依据推断比较D、E两种元素离子半径的大小
(5)C的最高价氧化物对应的水化物与E的最高价氧化物对应的水化物反应的离子方程式为
(6)该化合物500℃热分解后生成的固体氧化物可与Mg单质发生置换反应,写出化学方程式
您最近半年使用:0次
名校
8 . 元素周期表中E、G、L、M、P、Q、R为7种短周期元素,M是非金属性最强的元素,Q的单质广泛用作半导体材料,其余元素的信息如图所示。下列说法正确的有
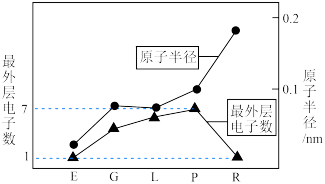
| A.G和Q所对应的气态氢化物的还原性,后者更强 |
| B.L和R形成的化合物为离子化合物,只含有离子键 |
| C.Q和P最高价氧化物对应水化物的酸性,后者更强 |
| D.非金属性:M>P,M的单质能将P单质从RP溶液中置换出来 |
您最近半年使用:0次
2023-08-14更新
|
248次组卷
|
4卷引用:山东省济南市历城第二中学等学校2022-2023学年高一下学期3月月考化学B卷试题
名校
解题方法
9 . 短周期元素X、Y、Z、W的原子序数依次增大,其中Y和W同主族,由X、Y、Z三种元素组成的四种二元微粒(分子或离子)A+、B-、C、D均具有10个电子,已知它们有如下转化关系:A++B- C+D↑,下列说法正确的是
C+D↑,下列说法正确的是
 C+D↑,下列说法正确的是
C+D↑,下列说法正确的是| A.X、Y、Z元素最高正化合价依次升高 |
| B.原子半径大小:W>Z>Y>X |
| C.只有原子核外最外层达到8电子结构才是稳定结构 |
| D.W、Y、Z所对应的三种气态氢化物的稳定性逐渐增强 |
您最近半年使用:0次
2023-08-14更新
|
242次组卷
|
3卷引用:山东省济南市历城第二中学等学校2022-2023学年高一下学期3月月考化学B卷试题
名校
解题方法
10 . 为纪念元素周期表诞生150周年,IUPAC等向世界介绍118位优秀青年化学家,并形成一张“青年化学家元素周期表”。中国学者雷晓光、姜雪峰、刘庄分别成为“N、S、Hg”元素的代言人。回答下列问题:
(1)汞的原子结构示意图 ,写出汞在周期表中的位置
,写出汞在周期表中的位置___________ 。
(2)下列有关性质的比较能用元素周期律解释的是___________。
(3)硒(Se)与硫位于同一主族,均是生命必需元素。下列推断错误的是___________ 。
A.硒元素的最低负化合价为-2价
B.二氧化硒(SeO2)具有还原性
C.硒的氧化物对应的水化物属于强酸
(4)某种化合物是工业洗涤剂的中间体,其结构如图所示。其中X、Y、Z、Q、W为原子序数依次增大的五种短周期元素,Q最外层电子数与Y核外电子总数相同,X的原子半径是元素周期表中最小的。回答下列问题:
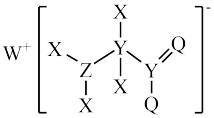
①Z单质的结构式为___________ 。
②Y、Z、Q三种元素所形成的简单气态氢化物中,稳定性最强的是___________ (填化学式);X、Y、Z、Q四种元素组成的化合物中,既含离子键又含共价键的是___________ (填化学式,一种即可)。
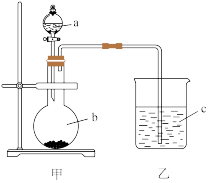
③利用如图装置可比较Y、Z两元素原子的得电子能力,b中发生反应的化学方程式为___________ 。
(1)汞的原子结构示意图
 ,写出汞在周期表中的位置
,写出汞在周期表中的位置(2)下列有关性质的比较能用元素周期律解释的是___________。
| A.酸性:HCl>H2SO3 | B.非金属性:O>S |
| C.碱性:NaOH>Mg(OH)2 | D.热稳定性:Na2CO3>NaHCO3 |
A.硒元素的最低负化合价为-2价
B.二氧化硒(SeO2)具有还原性
C.硒的氧化物对应的水化物属于强酸
(4)某种化合物是工业洗涤剂的中间体,其结构如图所示。其中X、Y、Z、Q、W为原子序数依次增大的五种短周期元素,Q最外层电子数与Y核外电子总数相同,X的原子半径是元素周期表中最小的。回答下列问题:

①Z单质的结构式为
②Y、Z、Q三种元素所形成的简单气态氢化物中,稳定性最强的是
③利用如图装置可比较Y、Z两元素原子的得电子能力,b中发生反应的化学方程式为

您最近半年使用:0次



