1 . 如图表示元素周期表中部分元素的某种性质(X值)随原子序数变化的关系示意图。___________ (填元素符号)。
(2)同主族内不同元素的X值变化的特点是___________ ;
(3)预测S元素与Se元素X值的大小关系为___________ ,X值最小的元素在元素周期表中的位置是___________ (放射性元素除外)。
(4)依据X值判断 是
是___________ (填共价化合物或离子化合物),如何通过实验来判断你的结论___________
(5)下列关于元素性质的说法正确的是___________ (填标号)。
a.X值可反映元素最高正化合价的变化规律
b.X值可反映元素在化合物中吸引电子的能力
c.X值的大小可用来判断元素金属性和非金属性的强弱

(2)同主族内不同元素的X值变化的特点是
(3)预测S元素与Se元素X值的大小关系为
(4)依据X值判断
 是
是(5)下列关于元素性质的说法正确的是
a.X值可反映元素最高正化合价的变化规律
b.X值可反映元素在化合物中吸引电子的能力
c.X值的大小可用来判断元素金属性和非金属性的强弱
您最近一年使用:0次
解题方法
2 . A、B、C、D、E、F、G、H是元素周期表前四周期常见元素,且原子序数依次增大,其相关信息如下表:
请用化学用语填空:
(1)C元素和F元素的电负性比较,较小的是___________ 。
(2)B元素与宇宙中含量最丰富的元素形成的含有18 的分子的电子式为
的分子的电子式为___________ 。
(3)实验室用一种黄色溶液检验 时产生蓝色沉淀,该反应的离子方程式为
时产生蓝色沉淀,该反应的离子方程式为___________ ;与E元素成对角线关系的某元素的最高价氧化物的水化物具有两性,写出该两性物质与D元素的最高价氧化物的水化物反应的化学方程式:___________ 。
(4)氮、磷、砷等元素的单质及其化合物在生产生活中应用广泛。回答下列问题:
①处于下列状态的磷原子或离子失去最外层一个电子所需能量最高的是___________ (填标号)。
a. b.
b.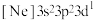 c.
c.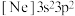 d.
d.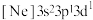
②M是氮杂氟硼二吡咯类物质,常用作光敏剂,其结构如图。 键,则该环N原子价层孤对电子填充在
键,则该环N原子价层孤对电子填充在___________ 轨道;M中存在的微粒间作用力有___________ (填标号)。
a.共价键 b.离子键 c.氢键 d.配位键
| 元素 | 相关信息 |
| A | 原子核外有6种不同运动状态的电子 |
| C | 基态原子中s电子总数与p电子总数相等 |
| D | 原子半径在同周期元素中最大 |
| E | 同周期元素原子的简单离子中半径最小 |
| F | 基态原子的最外层p轨道有两个电子的自旋方向与其他电子的自旋方向相反 |
| G | 基态原子核外有7个能级且能量最高的能级上有6个电子 |
| H | 是我国使用最早的合金中的最主要元素 |
(1)C元素和F元素的电负性比较,较小的是
(2)B元素与宇宙中含量最丰富的元素形成的含有18
 的分子的电子式为
的分子的电子式为(3)实验室用一种黄色溶液检验
 时产生蓝色沉淀,该反应的离子方程式为
时产生蓝色沉淀,该反应的离子方程式为(4)氮、磷、砷等元素的单质及其化合物在生产生活中应用广泛。回答下列问题:
①处于下列状态的磷原子或离子失去最外层一个电子所需能量最高的是
a.
 b.
b.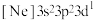 c.
c.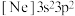 d.
d.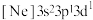
②M是氮杂氟硼二吡咯类物质,常用作光敏剂,其结构如图。

 键,则该环N原子价层孤对电子填充在
键,则该环N原子价层孤对电子填充在a.共价键 b.离子键 c.氢键 d.配位键
您最近一年使用:0次
3 . A、B都是短周期元素,原子半径B>A,它们可以形成化合物AB2,由此可得出的不正确判断是
| A.A、B不在同一周期 |
| B.A肯定是金属元素 |
| C.A、B可能都是非金属元素 |
| D.A可能在第2周期的ⅡA族或ⅣA族 |
您最近一年使用:0次
4 . 已知X、Y、Z、W均为短周期主族元素,在周期表中的相对位置如图所示,下列说法正确的是
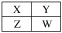
| A.若HmXOn为强酸,则X的氢化物溶于水一定显酸性(m、n均为正整数) |
| B.若四种元素均为金属元素,则Z的最高价氧化物对应的水化物一定为强碱 |
| C.若四种元素均为非金属元素,则W的最高价氧化物对应的水化物一定为强酸 |
| D.若四种元素中只有一种为金属元素,则Z与Y二者的最高价氧化物对应的水化物能反应 |
您最近一年使用:0次
5 . 短周期主族元素X、Y、Z、W的原子序数依次增大,Z可与X形成淡黄色化合物Z2X2,Y、W最外层电子数相同。下列说法正确的是
| A.得电子能力:W>X>Y |
| B.简单离子的还原性:Y>X>W |
| C.简单离子的半径:W>X>Y>Z |
| D.氢化物水溶液的酸性:Y>W |
您最近一年使用:0次
名校
6 . 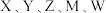 为五种短周期元素,
为五种短周期元素, 是原子序数依次递增的同周期元素,且最外层电子数之和为15;
是原子序数依次递增的同周期元素,且最外层电子数之和为15; 与
与 可形成XZ2分子;
可形成XZ2分子; 与
与 形成的气态化合物在标准状态下的密度为
形成的气态化合物在标准状态下的密度为 的质子数是
的质子数是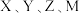 四种元素质子数之和的
四种元素质子数之和的 。下列说法不正确的是
。下列说法不正确的是
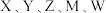 为五种短周期元素,
为五种短周期元素, 是原子序数依次递增的同周期元素,且最外层电子数之和为15;
是原子序数依次递增的同周期元素,且最外层电子数之和为15; 与
与 可形成XZ2分子;
可形成XZ2分子; 与
与 形成的气态化合物在标准状态下的密度为
形成的气态化合物在标准状态下的密度为 的质子数是
的质子数是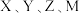 四种元素质子数之和的
四种元素质子数之和的 。下列说法不正确的是
。下列说法不正确的是A.离子半径: |
B.简单气态氢化物的稳定性: |
C.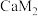 和 和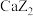 两种化合物中,阳离子与阴离子个数比均为 两种化合物中,阳离子与阴离子个数比均为 |
D.由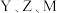 三种元素所组成的化合物的水溶液可能显酸性也可能显碱性 三种元素所组成的化合物的水溶液可能显酸性也可能显碱性 |
您最近一年使用:0次
7 . Se元素是人体必需的微量元素之一。下列说法正确的是
A. 不可以被氧化 不可以被氧化 | B. 的分子构型为V型 的分子构型为V型 |
C. 不能和碱溶液反应 不能和碱溶液反应 | D. 的热稳定性强于 的热稳定性强于 |
您最近一年使用:0次
名校
8 . 下表为截取的元素周期表前4周期的一部分,且X、Y、Z、R和W均为主族元素。下列说法不正确的是
| X | ||
| Y | Z | R |
| W |
| A.五种元素原子最外层电子数一定都大于2 |
| B.Y与W原子序数一定相差18 |
| C.R的最高价氧化物的水化物一定是强酸 |
| D.简单气态氢化物沸点:X可能高于Z |
您最近一年使用:0次
名校
9 . 八角形元素周期表的每个顶角对应一种元素,下列说法正确的是
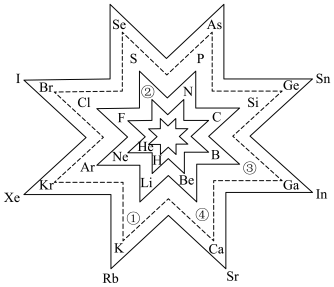
| A.虚线八角形顶角排列了第四周期所有元素 |
| B.等物质的量的①和③的单质混合能完全溶于足量水 |
| C.元素②的最高正化合价=主族序数 |
| D.金属性强弱:④>Sr |
您最近一年使用:0次
10 . 已知 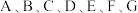 是原子序数依次递增的短周期元素,已知 A和
是原子序数依次递增的短周期元素,已知 A和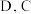 和
和  为同一主族元素,A与
为同一主族元素,A与 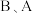 与
与  形成共价化合物,B原子的最外层电子数比次外层多3,
形成共价化合物,B原子的最外层电子数比次外层多3, 元素的最高正化合价与最低负化合价的代数和为6,
元素的最高正化合价与最低负化合价的代数和为6, 是同周期中离子半径最小的元素,
是同周期中离子半径最小的元素, 形成的化合物是造成酸雨的主要原因。请回答下列问题:
形成的化合物是造成酸雨的主要原因。请回答下列问题:
(1)七种元素中,非金属性最强的元素在周期表中的位置是_____________ ,画出其原子结构示意图:_________________ .
(2)元素 的简单离子的半径由小到大的顺序为
的简单离子的半径由小到大的顺序为_____________________________ 。
(3)元素B的最低价氢化物的电子式为_____________________ 。
(4)由 所形成的常见离子化合物是
所形成的常见离子化合物是_____________ (写化学式),其所含化学键类型为_____________ 。
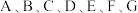 是原子序数依次递增的短周期元素,已知 A和
是原子序数依次递增的短周期元素,已知 A和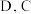 和
和  为同一主族元素,A与
为同一主族元素,A与 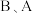 与
与  形成共价化合物,B原子的最外层电子数比次外层多3,
形成共价化合物,B原子的最外层电子数比次外层多3, 元素的最高正化合价与最低负化合价的代数和为6,
元素的最高正化合价与最低负化合价的代数和为6, 是同周期中离子半径最小的元素,
是同周期中离子半径最小的元素, 形成的化合物是造成酸雨的主要原因。请回答下列问题:
形成的化合物是造成酸雨的主要原因。请回答下列问题:(1)七种元素中,非金属性最强的元素在周期表中的位置是
(2)元素
 的简单离子的半径由小到大的顺序为
的简单离子的半径由小到大的顺序为(3)元素B的最低价氢化物的电子式为
(4)由
 所形成的常见离子化合物是
所形成的常见离子化合物是
您最近一年使用:0次



