解题方法
1 . 元素周期表与元素周期律在化学学习研究中有很重要的作用。如表所示是五种元素的相关信息,W、X都位于第三周期。
(1)W在元素周期表中的位置是____ 。
(2)Y的气态氢化物的空间结构是____ ,W、Z、X的简单离子半径由大到小的顺序为____ 。
(3)X单质、W单质均能与水反应,写出实验室制备W单质的离子方程式为____ ,X单质与乙醇反应的化学方程式是____ 。
(4)金属性Z>X,用原子结构解释原因:____ ,失电子能力Z>X,金属性Z>X。
(5)化合物M是由Q和Y两种元素组成的,其相对分子质量为72,写出其含有支链的同分异构体的结构简式____ 。
| 元素 | 信息 |
| Q | 在元素周期表中,原子半径最小 |
| W | 最高化合价为+7 |
| X | 最高价氧化物对应的水化物在第三周期中碱性最强 |
| Y | 原子的最外层电子数为次外层电子数的2倍 |
| Z | 阳离子结构示意图为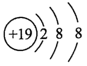 |
(2)Y的气态氢化物的空间结构是
(3)X单质、W单质均能与水反应,写出实验室制备W单质的离子方程式为
(4)金属性Z>X,用原子结构解释原因:
(5)化合物M是由Q和Y两种元素组成的,其相对分子质量为72,写出其含有支链的同分异构体的结构简式
您最近一年使用:0次
名校
2 . 现有短周期主族元素X、Y、Z、R、W、T,R原子最外层电子数是电子层数的2倍,Z是金属元素,Y与Z能形成Z2Y、Z2Y2型化合物,Z与W形成化学式为Z2W的化合物,五种元素的原子半径与原子序数的关系如图所示。下列推断正确的是
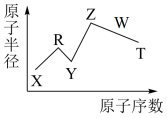

| A.原子半径和离子半径均满足:Y<Z |
| B.最高价氧化物对应的水化物的酸性:T<W<R |
| C.简单氢化物的稳定性:Y>T |
| D.由X、Y、Z、R四种元素组成的化合物中只含有共价键 |
您最近一年使用:0次
2022-09-10更新
|
235次组卷
|
2卷引用:山东省菏泽市2020-2021学年高一下学期期末考试化学试题
名校
解题方法
3 . W、X、Y、Z、R是五种短周期主族元素,原子序数依次增大。W元素的一种离子与 具有相同的电子层排布且半径稍大,X原子核外L层的电子数与Y原子核外M层的电子数之比为
具有相同的电子层排布且半径稍大,X原子核外L层的电子数与Y原子核外M层的电子数之比为 ,X与Z同主族,Z的价电子排布式为3s23p4,下列说法不正确的是
,X与Z同主族,Z的价电子排布式为3s23p4,下列说法不正确的是
 具有相同的电子层排布且半径稍大,X原子核外L层的电子数与Y原子核外M层的电子数之比为
具有相同的电子层排布且半径稍大,X原子核外L层的电子数与Y原子核外M层的电子数之比为 ,X与Z同主族,Z的价电子排布式为3s23p4,下列说法不正确的是
,X与Z同主族,Z的价电子排布式为3s23p4,下列说法不正确的是| A.与W生成的气态化合物的热稳定性:Z>Y |
B.W与 的原子半径:W<Li 的原子半径:W<Li |
| C.X和Y的第一电离能:X>Y |
D.X、Z、R的电负性: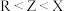 |
您最近一年使用:0次
2022-03-19更新
|
763次组卷
|
10卷引用:山东省泰安市2020-2021学年高二上学期期末考试化学试题
山东省泰安市2020-2021学年高二上学期期末考试化学试题(已下线)专题二 原子结构与元素的性质-2020-2021学年高二《新题速递·化学》(人教版选修3)2月刊 (同步课堂必刷题)(已下线)专题二 原子结构与元素的性质-2020-2021学年高二《新题速递·化学》(人教版2019选择性必修2)2月刊 (同步课堂必刷题)陕西省咸阳市实验中学2021-2022学年高二上学期第一次月考化学试题辽宁省凤城市第一中学2021-2022学年高二上学期12月月考化学试题 山东省菏泽第一中学2022-2023学年高二上学期期末考试化学试题(已下线)化学-2022年高考押题预测卷01(江苏卷)第一章原子结构与性质(基础卷)江西省宜春市宜丰中学2023-2024学年高二上学期12月月考化学试题广东省江门市广雅中学2023-2024学年高二下学期3月月考化学试题A卷
4 . 用中子轰击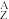 X原子产生α粒子(即氦核
X原子产生α粒子(即氦核 He)的核反应为
He)的核反应为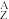 X+
X+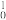 n→
n→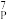 Y+
Y+ He。已知元素Y在化合物中呈+1价,下列说法正确的是
He。已知元素Y在化合物中呈+1价,下列说法正确的是
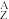 X原子产生α粒子(即氦核
X原子产生α粒子(即氦核 He)的核反应为
He)的核反应为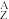 X+
X+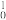 n→
n→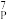 Y+
Y+ He。已知元素Y在化合物中呈+1价,下列说法正确的是
He。已知元素Y在化合物中呈+1价,下列说法正确的是A.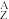 X原子核内中子数与核外电子数之差为5 X原子核内中子数与核外电子数之差为5 |
| B.6Y和7Y属于同种元素 |
| C.Y的核素种类由P决定 |
| D.金属性:X>Y |
您最近一年使用:0次
2021-12-30更新
|
359次组卷
|
3卷引用:山东省威海乳山市2021-2022学年高二上学期期中考试化学试题
解题方法
5 . 下列关于元素周期表的叙述正确的是
| A.周期表中有七个主族,八个副族 |
| B.主族元素的原子形成单原子离子时,其离子的化合价与元素所在族序数相等 |
| C.短周期元素是指1~20号元素 |
| D.从IIIB到IIB共10个纵列的元素都是金属元素,称为过渡金属 |
您最近一年使用:0次
6 . LDFCB是锂离子电池的一种电解质,该电解质阴离子由同周期元素W、X、Y、Z构成(如下图),Y的最外层电子数等于X的核外电子总数,四种元素最外层电子数之和为20.下列说法正确的是
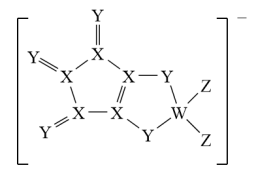

| A.Z的气态氢化物水溶液中存在3种氢键 |
| B.X2Z4的聚合物可用来制作不粘锅涂层 |
| C.W、Z形成的分子中各原子均满足8电子稳定结构 |
| D.YZ2分子的VSEPR模型为角形 |
您最近一年使用:0次
2021-12-21更新
|
253次组卷
|
2卷引用:山东省潍坊市2021-2022学年高三上学期学科核心素养测评化学试题
7 . 短周期主族元素X、Y、Z、W的原子序数依次增大,它们原子的最外层电子数之和为18,X最外层电子数是次外层电子数的3倍,Z的单质晶体是应用广泛的半导体材料,W与X位于同一主族。下列说法不正确的是
| A.X、W都能与Y形成离子化合物 | B.W的简单阴离子能促进水电离 |
| C.原子半径:r(W)>r(Z)>r(Y)>r(X) | D.最高价氧化物对应水化物的酸性:W>Z |
您最近一年使用:0次
2021-12-19更新
|
1131次组卷
|
7卷引用:山东省滨州市2021-2022学年高三上学期第一次检测化学试题
山东省滨州市2021-2022学年高三上学期第一次检测化学试题陕西省汉中市2021-2022学年高三上学期教学质量第一次检测考试化学试题(已下线)第一单元培优练-2021-2022学年高二化学课后培优练(人教版2019选择性必修2)(已下线)一轮巩固卷9-【赢在高考·黄金20卷】备战2022年高考化学模拟卷(全国卷专用)(已下线)必刷卷03-2022年高考化学考前信息必刷卷(广东专用)重庆市巫山县官渡中学2021-2022学年高二下学期期末考试化学试题黑龙江省哈尔滨师范大学青冈实验中学校2021-2022学年高二下学期开学考试化学试题
名校
解题方法
8 . 短周期主族元素X、Y、Z、W原子序数依次增大,X原子核外有7个电子,基态Y原子无未成对电子,Z与X为同族元素,W最高价含氧酸为二元酸,下列说法正确的是
| A.原子半径:r(X)<r(Y)<r(Z)<r(W) |
| B.元素Y、W的简单离子具有相同的电子层结构 |
| C.Z的最高价氧化物对应水化物的酸性比X的强 |
| D.第一电离能:I1(Y)<I1(W)<I1(Z) |
您最近一年使用:0次
2021-12-07更新
|
381次组卷
|
2卷引用:山东省日照市2021-2022学年高三上学期校际联考化学试题
名校
解题方法
9 .  、
、 、
、 、
、 、
、 是元素周期表中前20号的主族元素,它们的原子序数依次增大。
是元素周期表中前20号的主族元素,它们的原子序数依次增大。 原子的
原子的 层电子数是其
层电子数是其 层电子数的3倍,
层电子数的3倍, 是短周期金属性最强的元素,
是短周期金属性最强的元素, 是地壳中含量最多的金属元素,
是地壳中含量最多的金属元素, 与
与 同主族。回答下列问题:
同主族。回答下列问题:
(1) 在元素周期表中的位置为
在元素周期表中的位置为___________ ; 、
、 非金属性较强的是
非金属性较强的是___________ (填元素符号)。
(2) 、
、 简单离子半径较小的是
简单离子半径较小的是___________ (填离子符号)。
(3) 、
、 最高价氧化物对应水化物的碱性较弱的是
最高价氧化物对应水化物的碱性较弱的是___________ (填化学式)。
(4) 、
、 最高价氧化物对应水化物之间反应的化学方程式为
最高价氧化物对应水化物之间反应的化学方程式为___________ 。
 、
、 、
、 、
、 、
、 是元素周期表中前20号的主族元素,它们的原子序数依次增大。
是元素周期表中前20号的主族元素,它们的原子序数依次增大。 原子的
原子的 层电子数是其
层电子数是其 层电子数的3倍,
层电子数的3倍, 是短周期金属性最强的元素,
是短周期金属性最强的元素, 是地壳中含量最多的金属元素,
是地壳中含量最多的金属元素, 与
与 同主族。回答下列问题:
同主族。回答下列问题:(1)
 在元素周期表中的位置为
在元素周期表中的位置为 、
、 非金属性较强的是
非金属性较强的是(2)
 、
、 简单离子半径较小的是
简单离子半径较小的是(3)
 、
、 最高价氧化物对应水化物的碱性较弱的是
最高价氧化物对应水化物的碱性较弱的是(4)
 、
、 最高价氧化物对应水化物之间反应的化学方程式为
最高价氧化物对应水化物之间反应的化学方程式为
您最近一年使用:0次
2021-10-09更新
|
443次组卷
|
3卷引用:山东省2021年普通高中合格考化学试题
10 . 下表是部分短周期元素的性质或原子结构特点。
请回答下列问题:
(1)T元素的离子结构示意图为___________ ;元素X的一种质子数与中子数相同的核素符号为___________ 。
(2)元素Y与氢元素形成一种离子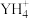 ,检验某溶液中含该离子的方法是
,检验某溶液中含该离子的方法是___________ 。
(3)元素Z在元素周期表中的位置是___________ ,元素Z与元素T相比,元素原子得电子能力较强的是___________ (用元素符号表示)。下列表述中能证明这一事实的是___________ (填序号)。
a.常温下Z的单质和T的单质状态不同
b.Z元素的氢化物比T元素的氢化物稳定
c.一定条件下Z和T的单质都能与氢氧化钠溶液反应
(4)T、X、Y、Z四种元素的最高价氧化物对应水化物中性质明显不同于其他三种的是___________ (填化学式),理由是___________ 。
(5)Z的最高价氧化物对应水化物与W的最高价氧化物对应水化物反应的离子方程式为___________ ;T的低价氧化物与Z的单质等体积混合后通入品红溶液中品红不褪色。原因是___________ (用化学方程式表示)。
| 元素编号 | 元素性质或原子结构 |
| T | M层上有6个电子 |
| X | 最外层电子数是次外层电子数的2倍 |
| Y | 常温下单质为双原子分子,其氢化物水溶液呈碱性 |
| Z | 元素最高正价是 价 价 |
| W | 其最高价氧化物对应水化物既能跟酸反应,又能跟强碱反应 |
(1)T元素的离子结构示意图为
(2)元素Y与氢元素形成一种离子
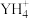 ,检验某溶液中含该离子的方法是
,检验某溶液中含该离子的方法是(3)元素Z在元素周期表中的位置是
a.常温下Z的单质和T的单质状态不同
b.Z元素的氢化物比T元素的氢化物稳定
c.一定条件下Z和T的单质都能与氢氧化钠溶液反应
(4)T、X、Y、Z四种元素的最高价氧化物对应水化物中性质明显不同于其他三种的是
(5)Z的最高价氧化物对应水化物与W的最高价氧化物对应水化物反应的离子方程式为
您最近一年使用:0次



