名校
解题方法
1 . W、X、Y、Z为原子序数依次增大的短周期主族元素,其原子的最外层电子数之和为18,W和Y同主族,X、Y、Z同周期,X原子的电子层数与最外层电子数相等,Z元素最高正价与最低负价的代数和为6.下列说法不正确的是
| A.Z的氧化物的水化物酸性一定大于W | B.W的某种单质的沸点比X高 |
| C.W与Y可形成一种硬度很大的化合物 | D.W、X、Y均能与Z形成共价化合物 |
您最近一年使用:0次
名校
解题方法
2 . 短周期主族元素a、b、c、d 的原子序数依次增大,这四种元素形成的单质依次为m、n、p、q;x、y、z是由这些元素组成的二元化合物,其中z 为形成酸雨的主要物质之一;25℃时,0.01mol·L-l w溶液中, =1.0×10-10。上述物质的转化关系如图所示,下列说法正确的是
=1.0×10-10。上述物质的转化关系如图所示,下列说法正确的是
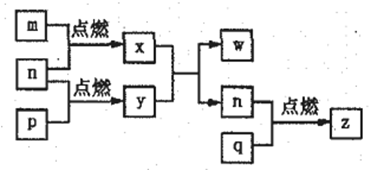
 =1.0×10-10。上述物质的转化关系如图所示,下列说法正确的是
=1.0×10-10。上述物质的转化关系如图所示,下列说法正确的是
| A.原子半径的大小:a<b<c<d |
| B.简单氢化物的沸点:b>d |
C.y 的电子式: |
| D.y、w 含有的化学键类型完全相同 |
您最近一年使用:0次
2018-04-29更新
|
431次组卷
|
3卷引用:【全国市级联考】河南省洛阳市2018届高三下学期尖子生第二次联考化学试题
【全国市级联考】河南省洛阳市2018届高三下学期尖子生第二次联考化学试题【全国百强校】新疆维吾尔自治区乌鲁木齐市第一中学2019届高三上学期第一次月考(9月)化学试题(已下线)专题讲座(五) “位-构-性”综合推断题的解题方法(精练)-2021年高考化学一轮复习讲练测
名校
解题方法
3 . 短周期主族元素a、b、c、d原子序数依次增大,b元素的一种同位素可用于考古年代鉴定。甲、乙分别是元素b、d的单质,通常甲为固体,乙为气体,0.00l mol/L的丙溶液pH=3;W、X、Y均是由这些元素构成的二元化合物,Y是形成酸雨的主要物质之一。上述物质的转化关系如图,下列说法正确的是
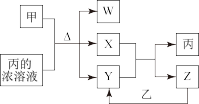

| A.原子半径:b>d>c |
| B.a、c、d形成的化合物一定是共价化合物 |
| C.W、X、Y中X的熔沸点最高 |
| D.Y、Z均可用排水法收集 |
您最近一年使用:0次
2018-04-25更新
|
329次组卷
|
3卷引用:【全国市级联考】四川省绵阳市2018届高三第三次诊断性考试理综化学试题
解题方法
4 . 短周期元素W、X、Y、Z在元素周期表中的相对位置如下图所示,其中W的最高正价和最低负价的代数和为2。下列判断正确的是
| W | |||
| X | Y | Z |
| A.最高价氧化物对应水化物的酸性:Y>W |
| B.最简单气态氢化物的稳定性:Z>Y |
| C.元素W与元素Y形成的化合物Y3W4是一种新型有机材料 |
| D.X的单质能与W的最高价氧化物对应水化物的浓溶液反应产生氢气 |
您最近一年使用:0次
名校
5 . 短周期主族元素X、Y、Z、W原子序数依次增大,X 与Y、Z、W不在同一周期,Y最外层电子数是次外层电子数的3倍,W与Y同主族,Z是地壳中含量最多的金属元素。下列说法正确的是( )
| A.Y的单质的氧化性比W的弱 |
| B.原子半径:r(X)< r(Y)< r(W)< r(Z) |
| C.化合物X2Y和Z2Y3,含有相同类型的化学键 |
| D.元素Y、Z形成的化合物熔点高,不能用电解法制备其中的金属单质 |
您最近一年使用:0次
2018-01-13更新
|
443次组卷
|
5卷引用:湖北省黄冈市2018届高三上学期元月调研考试理综化学试题
解题方法
6 . Ⅰ.几种短周期元素的原子半径及主要化合价如下表:已知X是短周期中最活泼的金属,且与R同周期。(请用化学用语答题)
(1)R的元素符号为_______ ; M在元素周期表中的位置为___________________ 。
(2)X与Y按原子个数比1:1构成的物质的电子式为________ ;所含化学键类型________ 。
(3)X+, Y2‾,M2‾ 离子半径大小顺序为________________________________ 。
(4)将YM2通入FeCl3溶液中的离子方程式_________________________________ 。
(5)用Cu单质作阳极,石墨作阴极,X的最高价氧化物对应的水化物溶液作电解液进行电解,写出阳极的反应式_________________________ 。
Ⅱ.如下图转化关系

①若B为白色胶状不溶物,则A与C反应的离子方程式为____________________________ 。
②若向B溶液中滴加铁氰化钾溶液会产生特征蓝色沉淀,则A与C反应的离子方程式为______________________________ 。
元素代号 | X | Y | Z | M | R |
原子半径/nm | 0.186 | 0.102 | 0.075 | 0.074 | 0.143 |
主要化合价 | +1 | +6 -2 | +5 -3 | -2 | +3 |
(2)X与Y按原子个数比1:1构成的物质的电子式为
(3)X+, Y2‾,M2‾ 离子半径大小顺序为
(4)将YM2通入FeCl3溶液中的离子方程式
(5)用Cu单质作阳极,石墨作阴极,X的最高价氧化物对应的水化物溶液作电解液进行电解,写出阳极的反应式
Ⅱ.如下图转化关系

①若B为白色胶状不溶物,则A与C反应的离子方程式为
②若向B溶液中滴加铁氰化钾溶液会产生特征蓝色沉淀,则A与C反应的离子方程式为
您最近一年使用:0次
名校
解题方法
7 . 下表为元素周期表中短周期的一部分,其中Y元素的原子序数为M与N元素原子序数之和。下列说法正确的是
| M | N | ||
| X | Y | Z |
| A.氢化物的稳定性:N>Z,是因为其氢化物分子可形成氢键 |
| B.元素的非金属性:M>Y,是因为单质M能与YN2反应生成单质Y |
| C.熔沸点:YN2>MN2,是因为YN2的分子间作用力强 |
| D.简单离子的半径:N>X,是因为它们具有相同的电子层结构且X的核电荷数更大 |
您最近一年使用:0次
2017-03-13更新
|
519次组卷
|
2卷引用:2017届湖北省黄冈市高三3月质量检测理科综合化学试卷
8 . W、R、X、Y、Z是原子序数依次增大的短周期主族元素。Y原子半径在短周期主族元素中最大。W与Y同主族,X与Z同主族。R原子最外层电子数比内层电子数多3,W、Y原子的电子数总和与X、Z原子的电子数总和之比为1∶2。下列说法正确的是
| A.原子半径: r(X)>r(R)>r(W) |
| B.X与Y只能形成一种化合物 |
| C.X的简单气态氢化物的热稳定性比Z的弱 |
| D.由W、R、X三种元素组成的化合物可以是酸、碱或盐 |
您最近一年使用:0次
2017-02-27更新
|
769次组卷
|
7卷引用:江苏省镇江市2017届高三三模(最后一卷)化学试题
2014·全国·一模
名校
解题方法
9 . 短周期元素X、Y、Z、W的原子序数依次增大,X 原子的最外层电子数是其内层电子总数的3 倍,Y 原子的最外层只有2 个电子,Z 单质可制成半导体材料,W与X属于同一主族。下列叙述正确的是
| A.元素W的简单气态氢化物的热稳定性比X 的强 |
| B.元素W 的最高价氧化物对应水化物的酸性比Z 的弱 |
| C.化合物YX、ZX2、WX3中化学键的类型相同 |
| D.原子半径的大小顺序: rY>rZ>rW>rX |
您最近一年使用:0次
2016-12-09更新
|
700次组卷
|
4卷引用:2014高考名师推荐化学化学键与分之间作用力
(已下线)2014高考名师推荐化学化学键与分之间作用力(已下线)2013-2014甘肃省兰州一中下学期期中考试高二化学试卷【全国百强校】甘肃省兰州市第一中学2019届高三上学期12月月考化学试题甘肃省天水市一中2020届高三上学期第四次考试化学试题
13-14高三上·上海黄浦·期末
解题方法
10 . 现有1——20号元素A、B、C、D所对应的物质的性质或微粒结构如下表:
(1)元素A的原子最外层共有______ 种不同运动状态的电子,有___ 种能量不同的电子。B的
离子与D的离子相互组合形成的干燥剂的化学式是_________ 。
(2)元素C与氢元素形成带一个单位正电荷的离子,写出该微粒的电子式(用元素符号表示)
_________________
(3)元素A与元素D相比,非金属性较强的是_____ (用元素符号表示),下列表述中能证明
这一事实的是_______
A.常温下A的单质和D的单质状态不同
B.A的氢化物比D的氢化物稳定
C.一定条件下D能从A的氢化物水溶液中置换出A单质
D.HD的酸性比HA酸性强
(4)C的氢化物固态时属于______ 晶体,该氢化物与A的最高价氧化物水化物反应的化学方程式是__________________________________________________ 。
| 元素 | 物质性质或微粒结构 |
| A | M层上有2对成对电子 |
| B | B的离子与D的离子具有相同电子层结构,且可以相互组合形成干燥剂 |
| C | 常温下单质为双原子分子,其氢化物水溶液呈碱性 |
| D | 元素最高正价是+7价 |
(1)元素A的原子最外层共有
离子与D的离子相互组合形成的干燥剂的化学式是
(2)元素C与氢元素形成带一个单位正电荷的离子,写出该微粒的电子式(用元素符号表示)
(3)元素A与元素D相比,非金属性较强的是
这一事实的是
A.常温下A的单质和D的单质状态不同
B.A的氢化物比D的氢化物稳定
C.一定条件下D能从A的氢化物水溶液中置换出A单质
D.HD的酸性比HA酸性强
(4)C的氢化物固态时属于
您最近一年使用:0次



