1 . 通过复习总结,下列归纳正确的是
| A.简单非金属阴离子只有还原性,而金属阳离子一定只有氧化性 |
B.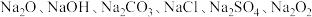 都属于钠的含氧化合物 都属于钠的含氧化合物 |
C.日本福岛核电站爆炸时释放的两种放射性同位素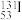 与 与 的中子数相等 的中子数相等 |
D.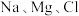 是海水中的重要元素,从海水中制备这三种元素单质的反应都是氧化还原反应 是海水中的重要元素,从海水中制备这三种元素单质的反应都是氧化还原反应 |
您最近一年使用:0次
2 . 硅是地壳中含量第二大的元素,其单质是一种重要的半导体材料。
(1) 是硅的一种同位素,其原子核内质子数为
是硅的一种同位素,其原子核内质子数为_______ ,Si原子的电子式为_______ 。Si与C的化学性质相似,由此猜想二者在原子结构上的相似之处是_______ 。
(2)如图中,“28.09”的含义是指_______ 。
(3)硅元素在自然界中通常以石英石( )和硅酸盐的形式存在。已知
)和硅酸盐的形式存在。已知 是一种酸性氧化物,请写出其与氢氧化钠溶液反应的化学方程式
是一种酸性氧化物,请写出其与氢氧化钠溶液反应的化学方程式_______ 。0.1mol的硅酸根离子( )中含有质子
)中含有质子_______ mol,电子_______ 个。
(4)高纯硅单质可由石英砂(主要成分是SiO2)制得,制备高纯硅的主要工艺流程如图所示:

i.硅元素有无定形硅和晶体硅两种单质,他们互为_______ ;
ii.流程①焦炭体现了_______ (填“氧化性”或“还原性”)。
iii.流程④的化学反应为置换反应,写出其化学方程式:_______ 。
(1)
 是硅的一种同位素,其原子核内质子数为
是硅的一种同位素,其原子核内质子数为(2)如图中,“28.09”的含义是指
| 14 Si 硅 28.09 |
 )和硅酸盐的形式存在。已知
)和硅酸盐的形式存在。已知 是一种酸性氧化物,请写出其与氢氧化钠溶液反应的化学方程式
是一种酸性氧化物,请写出其与氢氧化钠溶液反应的化学方程式 )中含有质子
)中含有质子(4)高纯硅单质可由石英砂(主要成分是SiO2)制得,制备高纯硅的主要工艺流程如图所示:

i.硅元素有无定形硅和晶体硅两种单质,他们互为
ii.流程①焦炭体现了
iii.流程④的化学反应为置换反应,写出其化学方程式:
您最近一年使用:0次
名校
解题方法
3 . 下列叙述正确的是
| A.两粒子若核外电子排布完全相同,则其化学性质相同 |
| B.凡单核原子形成的离子,一定具有稀有气体元素原子的核外电子排布 |
| C.单核微粒的阴离子一定具有还原性、阳离子一定具有氧化性 |
| D.两粒子如果质子数及核外电子数均相同,则两者一定属于同种元素 |
您最近一年使用:0次
名校
解题方法
4 . 下列说法正确的是
①氧化剂具有氧化性
②某元素在反应中由化合物转化为单质,该元素一定被氧化
③失电子越多的还原剂,其还原性越强
④中国科学家胡炳成教授团队近日成功合成全氮阴离子N ,每个N
,每个N 中含有36个电子
中含有36个电子
⑤氢键是一种较弱的化学键
①氧化剂具有氧化性
②某元素在反应中由化合物转化为单质,该元素一定被氧化
③失电子越多的还原剂,其还原性越强
④中国科学家胡炳成教授团队近日成功合成全氮阴离子N
 ,每个N
,每个N 中含有36个电子
中含有36个电子⑤氢键是一种较弱的化学键
| A.②④ | B.①④ | C.②③④ | D.②④⑤ |
您最近一年使用:0次
19-20高一·全国·课时练习
5 . 某同学在画某种原色的一种单核微粒的结构示意图时,忘记在圆圈内标出其核电荷数,请你根据下面的提示做出自己的判断。

(1)若该微粒是电中性微粒,这种微粒的元素符号是_____________ 。
(2)若该微粒的还原性很弱,失去1个电子后变为原子,该原子的单质氧化性很强,该单质与水反应的 化学方程式为______________ 。
(3)若该微粒的氧化性很弱,得到1个电子后变为原子,该原子的单质还原性很强,该单质在氧气中燃烧所得产物的化学式为_______________ 。
(4)若该微粒的还原性很弱,失去2个电子后变成原子,其氢化物的结构式为_____________ 。
(5)若该微粒的符号为X3+,其氢氧化物与强碱反应的离子方程式为___________________ 。

(1)若该微粒是电中性微粒,这种微粒的元素符号是
(2)若该微粒的还原性很弱,失去1个电子后变为原子,该原子的单质氧化性很强,该单质与水反应的 化学方程式为
(3)若该微粒的氧化性很弱,得到1个电子后变为原子,该原子的单质还原性很强,该单质在氧气中燃烧所得产物的化学式为
(4)若该微粒的还原性很弱,失去2个电子后变成原子,其氢化物的结构式为
(5)若该微粒的符号为X3+,其氢氧化物与强碱反应的离子方程式为
您最近一年使用:0次
名校
解题方法
6 . 已知X、Y、Z、W原子序数都不超过18,它们的离子aX (n+1)+、bY n+、cZ (n+1)-、dW n-具有相同的电子层结构,则下列说法正确的是
| A.原子序数:a>b>c>d | B.离子半径:X (n+1)+>Y n+>Z (n+1)->W n- |
| C.单质还原性:X <Y | D.单质氧化性:Z>W |
您最近一年使用:0次
2019-12-26更新
|
90次组卷
|
2卷引用:贵州省贵阳清镇北大培文学校2018-2019学年高一下学期3月份月考化学试题
解题方法
7 . 有几种元素的微粒的最外电子层结构如图所示, 其中:
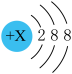
(1)某电中性微粒一般不和其他元素的原子反应, 这种微粒符号是_______ ;
(2)某微粒的盐溶液, 加入AgNO3溶液时会出现白色浑浊, 这种微粒符号是_____ ;
(3)某微粒氧化性甚弱, 但得到电子后还原性强, 且这种原子有一个单电子, 这种微粒的符号是_______ ;
(4)某微粒具有还原性, 且这种微粒失去 2 个电子即变为原子, 这种微粒的符号是___

(1)某电中性微粒一般不和其他元素的原子反应, 这种微粒符号是
(2)某微粒的盐溶液, 加入AgNO3溶液时会出现白色浑浊, 这种微粒符号是
(3)某微粒氧化性甚弱, 但得到电子后还原性强, 且这种原子有一个单电子, 这种微粒的符号是
(4)某微粒具有还原性, 且这种微粒失去 2 个电子即变为原子, 这种微粒的符号是
您最近一年使用:0次
11-12高三上·湖北黄冈·阶段练习
名校
8 . 已知A、B、C、D的原子序数都不超过18,它们的离子aA(n+1)+、bBn+、cC(n+1)-、dDn-均具有相同的电子层结构,则下列叙述正确的是( )
| A.原子序数:a>b>c>d |
| B.单质还原性:B>A,单质氧化性:D>C |
| C.离子还原性:A(n+1)+>Bn+,离子氧化性:C(n+1)->Dn- |
| D.离子半径:A(n+1)+>Bn+>C(n+1)->Dn- |
您最近一年使用:0次
2019-09-02更新
|
112次组卷
|
12卷引用:2011-2012学年辽宁省抚顺县高级中学高一4月月考化学试卷
(已下线)2011-2012学年辽宁省抚顺县高级中学高一4月月考化学试卷(已下线)2011-2012学年内蒙古巴市一中高一下学期4月月考化学试卷(已下线)2011-2012学年江西省九江一中高一下学期期中考试理科化学试卷(已下线)2011-2012学年江西省吉安二中高一6月月考化学试卷(已下线)2011-2012学年山东省汶上一中高一下学期期中考试化学试卷2014—2015江西省九江市彭泽县第二高中高一下学期期中考试化学试卷2014-2015学年辽宁省沈阳市第二中学高一下期中化学试卷湖北省武汉市钢城四中2017-2018学年高一下学期3月月考化学试题安徽省淮北市树人高级中学2020-2021学年高一下学期第一次阶段考试化学试题(已下线)2012届湖北省武穴中学高三上学期11月份月考化学试卷黑龙江省大庆铁人中学2019-2020学年高二上学期入学考试化学试题辽宁省营口市第二高级中学2020届高三上学期第一次月考化学试题
解题方法
9 . Ⅰ.  U是重要的核工业原料,在自然界的丰度很低。
U是重要的核工业原料,在自然界的丰度很低。 U的浓缩一直为国际社会关注。回答下列有关问题:
U的浓缩一直为国际社会关注。回答下列有关问题:
(1) U的中子数是
U的中子数是___ 。
(2) U、
U、 U、
U、 U互为同位素,下列对同位素的理解不正确的是
U互为同位素,下列对同位素的理解不正确的是___ (填序号,下同)。
A.元素符号相同 B.物理性质相同 C.化学性质基本相同 D.在周期表中位置相同
(3)下列有关 U说法不正确的是
U说法不正确的是___ 。
A. U原子核内中子数与质子数之差为51
U原子核内中子数与质子数之差为51
B. U与
U与 U的质子数、电子数都相等
U的质子数、电子数都相等
C. U与
U与 U是两种质子数相同,中子数不同的原子
U是两种质子数相同,中子数不同的原子
D. U与
U与 U是同种原子
U是同种原子
Ⅱ.锂的材料在社会生活中广泛应用,如亚氨基锂(Li2NH)是一种储氢容量高、安全性好的固体储氢材料,LiCoO2用作便携式电源的正极材料,碳酸锂(Li2CO3)广泛应用于陶瓷和医药等领域。根据下列要求回答相关问题:
(1)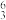 Li和
Li和 Li用作核反应堆最佳载热体,
Li用作核反应堆最佳载热体, LiH和
LiH和 LiD用作高温堆减速剂。下列说法中正确的是
LiD用作高温堆减速剂。下列说法中正确的是_______ (填序号,下同)。
A.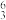 Li和
Li和 Li互为同位素 B
Li互为同位素 B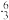 Li和
Li和 Li属于同种核素
Li属于同种核素
C. LiH和
LiH和 LiD的化学性质不同 D.
LiD的化学性质不同 D. LiH和
LiH和 LiD是同种物质
LiD是同种物质
(2)下列说法不正确的是_________ 。
A.碱性:Be(OH)2<LiOH<NaOH<KOH B.半径:K>Na>Li>Li+
C.氧化性:Li+<Na+<K+<Rb+<Cs+ D.金属性:Cs>Rb>K>Na>Li>Be
 U是重要的核工业原料,在自然界的丰度很低。
U是重要的核工业原料,在自然界的丰度很低。 U的浓缩一直为国际社会关注。回答下列有关问题:
U的浓缩一直为国际社会关注。回答下列有关问题:(1)
 U的中子数是
U的中子数是(2)
 U、
U、 U、
U、 U互为同位素,下列对同位素的理解不正确的是
U互为同位素,下列对同位素的理解不正确的是A.元素符号相同 B.物理性质相同 C.化学性质基本相同 D.在周期表中位置相同
(3)下列有关
 U说法不正确的是
U说法不正确的是A.
 U原子核内中子数与质子数之差为51
U原子核内中子数与质子数之差为51B.
 U与
U与 U的质子数、电子数都相等
U的质子数、电子数都相等C.
 U与
U与 U是两种质子数相同,中子数不同的原子
U是两种质子数相同,中子数不同的原子D.
 U与
U与 U是同种原子
U是同种原子Ⅱ.锂的材料在社会生活中广泛应用,如亚氨基锂(Li2NH)是一种储氢容量高、安全性好的固体储氢材料,LiCoO2用作便携式电源的正极材料,碳酸锂(Li2CO3)广泛应用于陶瓷和医药等领域。根据下列要求回答相关问题:
(1)
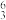 Li和
Li和 Li用作核反应堆最佳载热体,
Li用作核反应堆最佳载热体, LiH和
LiH和 LiD用作高温堆减速剂。下列说法中正确的是
LiD用作高温堆减速剂。下列说法中正确的是A.
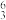 Li和
Li和 Li互为同位素 B
Li互为同位素 B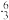 Li和
Li和 Li属于同种核素
Li属于同种核素C.
 LiH和
LiH和 LiD的化学性质不同 D.
LiD的化学性质不同 D. LiH和
LiH和 LiD是同种物质
LiD是同种物质(2)下列说法不正确的是
A.碱性:Be(OH)2<LiOH<NaOH<KOH B.半径:K>Na>Li>Li+
C.氧化性:Li+<Na+<K+<Rb+<Cs+ D.金属性:Cs>Rb>K>Na>Li>Be
您最近一年使用:0次
名校
10 . 已知A、B、C、D的原子序数都不超过18,它们的离子aAm+、bBn+ 、cCm- 、dDn- (m>n)均具有相同的电子层结构,则下列叙述正确的是
| A.原子序数:a>b>c>d | B.离子半径:aAm+>bBn+>cCm->dDn- |
| C.离子还原性:aAm+ >bBn+,离子氧化性:cCm- >dDn- | D.单质还原性:B>A,单质氧化性:D>C |
您最近一年使用:0次



