1 . 实验室加热液体时,常加入沸石、其主要成分为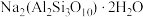 ,根据其组成元素完成下列填空:
,根据其组成元素完成下列填空:
(1)指出 元素在周期表中的位置
元素在周期表中的位置_______ 。
(2)沸石中的元素可形成多种化合物; 元素与原子半径最小的元素组成化合物甲,常作强还原剂,化合物甲的电子式为
元素与原子半径最小的元素组成化合物甲,常作强还原剂,化合物甲的电子式为_______ ;化合物乙可作为呼吸面具或潜艇氧气的来源,乙是_______ (填化学式),化合物乙中存在的化学键类型为_______ 。
(3)O元素和其同周期相邻的两种元素分别形成的简单氢化物中最稳定的是_______ (填化学式)。
(4)已知硅酸(H2SiO3)为白色胶状沉淀。
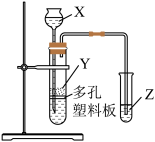
实验室中现有药品:①稀盐酸、②稀硫酸、③NaHCO3固体、④CaCO3固体、⑤Na2SiO3溶液,请选择合适药品利用上述装置设计实验验证C、Si的非金属性的变化规律;装置X、Y、Z处所盛装或放置的药品分别为_______ 、_______ 、_______ (填序号)。但有同学认为该实验所得现象无法充分证明C、Si的非金属性强弱,如何改进?_______ 。
(5)Uue是暂时未合成的化学元素,与Na同主族,位于第八周期,称为类钫,其一种可能存在的核素原子核中有180个中子,则 中A=
中A=_______ 、Z=_______ 。
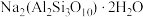 ,根据其组成元素完成下列填空:
,根据其组成元素完成下列填空:(1)指出
 元素在周期表中的位置
元素在周期表中的位置(2)沸石中的元素可形成多种化合物;
 元素与原子半径最小的元素组成化合物甲,常作强还原剂,化合物甲的电子式为
元素与原子半径最小的元素组成化合物甲,常作强还原剂,化合物甲的电子式为(3)O元素和其同周期相邻的两种元素分别形成的简单氢化物中最稳定的是
(4)已知硅酸(H2SiO3)为白色胶状沉淀。

实验室中现有药品:①稀盐酸、②稀硫酸、③NaHCO3固体、④CaCO3固体、⑤Na2SiO3溶液,请选择合适药品利用上述装置设计实验验证C、Si的非金属性的变化规律;装置X、Y、Z处所盛装或放置的药品分别为
(5)Uue是暂时未合成的化学元素,与Na同主族,位于第八周期,称为类钫,其一种可能存在的核素原子核中有180个中子,则
 中A=
中A=
您最近一年使用:0次
名校
2 . 填空:
(1)有下列微粒或物质:① O、
O、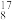 O、
O、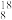 O②H2O、D2O③石墨、金刚石④H2、D2、T2⑤H、D、T⑥
O②H2O、D2O③石墨、金刚石④H2、D2、T2⑤H、D、T⑥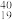 K、
K、 Ca、
Ca、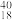 Ar,回答下列问题:
Ar,回答下列问题:
a.互为同位素的是_______ ;
b.互为同素异形体的是_______ ;
c.上述微粒中出现的核素符号有_______ 种;
d.由①和⑤中的微粒能结合成水,可得相对分子质量不同的水分子种数为_______ 种,相对分子质量最大的是_______ (写化学式)。
(2)相同质量的 H2
H2 O与
O与 H2
H2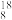 O所含中子数之比为
O所含中子数之比为_______ 。
(3)元素周期表中,甲、乙分别是第五周期的ⅡA族和ⅦA族元素,原子序数分别为m和n,则m和n的关系为_______ 。
(4)某中学化学兴趣小组同学为探究元素周期律,设计了如下实验。利用下图所示装置可以验证元素的非金属性的变化规律。
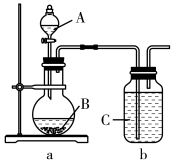
甲同学设计实验:A为硝酸,B为石灰石,C为硅酸钠溶液。实验现象:a装置中圆底烧瓶中产生大量气泡,b装置中出现浑浊或白色沉淀。
①甲同学由实验得出酸性由强到弱的顺序为:_______ 。
②乙同学分析甲同学设计的实验方案,认为该方案存在不足之处,请分析乙同学的理由_______ ,并提出改进实验方案_______ 。
(1)有下列微粒或物质:①
 O、
O、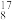 O、
O、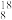 O②H2O、D2O③石墨、金刚石④H2、D2、T2⑤H、D、T⑥
O②H2O、D2O③石墨、金刚石④H2、D2、T2⑤H、D、T⑥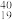 K、
K、 Ca、
Ca、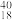 Ar,回答下列问题:
Ar,回答下列问题:a.互为同位素的是
b.互为同素异形体的是
c.上述微粒中出现的核素符号有
d.由①和⑤中的微粒能结合成水,可得相对分子质量不同的水分子种数为
(2)相同质量的
 H2
H2 O与
O与 H2
H2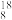 O所含中子数之比为
O所含中子数之比为(3)元素周期表中,甲、乙分别是第五周期的ⅡA族和ⅦA族元素,原子序数分别为m和n,则m和n的关系为
(4)某中学化学兴趣小组同学为探究元素周期律,设计了如下实验。利用下图所示装置可以验证元素的非金属性的变化规律。

甲同学设计实验:A为硝酸,B为石灰石,C为硅酸钠溶液。实验现象:a装置中圆底烧瓶中产生大量气泡,b装置中出现浑浊或白色沉淀。
①甲同学由实验得出酸性由强到弱的顺序为:
②乙同学分析甲同学设计的实验方案,认为该方案存在不足之处,请分析乙同学的理由
您最近一年使用:0次
名校
3 . 含氮化合物( 、
、 、
、 等)是环境污染物,可用以下方法消除其污染。
等)是环境污染物,可用以下方法消除其污染。
Ⅰ.苯酚( )是一种广泛使用、易氧化的化工产品。一种在
)是一种广泛使用、易氧化的化工产品。一种在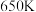 下用
下用 废气催化氧化苯制备苯酚的新方法为:
废气催化氧化苯制备苯酚的新方法为: 。
。
(1)已知



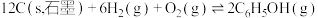
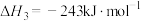
则

___________ 。
Ⅱ.在金属Pt、Cu和铱(Ir)的催化作用下,密闭容器中的 可高效转化酸性溶液中的硝态氮(
可高效转化酸性溶液中的硝态氮( ),以达到消除污染的目的,其工作原理如图-1所示。
),以达到消除污染的目的,其工作原理如图-1所示。
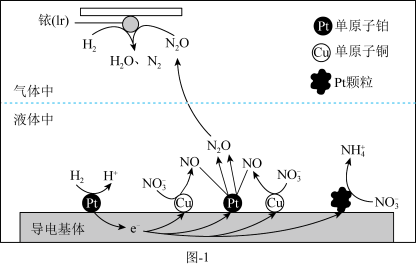
(2) 被
被 还原为
还原为 的过程可描述为:液体中,
的过程可描述为:液体中, 在导电基体的单原子铂上失去电子生成
在导电基体的单原子铂上失去电子生成 ,电子进入导电基体中进行传导,
,电子进入导电基体中进行传导,___________ 。
(3)若导电基体上的Pt颗粒增多,造成的后果是___________ 。
(4)单原子铂催化剂相比于Pt颗粒催化剂,优点有___________ 。
Ⅲ.三维电极法:它是在传统的电解槽两电极之间填充粒状或碎屑状材料,填充的粒子电极表面能带电,成为新的一极(第三极)。如图2为用三维电极法处理氨氮废水的原理图,石墨板作为阴、阳极,自制活性炭为填充材料,电解一定浓度的 、
、 与NaCl的酸性混合溶液来进行模拟。
与NaCl的酸性混合溶液来进行模拟。

(5)该装置可以生成大量氧化性更强的 ,
, 去除
去除 的离子方程式为
的离子方程式为___________ 。
(6)相比于传统的二维电极反应系统,三维电极的优点有___________ 。
 、
、 、
、 等)是环境污染物,可用以下方法消除其污染。
等)是环境污染物,可用以下方法消除其污染。Ⅰ.苯酚(
 )是一种广泛使用、易氧化的化工产品。一种在
)是一种广泛使用、易氧化的化工产品。一种在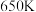 下用
下用 废气催化氧化苯制备苯酚的新方法为:
废气催化氧化苯制备苯酚的新方法为: 。
。(1)已知




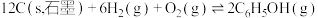
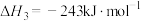
则


Ⅱ.在金属Pt、Cu和铱(Ir)的催化作用下,密闭容器中的
 可高效转化酸性溶液中的硝态氮(
可高效转化酸性溶液中的硝态氮( ),以达到消除污染的目的,其工作原理如图-1所示。
),以达到消除污染的目的,其工作原理如图-1所示。
(2)
 被
被 还原为
还原为 的过程可描述为:液体中,
的过程可描述为:液体中, 在导电基体的单原子铂上失去电子生成
在导电基体的单原子铂上失去电子生成 ,电子进入导电基体中进行传导,
,电子进入导电基体中进行传导,(3)若导电基体上的Pt颗粒增多,造成的后果是
(4)单原子铂催化剂相比于Pt颗粒催化剂,优点有
Ⅲ.三维电极法:它是在传统的电解槽两电极之间填充粒状或碎屑状材料,填充的粒子电极表面能带电,成为新的一极(第三极)。如图2为用三维电极法处理氨氮废水的原理图,石墨板作为阴、阳极,自制活性炭为填充材料,电解一定浓度的
 、
、 与NaCl的酸性混合溶液来进行模拟。
与NaCl的酸性混合溶液来进行模拟。
(5)该装置可以生成大量氧化性更强的
 ,
, 去除
去除 的离子方程式为
的离子方程式为(6)相比于传统的二维电极反应系统,三维电极的优点有
您最近一年使用:0次
名校
解题方法
4 . 回答下列问题:
(1)相同物质的量的14C18O2与32S16O2的原子数之比为_______ ,中子数之比为_______ ,电子数之比为_______ 。
(2)SiO2和NaOH焙烧制备硅酸钠,可采用的装置为_______ (填代号)。
(3)利用元素周期律可预测陌生元素及物质的性质,已知Rb与Na处于同一主族,下列说法正确的是_______。
(1)相同物质的量的14C18O2与32S16O2的原子数之比为
(2)SiO2和NaOH焙烧制备硅酸钠,可采用的装置为_______ (填代号)。
A. | B.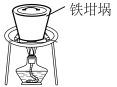 | C.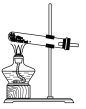 | D.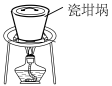 |
| A.失电子能力: Rb>Na |
| B.碱性: NaOH>RbOH |
| C.Rb比Na更易与氧气发生反应 |
| D.Rb不易与水反应放出H2 |
您最近一年使用:0次



