1 . 通过复习总结,下列归纳正确的是
| A.简单非金属阴离子只有还原性,而金属阳离子一定只有氧化性 |
B.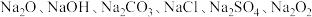 都属于钠的含氧化合物 都属于钠的含氧化合物 |
C.日本福岛核电站爆炸时释放的两种放射性同位素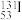 与 与 的中子数相等 的中子数相等 |
D.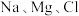 是海水中的重要元素,从海水中制备这三种元素单质的反应都是氧化还原反应 是海水中的重要元素,从海水中制备这三种元素单质的反应都是氧化还原反应 |
您最近半年使用:0次
2 . 硅是地壳中含量第二大的元素,其单质是一种重要的半导体材料。
(1) 是硅的一种同位素,其原子核内质子数为
是硅的一种同位素,其原子核内质子数为_______ ,Si原子的电子式为_______ 。Si与C的化学性质相似,由此猜想二者在原子结构上的相似之处是_______ 。
(2)如图中,“28.09”的含义是指_______ 。
(3)硅元素在自然界中通常以石英石( )和硅酸盐的形式存在。已知
)和硅酸盐的形式存在。已知 是一种酸性氧化物,请写出其与氢氧化钠溶液反应的化学方程式
是一种酸性氧化物,请写出其与氢氧化钠溶液反应的化学方程式_______ 。0.1mol的硅酸根离子( )中含有质子
)中含有质子_______ mol,电子_______ 个。
(4)高纯硅单质可由石英砂(主要成分是SiO2)制得,制备高纯硅的主要工艺流程如图所示:

i.硅元素有无定形硅和晶体硅两种单质,他们互为_______ ;
ii.流程①焦炭体现了_______ (填“氧化性”或“还原性”)。
iii.流程④的化学反应为置换反应,写出其化学方程式:_______ 。
(1)
 是硅的一种同位素,其原子核内质子数为
是硅的一种同位素,其原子核内质子数为(2)如图中,“28.09”的含义是指
| 14 Si 硅 28.09 |
 )和硅酸盐的形式存在。已知
)和硅酸盐的形式存在。已知 是一种酸性氧化物,请写出其与氢氧化钠溶液反应的化学方程式
是一种酸性氧化物,请写出其与氢氧化钠溶液反应的化学方程式 )中含有质子
)中含有质子(4)高纯硅单质可由石英砂(主要成分是SiO2)制得,制备高纯硅的主要工艺流程如图所示:

i.硅元素有无定形硅和晶体硅两种单质,他们互为
ii.流程①焦炭体现了
iii.流程④的化学反应为置换反应,写出其化学方程式:
您最近半年使用:0次
名校
解题方法
3 . 下列叙述正确的是
| A.两粒子若核外电子排布完全相同,则其化学性质相同 |
| B.凡单核原子形成的离子,一定具有稀有气体元素原子的核外电子排布 |
| C.单核微粒的阴离子一定具有还原性、阳离子一定具有氧化性 |
| D.两粒子如果质子数及核外电子数均相同,则两者一定属于同种元素 |
您最近半年使用:0次
解题方法
4 . Ⅰ.  U是重要的核工业原料,在自然界的丰度很低。
U是重要的核工业原料,在自然界的丰度很低。 U的浓缩一直为国际社会关注。回答下列有关问题:
U的浓缩一直为国际社会关注。回答下列有关问题:
(1) U的中子数是
U的中子数是___ 。
(2) U、
U、 U、
U、 U互为同位素,下列对同位素的理解不正确的是
U互为同位素,下列对同位素的理解不正确的是___ (填序号,下同)。
A.元素符号相同 B.物理性质相同 C.化学性质基本相同 D.在周期表中位置相同
(3)下列有关 U说法不正确的是
U说法不正确的是___ 。
A. U原子核内中子数与质子数之差为51
U原子核内中子数与质子数之差为51
B. U与
U与 U的质子数、电子数都相等
U的质子数、电子数都相等
C. U与
U与 U是两种质子数相同,中子数不同的原子
U是两种质子数相同,中子数不同的原子
D. U与
U与 U是同种原子
U是同种原子
Ⅱ.锂的材料在社会生活中广泛应用,如亚氨基锂(Li2NH)是一种储氢容量高、安全性好的固体储氢材料,LiCoO2用作便携式电源的正极材料,碳酸锂(Li2CO3)广泛应用于陶瓷和医药等领域。根据下列要求回答相关问题:
(1)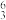 Li和
Li和 Li用作核反应堆最佳载热体,
Li用作核反应堆最佳载热体, LiH和
LiH和 LiD用作高温堆减速剂。下列说法中正确的是
LiD用作高温堆减速剂。下列说法中正确的是_______ (填序号,下同)。
A.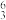 Li和
Li和 Li互为同位素 B
Li互为同位素 B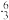 Li和
Li和 Li属于同种核素
Li属于同种核素
C. LiH和
LiH和 LiD的化学性质不同 D.
LiD的化学性质不同 D. LiH和
LiH和 LiD是同种物质
LiD是同种物质
(2)下列说法不正确的是_________ 。
A.碱性:Be(OH)2<LiOH<NaOH<KOH B.半径:K>Na>Li>Li+
C.氧化性:Li+<Na+<K+<Rb+<Cs+ D.金属性:Cs>Rb>K>Na>Li>Be
 U是重要的核工业原料,在自然界的丰度很低。
U是重要的核工业原料,在自然界的丰度很低。 U的浓缩一直为国际社会关注。回答下列有关问题:
U的浓缩一直为国际社会关注。回答下列有关问题:(1)
 U的中子数是
U的中子数是(2)
 U、
U、 U、
U、 U互为同位素,下列对同位素的理解不正确的是
U互为同位素,下列对同位素的理解不正确的是A.元素符号相同 B.物理性质相同 C.化学性质基本相同 D.在周期表中位置相同
(3)下列有关
 U说法不正确的是
U说法不正确的是A.
 U原子核内中子数与质子数之差为51
U原子核内中子数与质子数之差为51B.
 U与
U与 U的质子数、电子数都相等
U的质子数、电子数都相等C.
 U与
U与 U是两种质子数相同,中子数不同的原子
U是两种质子数相同,中子数不同的原子D.
 U与
U与 U是同种原子
U是同种原子Ⅱ.锂的材料在社会生活中广泛应用,如亚氨基锂(Li2NH)是一种储氢容量高、安全性好的固体储氢材料,LiCoO2用作便携式电源的正极材料,碳酸锂(Li2CO3)广泛应用于陶瓷和医药等领域。根据下列要求回答相关问题:
(1)
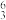 Li和
Li和 Li用作核反应堆最佳载热体,
Li用作核反应堆最佳载热体, LiH和
LiH和 LiD用作高温堆减速剂。下列说法中正确的是
LiD用作高温堆减速剂。下列说法中正确的是A.
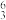 Li和
Li和 Li互为同位素 B
Li互为同位素 B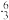 Li和
Li和 Li属于同种核素
Li属于同种核素C.
 LiH和
LiH和 LiD的化学性质不同 D.
LiD的化学性质不同 D. LiH和
LiH和 LiD是同种物质
LiD是同种物质(2)下列说法不正确的是
A.碱性:Be(OH)2<LiOH<NaOH<KOH B.半径:K>Na>Li>Li+
C.氧化性:Li+<Na+<K+<Rb+<Cs+ D.金属性:Cs>Rb>K>Na>Li>Be
您最近半年使用:0次
5 . I.  U是重要的核工业原料,在自然界的丰度很低。
U是重要的核工业原料,在自然界的丰度很低。 U的浓缩一直为国际社会关注。回答下列有关问题:
U的浓缩一直为国际社会关注。回答下列有关问题:
(1) U表示的含义是
U表示的含义是________________ 。
(2)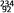 U、
U、 U、
U、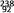 互为同位素,下列对同位素的理解不正确的是
互为同位素,下列对同位素的理解不正确的是________ (填序号,下同)。
A.元素符号相同 B.物理性质相同
C.化学性质基本相同 D.在周期表中位置相同
(3)下列有关 U说法不正确的是
U说法不正确的是________ 。
A. U原子核的中子数与质子数之差为51
U原子核的中子数与质子数之差为51
B. U与
U与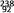 U的质子数、电子数都相等
U的质子数、电子数都相等
C. U与
U与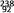 U是两种质子数相同,中子数不同的原子
U是两种质子数相同,中子数不同的原子
D. U与
U与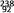 U是同种原子
U是同种原子
Ⅱ.锂的材料在社会生活中广泛应用,如亚氨基锂(Li2NH)是一种储氢容量高、安全性好的固体储氢材料,LiCoO2作便携式电源的正极材料,碳酸锂(Li2CO3)广泛应用于陶瓷和医药等领域。根据下列要求回答相关问题:
(1)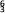 Li和
Li和 Li作核反应堆最佳载热体,
Li作核反应堆最佳载热体, LiH和
LiH和 LiD作高温堆减速剂。下列说法中 正确的是
LiD作高温堆减速剂。下列说法中 正确的是________ (填序号,下同)。
A.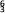 Li和
Li和 Li互为同位素 B.
Li互为同位素 B.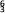 Li和
Li和 Li属于同种核素
Li属于同种核素
C. LiH和
LiH和 LiD的化学性质不同 D.
LiD的化学性质不同 D. LiH和
LiH和 LiD是同种物质
LiD是同种物质
(2)下列说法不正确的是________ 。
A.碱性:Be(OH)2<LiOH<NaOH<KOH B.半径:K>Na>Li>Li+
C.氧化性:Li+<Na+<K+<Rb+<Cs+ D.金属性:Cs>Rb>K>Na>Li>Be
(3)锂是碱金属族首元素,其性质明显不同于其他碱金属性质,下列能支持这一观点的性质是________ 。
A.碱金属与水反应 B.碱金属在氧气中燃烧
C.碱金属与氢气反应 D.碱金属与氯气反应
 U是重要的核工业原料,在自然界的丰度很低。
U是重要的核工业原料,在自然界的丰度很低。 U的浓缩一直为国际社会关注。回答下列有关问题:
U的浓缩一直为国际社会关注。回答下列有关问题:(1)
 U表示的含义是
U表示的含义是(2)
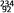 U、
U、 U、
U、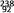 互为同位素,下列对同位素的理解不正确的是
互为同位素,下列对同位素的理解不正确的是A.元素符号相同 B.物理性质相同
C.化学性质基本相同 D.在周期表中位置相同
(3)下列有关
 U说法不正确的是
U说法不正确的是A.
 U原子核的中子数与质子数之差为51
U原子核的中子数与质子数之差为51 B.
 U与
U与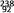 U的质子数、电子数都相等
U的质子数、电子数都相等C.
 U与
U与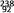 U是两种质子数相同,中子数不同的原子
U是两种质子数相同,中子数不同的原子 D.
 U与
U与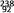 U是同种原子
U是同种原子Ⅱ.锂的材料在社会生活中广泛应用,如亚氨基锂(Li2NH)是一种储氢容量高、安全性好的固体储氢材料,LiCoO2作便携式电源的正极材料,碳酸锂(Li2CO3)广泛应用于陶瓷和医药等领域。根据下列要求回答相关问题:
(1)
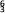 Li和
Li和 Li作核反应堆最佳载热体,
Li作核反应堆最佳载热体, LiH和
LiH和 LiD作高温堆减速剂。下列说法中 正确的是
LiD作高温堆减速剂。下列说法中 正确的是A.
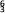 Li和
Li和 Li互为同位素 B.
Li互为同位素 B.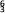 Li和
Li和 Li属于同种核素
Li属于同种核素C.
 LiH和
LiH和 LiD的化学性质不同 D.
LiD的化学性质不同 D. LiH和
LiH和 LiD是同种物质
LiD是同种物质(2)下列说法不正确的是
A.碱性:Be(OH)2<LiOH<NaOH<KOH B.半径:K>Na>Li>Li+
C.氧化性:Li+<Na+<K+<Rb+<Cs+ D.金属性:Cs>Rb>K>Na>Li>Be
(3)锂是碱金属族首元素,其性质明显不同于其他碱金属性质,下列能支持这一观点的性质是
A.碱金属与水反应 B.碱金属在氧气中燃烧
C.碱金属与氢气反应 D.碱金属与氯气反应
您最近半年使用:0次
名校
解题方法
6 . 已知 ,其中元素X、Y均为第二周期元素,其原子的最外层电子数之和为11。下列叙述正确的是
,其中元素X、Y均为第二周期元素,其原子的最外层电子数之和为11。下列叙述正确的是
 ,其中元素X、Y均为第二周期元素,其原子的最外层电子数之和为11。下列叙述正确的是
,其中元素X、Y均为第二周期元素,其原子的最外层电子数之和为11。下列叙述正确的是| A.Y原子核内中子数为9 | B.X单质常温下是液态 |
| C.H2Y2溶液只有强氧化性 | D. 与 与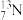 互为同素异形体 互为同素异形体 |
您最近半年使用:0次
7 . 物质结构决定物质性质。已知氢元素原子的核电荷数为1。试分析:
(1) 是一种离子化合物,应读作
是一种离子化合物,应读作_______ 。它与盐酸反应生成一种盐和一种可燃性气体,其化学方程式为_______ 。已知反应物中具有氧化性的物质,发生还原反应后,元素化合价降低。请判断上述反应中,反应物_______ (填化学式)具有氧化性。
(2)氢原子可以和很多原子组成10电子或18电子的微粒。请写出氢原子与其他一种原子形成的五核(五个原子)10电子微粒且带正荷的化学式:_______ ;也请写出氢原子与其他一种原子形成的六核(六个原子)18电子微粒的分子式:_______ 。
(1)
 是一种离子化合物,应读作
是一种离子化合物,应读作(2)氢原子可以和很多原子组成10电子或18电子的微粒。请写出氢原子与其他一种原子形成的五核(五个原子)10电子微粒且带正荷的化学式:
您最近半年使用:0次
解题方法
8 . 有A、B、C、D、E5种短周期元素,A与B可形成BA型化合物,A元素的单质常用于自来水消毒;金属B的原子核内质子数比它前一周期同主族元素原子的质子数多8;C元素有3种同位素C1、C2、C3,自然界里含量最多的是C1,C3原子的质量数是C1的3倍,C2原子的质量数是C1的2倍;D的气态氢化物的水溶液呈碱性,而其最高价氧化物对应的水化物为强酸;E元素原子的最外层电子数比次外层电子数多4。
(1)写出下列元素的元素名称:A_________ ,B_________ 。
(2)写出C1、C3两种原子的符号:C1____________ ,C3___________ 。
(3)A、B、E形成的一种化合物是某种家用消毒液的有效成分,其电子式是___________ 。
(4)D的最高价氧化物的水化物与其氢化物反应形成化合物的化学式是___________ ,其所含化学键的类型是____________ ,由最常见的E原子与C2原子形成的最简单分子0.5mol中,所含中子的数目是___________ 。
(5)C、E的单质在碱性(KOH溶液)条件下可设计成一种燃料电池,其正极的电极反应式为_________ 。
(1)写出下列元素的元素名称:A
(2)写出C1、C3两种原子的符号:C1
(3)A、B、E形成的一种化合物是某种家用消毒液的有效成分,其电子式是
(4)D的最高价氧化物的水化物与其氢化物反应形成化合物的化学式是
(5)C、E的单质在碱性(KOH溶液)条件下可设计成一种燃料电池,其正极的电极反应式为
您最近半年使用:0次
解题方法
9 . 已知次氯酸具有强氧化性,可将S2﹣氧化,其反应为HClO+S2﹣+H+=Cl﹣+S↓+H2O。下列表示相关微粒的化学用语不正确的是
| A.中子数为18的氯原子:35Cl | B.H2O的电子式:H:O:H |
| C.HClO的结构式:H﹣O﹣Cl | D.S2﹣的结构示意图: |
您最近半年使用:0次
10 . 下列说法不正确的是
| A.126C、136C、146C为碳元素的三种核素.元素周期表中碳的相对原子质量为12.01,说明自然界中的碳主要以126C的核素形式存在 |
| B.汽车尾气催化转化装置可将尾气中的NO和CO等有害气体转化为N2和CO2 , 该装置中的催化剂可降低NO和CO反应的活化能,加快该反应的速率,却不能提高该反应的平衡转化率 |
| C.人们通常用标准燃烧热或热值来衡量燃料燃烧放出热量的大小,某物质的热值越高则其标准燃烧热越大 |
| D.绿色荧光蛋白在研究癌症发病机制的过程中应用突出,但其在酸性或碱性条件下可能会失去发光功能 |
您最近半年使用:0次



