名校
1 . 下列说法正确的是
A.HCl属于共价化合物,溶于水能电离出 和 和 |
| B.NaOH是离子化合物,该物质中只含离子键 |
| C.HI气体受热分解的过程中,只需克服分子间作用力 |
| D.炭黑具有各向异性,碳原子在三维空间里呈周期性有序排列 |
您最近一年使用:0次
名校
解题方法
2 . 卤化钠(NaX)和四卤化钛(TiX4)的熔点如图所示。下列判断不正确的是
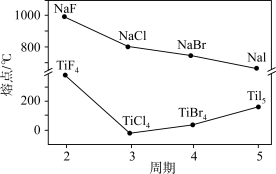
| A.NaX随X-半径增大,离子键减弱 |
| B.四氯化钛中存在共价键和分子间作用力 |
| C.TiF4的熔点反常升高是由于氢键的作用 |
| D.由图可看出F的电负性强于Cl、Br、I |
您最近一年使用:0次
名校
解题方法
3 . 乙烯催化氧化的过程如下图(部分相关离子未画出),下列描述不正确的是
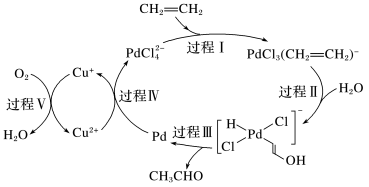
| A.该转化过程中Pd的价态发生了变化 |
| B.该转化过程中,有非极性键的断裂与极性键的形成 |
| C.Cu+为该反应的催化剂 |
D.乙烯催化氧化反应的化学方程式为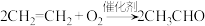 |
您最近一年使用:0次
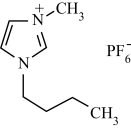
4 . 离子液体是指由体积较大的阴、阳离子组成,并且在室温或接近室温下呈液态的盐,也称为低温熔融盐。有许多优点,例如难挥发,有良好的导电性,可作溶剂、电解质、催化剂等。1-正丁基-3-甲基咪唑六氟磷酸盐是一种离子液体,结构简式如图,下列关于它的叙述正确的是
 或
或
A.该新型化合物含有的C、N、P元素均为 杂化 杂化 |
| B.1-正丁基-3-甲基咪唑六氟磷酸盐属于含共价键的离子化合物 |
| C.电负性:F>N>H>C |
| D.该新型化合物的组成元素全部位于元素周期表p区 |
您最近一年使用:0次
名校
解题方法
5 . 下列关于晶体的说法不正确的是
①含有离子的晶体一定是离子晶体
②分子晶体若采取面心密堆积方式,其配位数是12
③含有共价键的晶体一定是共价晶体
④分子晶体的熔点一定比金属晶体的低
⑤MgO远比NaCl的熔点高
⑥共价键的强弱决定分子晶体熔、沸点的高低
①含有离子的晶体一定是离子晶体
②分子晶体若采取面心密堆积方式,其配位数是12
③含有共价键的晶体一定是共价晶体
④分子晶体的熔点一定比金属晶体的低
⑤MgO远比NaCl的熔点高
⑥共价键的强弱决定分子晶体熔、沸点的高低
| A.①③④⑥ | B.①②③⑤ | C.①②④ | D.②③④⑥ |
您最近一年使用:0次
名校
6 . X、Y、Z、W、R为原子序数依次增大的短周期主族元素。X、Z原子中分别有1个、7个运动状态完全不同的电子,Y原子中3个能级中的电子数相等,W原子最外层电子数是内层的3倍,R的原子半径是该周期主族元素中最大的。下列说法正确的是
A.简单离子半径: | B.最高价含氧酸的酸性: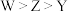 |
C.得电子能力: | D.X、Z、W形成的化合物一定不含离子键 |
您最近一年使用:0次
名校
解题方法
7 . 下列化学用语表示不正确的是
A. 的电子式: 的电子式: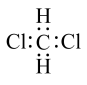 |
B. 杂化轨道模型: 杂化轨道模型: |
C.水合氢离子结构式: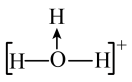 |
D.用原子轨道描述HCl分子中化学键的形成: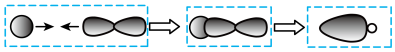 |
您最近一年使用:0次
解题方法
8 . 现代无机化学对硫﹣氮化合物的研究是最为活跃的领域之一、其中如图是已经合成的最著名的硫—氮化合物的分子结构。下列说法正确的是
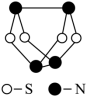
| A.该物质的分子式为SN | B.该物质的分子中只含极性键 |
| C.该物质的分子是极性分子 | D.N原子sp2杂化 |
您最近一年使用:0次
名校
解题方法
9 . 下列有关化学键的说法正确的是
| A.HCl和NaOH化学键类型都相同 | B.CaCl2中既有离子键又有共价键 |
| C.CH3COONa中含有极性键、非极性键和离子键 | D.H2O、HF、NH3中的共价键极性由强到弱 |
您最近一年使用:0次
名校
解题方法
10 . 下列叙述正确的是
| A.以极性键结合的分子,一定是极性分子 |
| B.由非金属元素组成的化合物不一定是共价化合物 |
| C.非极性分子中,各原子间都应以非极性键结合 |
| D.不同元素组成的多原子分子里的化学键一定都是极性键 |
您最近一年使用:0次



