名校
1 . 利用“价类二维图”研究物质的性质是化学研究的重要手段。如图是氯元素的化合价与部分物质类别的对应关系。下列说法正确的是


| A.D中含有的化学键类型只有离子键 |
| B.将E溶液滴入碳酸氢钠溶液中,有大量气泡产生 |
| C.A、B、C均属于电解质 |
| D.C的酸性和氧化性均强于E |
您最近一年使用:0次
名校
解题方法
2 . 回答下列问题
(1)肼(N2H4)分子可视为NH3分子中的一个氢原子被-NH2取代形成的另一种氮的氢化物。
① NH3分子的空间结构是_______ ;N2H4分子中氮原子轨道的杂化类型是 _______ 。
② 肼可用作火箭燃料,燃烧时发生的反应是N2O4(l) + 2N2H4(l)=3N2(g) + 4H2O(g) ΔH= -1038.7 kJ·mol-1,若该反应中有4 mol N-H断裂,则形成的 π 键有_______ mol。
③ 肼能与硫酸反应生成N2H6SO4,N2H6SO4与硫酸铵化合物类型相同,则N2H6SO4晶体不存在_______ (填标号)。
a. 离子键 b. 共价键 c. 范德华力
(2)第ⅥA族元素氧、硫、硒(Se)的化合物在研究和生产中有许多重要用途。请回答下列问题:
① H2Se的还原性比H2S_______ (填“强”或“弱”)。气态SeO3分子的空间结构为_______ ,SO2的VSEPR模型为_______ ,空间结构为_______ 。
② H2O内的O-H、水分子间的范德华力和氢键,从强到弱依次为_______ ,H+可与H2O形成H3O+,H3O+中O采用_______ 杂化,H3O+中H-O-H键角比H2O中的_______ (填“大”或“小”)
(1)肼(N2H4)分子可视为NH3分子中的一个氢原子被-NH2取代形成的另一种氮的氢化物。
① NH3分子的空间结构是
② 肼可用作火箭燃料,燃烧时发生的反应是N2O4(l) + 2N2H4(l)=3N2(g) + 4H2O(g) ΔH= -1038.7 kJ·mol-1,若该反应中有4 mol N-H断裂,则形成的 π 键有
③ 肼能与硫酸反应生成N2H6SO4,N2H6SO4与硫酸铵化合物类型相同,则N2H6SO4晶体不存在
a. 离子键 b. 共价键 c. 范德华力
(2)第ⅥA族元素氧、硫、硒(Se)的化合物在研究和生产中有许多重要用途。请回答下列问题:
① H2Se的还原性比H2S
② H2O内的O-H、水分子间的范德华力和氢键,从强到弱依次为
您最近一年使用:0次
2022-07-30更新
|
338次组卷
|
2卷引用:天津市第三中学2021-2022学年高二下学期期末质量检测化学试题
解题方法
3 . 氯及其化合物在生产生活中有着重要用途。请回答下列问题:
(1)下列与氯元素同一主族的元素是____ 。
a.Br b.Sr c.F d.B
(2)下列含氯物质:①CCl4②Cl2③CaCl2④NaClO⑤HClO4⑥NH4Cl⑦HCl,其中只含有离子键的是_____ (填序号);只含有共价键的是____ (填序号);属于强电解质的是____ (填序号)。
(3)将氯气通入到NaBr溶液中,发生反应的离子方程式为____ 。
(4)亚硝酸钠与氯化铵共热能发生反应,其化学方程式为:NaNO2+NH4Cl NaCl+X↑+2H2O,则X的化学式为
NaCl+X↑+2H2O,则X的化学式为____ 。该化学方程式里的含氮物质中,氮元素未表现出的化合价为____ 价(填序号)。
A.+3 B.-3 C.0 D.+5
(1)下列与氯元素同一主族的元素是
a.Br b.Sr c.F d.B
(2)下列含氯物质:①CCl4②Cl2③CaCl2④NaClO⑤HClO4⑥NH4Cl⑦HCl,其中只含有离子键的是
(3)将氯气通入到NaBr溶液中,发生反应的离子方程式为
(4)亚硝酸钠与氯化铵共热能发生反应,其化学方程式为:NaNO2+NH4Cl
 NaCl+X↑+2H2O,则X的化学式为
NaCl+X↑+2H2O,则X的化学式为A.+3 B.-3 C.0 D.+5
您最近一年使用:0次
名校
解题方法
4 . 下列叙述正确的组合是
①在空气中长时间放置少量金属钠,最终的产物是Na2CO3
②人们使用次氯酸盐代替氯水作为漂白剂,因为次氯酸盐的漂白性更强
③根据是否有丁达尔现象将分散系分为溶液、胶体和浊液
④在生产、生活中,铝合金是用量最大、用途最广的合金材料
⑤H2O的沸点比H2S的沸点高是因为H2O的分子间存在氢键
⑥由非金属元素形成的化合物一定是共价化合物
①在空气中长时间放置少量金属钠,最终的产物是Na2CO3
②人们使用次氯酸盐代替氯水作为漂白剂,因为次氯酸盐的漂白性更强
③根据是否有丁达尔现象将分散系分为溶液、胶体和浊液
④在生产、生活中,铝合金是用量最大、用途最广的合金材料
⑤H2O的沸点比H2S的沸点高是因为H2O的分子间存在氢键
⑥由非金属元素形成的化合物一定是共价化合物
| A.①⑤ | B.②③ | C.⑤⑥ | D.②④ |
您最近一年使用:0次
2021-02-02更新
|
296次组卷
|
4卷引用:湖北省沙市中学2020-2021学年高一上学期期末考试化学试题
名校
解题方法
5 . 下图是元素周期表的一部分:
Ⅰ.用化学用语 回答下列问题:
(1)①、②、⑥形成的化合物中存在的化学键类型有________ 。
(2)④、⑦、⑧的最高价含氧酸的酸性由强到弱的顺序是_______ 。
(3)写出②的离子结构示意图为__________ 。
(4)Y由②⑥⑧三种元素组成,它的水溶液是生活中常见的消毒剂。Y的水溶液与洁厕灵混合使用会产生一种有毒气体,该反应的离子方程式为_______ 。
Ⅱ.A、B、C、D都是中学化学中常见的物质,其中A、B、C均含有同一种元素,在一定条件下相互转化关系如下(部分反应中的水已略去)。根据题意回答下列问题:
(1)若A是一种金属单质,C是淡黄色固体,写出C的一种用途_____ ;
(2)若A、B、C均为化合物且含有同一种金属元素,D是会造成温室效应的一种气体,请写出D的电子式_____ ,A和C反应的离子方程式 ___ 。
(3)若D是一种常见的过渡金属单质,原子核内有26个质子,向C的水溶液中滴加AgNO3溶液,产生不溶于稀HNO3的白色沉淀,检验此C溶液中金属离子的方法是________ ;又知在酸性溶液中该金属离子能被双氧水氧化,写出该反应的离子方程式_________ 。
| ① | |||||||||||||||||
| ④ | ⑤ | ⑥ | |||||||||||||||
| ② | ③ | ⑦ | ⑧ | ||||||||||||||
| Fe | |||||||||||||||||
(1)①、②、⑥形成的化合物中存在的化学键类型有
(2)④、⑦、⑧的最高价含氧酸的酸性由强到弱的顺序是
(3)写出②的离子结构示意图为
(4)Y由②⑥⑧三种元素组成,它的水溶液是生活中常见的消毒剂。Y的水溶液与洁厕灵混合使用会产生一种有毒气体,该反应的离子方程式为
Ⅱ.A、B、C、D都是中学化学中常见的物质,其中A、B、C均含有同一种元素,在一定条件下相互转化关系如下(部分反应中的水已略去)。根据题意回答下列问题:
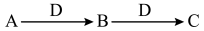
(1)若A是一种金属单质,C是淡黄色固体,写出C的一种用途
(2)若A、B、C均为化合物且含有同一种金属元素,D是会造成温室效应的一种气体,请写出D的电子式
(3)若D是一种常见的过渡金属单质,原子核内有26个质子,向C的水溶液中滴加AgNO3溶液,产生不溶于稀HNO3的白色沉淀,检验此C溶液中金属离子的方法是
您最近一年使用:0次



