名校
解题方法
1 . 含氯化合物有广泛的应用。
I.
(1)氯原子的核外有___________ 种能量不同的电子,氯化铵的电子式为___________ 。
(2)周期表中有3种主族元素与氯元素相邻,它们的气态氢化物的热稳定性由强至弱的顺序为___________ (用分子式表示)。通常状况下,Cl2、Br2、I2依次是气体、液体、固体,从结构的角度分析其原因:___________ 。
Ⅱ.ClO2是一种高效消毒剂,用KClO3和浓HCl可制得它:
(3)请完成该制备反应的化学方程式___________ 。
_______KClO3+____HCl(浓)=_____Cl2↑+_____ClO2↑+_____KCl+______。
若反应产生8.96LClO2(标准状况)时,则转移电子数为___________ 。
(4)Ca(ClO)2是漂白粉的有效成分,Ca(ClO)2中存在的化学键为___________ 。工业制漂白粉的气体原料来自于氯碱工业电解饱和食盐水设备的___________ (填电极名称)。
I.
(1)氯原子的核外有
(2)周期表中有3种主族元素与氯元素相邻,它们的气态氢化物的热稳定性由强至弱的顺序为
Ⅱ.ClO2是一种高效消毒剂,用KClO3和浓HCl可制得它:
(3)请完成该制备反应的化学方程式
_______KClO3+____HCl(浓)=_____Cl2↑+_____ClO2↑+_____KCl+______。
若反应产生8.96LClO2(标准状况)时,则转移电子数为
(4)Ca(ClO)2是漂白粉的有效成分,Ca(ClO)2中存在的化学键为
您最近一年使用:0次
2023-04-07更新
|
332次组卷
|
2卷引用:上海市奉贤区2022-2023学年高三下学期二模考试化学试题
2 . 车辆碰撞瞬间,安全装置通电点火,使其中的粉末分解释放出大量保护气形成安全气囊。经分析确定气囊中粉末含有Na、Al、N、O四种元素,叠氮化钠(NaN3)经碰撞后会分解为Na、N2。
(1)氮原子的最外层电子排布式是______ ,氧原子核外有______ 种能量不同的电子,叠氮化钠固体中阴阳离子的个数比为1:1,则该固体中含有的化学键是______ (填化学键名称)。
(2)在酸性溶液中,Al的最高价氧化物对应水化物的电离方程式为______ 。
(3)氮和氧两种元素,非金属性较强的是______ ,请用一个事实说明其强弱______ 。
工业上,通过如下转化可制得KClO3晶体:NaCl溶液 NaClO3溶液
NaClO3溶液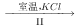 KClO3晶体
KClO3晶体
(4)①配平并完成Ⅰ中反应的总化学方程式,并用单线桥标出电子转移的方向和数目:______ NaCl+______ H2O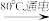
______ NaClO3 +______
②Ⅱ反应过程能析出KClO3晶体而无其它晶体析出的原因是______ 。
(1)氮原子的最外层电子排布式是
(2)在酸性溶液中,Al的最高价氧化物对应水化物的电离方程式为
(3)氮和氧两种元素,非金属性较强的是
工业上,通过如下转化可制得KClO3晶体:NaCl溶液
 NaClO3溶液
NaClO3溶液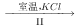 KClO3晶体
KClO3晶体(4)①配平并完成Ⅰ中反应的总化学方程式,并用单线桥标出电子转移的方向和数目:
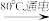
②Ⅱ反应过程能析出KClO3晶体而无其它晶体析出的原因是
您最近一年使用:0次
解题方法
3 . 生活污水中氮是造成水体富营养化的主要原因。
完成下列填空:
(1)某污水中存在NH4Cl。写出NH4Cl的电子式_______ 。该污水呈现酸性的原因_____________ (结合离子方程式及相关文字说明)。
(2)向饱和NH4Cl溶液中加入或通入一种物质,可以使NH4Cl结晶析出,这种物质可以是___________ (任写-种),理由是_______________________________ 。
(3)某污水中同时存在NH4+和NO3-时,可用下列方法除去:先利用O2将NH4+氧化成NO3-。请配平下列离子方程式并标出电子转移的方向和数目。___ NH4++___ O2→___ NO3-+___ H2O+___ H+,再将NO3-还原成N2,反应的离子方程式:2NO3-+5H2  N2+2 O H-+4H2O
N2+2 O H-+4H2O
①NH4NO3晶体中所含化学键为___________ 。
② 若该污水中含有1mol NH4NO3,用以上方法处理完全后,共消耗_______ mol氢气。
③ 该污水处理方法的好处是___________________________________________ 。
完成下列填空:
(1)某污水中存在NH4Cl。写出NH4Cl的电子式
(2)向饱和NH4Cl溶液中加入或通入一种物质,可以使NH4Cl结晶析出,这种物质可以是
(3)某污水中同时存在NH4+和NO3-时,可用下列方法除去:先利用O2将NH4+氧化成NO3-。请配平下列离子方程式并标出电子转移的方向和数目。
 N2+2 O H-+4H2O
N2+2 O H-+4H2O①NH4NO3晶体中所含化学键为
② 若该污水中含有1mol NH4NO3,用以上方法处理完全后,共消耗
③ 该污水处理方法的好处是
您最近一年使用:0次



