1 . 如图是s轨道和p轨道的原子轨道图,试回答问题:
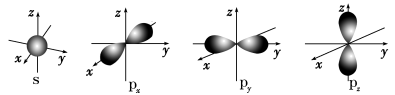
(1)s电子的原子轨道呈_______ 形,每个s轨道有_______ 个原子轨道;p电子的原子轨道呈_______ 形,每个p轨道有_______ 个原子轨道。
(2)元素X的原子最外层电子排布式为nsnnpn+1,原子中能量最高的是_______ 电子,其电子云在空间有_______ 个伸展方向;元素X的名称是_______ ,它的氢化物的化学式是_______ 。若元素X的原子最外层电子排布式为nsn−1npn+1,那么X的元素符号应为_______ ,原子的轨道表示式为_______ 。

(1)s电子的原子轨道呈
(2)元素X的原子最外层电子排布式为nsnnpn+1,原子中能量最高的是
您最近一年使用:0次
2022-12-12更新
|
254次组卷
|
2卷引用:河北省保定市崇德实验中学2020-2021学年度高二下学期期中考试化学试题
2 . 根据物质结构有关性质和特点,回答下列问题:
(1)钴位于元素周期表的___________ 。
(2)基态铝原子核外电子云轮廓图的形状有(填名称)___________ 。
(3)2020年新冠肺炎疫情席卷全球,酒精(CH3CH2OH)成为家庭必备品,乙醇分子中碳原子轨道的杂化类型是___________ 。
(4)[Fe(H2NCONH2)]6(NO3)3的名称是三硝酸六尿素合铁(III),是一种重要的配合物。该化合物中,所含非金属元素C的最高价氧化物的电子式为___________ ;Fe3+比Fe2+更稳定的原因___________ 。
(5)Co(NH3)5BrSO4可形成两种钴的配合物,结构分别为[Co(NH3)5Br]SO4和[Co(SO4)(NH3)5]Br。已知Co3+的配位数为6,为确定钴的配合物的结构,现对两种配合物进行如下实验:在第一种配合物溶液中加入硝酸银溶液产生白色沉淀,在第二种配合物溶液中加入硝酸银溶液产生淡黄色沉淀。则第二种配合物的配体为___________ 。
(6)高温超导材料镧钡铜氧化物中含有Cu3+。基态时Cu3+的电子排布式为___________ ;
(1)钴位于元素周期表的
(2)基态铝原子核外电子云轮廓图的形状有(填名称)
(3)2020年新冠肺炎疫情席卷全球,酒精(CH3CH2OH)成为家庭必备品,乙醇分子中碳原子轨道的杂化类型是
(4)[Fe(H2NCONH2)]6(NO3)3的名称是三硝酸六尿素合铁(III),是一种重要的配合物。该化合物中,所含非金属元素C的最高价氧化物的电子式为
(5)Co(NH3)5BrSO4可形成两种钴的配合物,结构分别为[Co(NH3)5Br]SO4和[Co(SO4)(NH3)5]Br。已知Co3+的配位数为6,为确定钴的配合物的结构,现对两种配合物进行如下实验:在第一种配合物溶液中加入硝酸银溶液产生白色沉淀,在第二种配合物溶液中加入硝酸银溶液产生淡黄色沉淀。则第二种配合物的配体为
(6)高温超导材料镧钡铜氧化物中含有Cu3+。基态时Cu3+的电子排布式为
您最近一年使用:0次
21-22高二·全国·课时练习
解题方法
3 . 回答下列问题:
(1)处于一定空间运动状态的电子在原子核外出现的概率密度分布可用_______ 形象化描述。在基态14C原子中,核外存在_______ 对自旋相反的电子。
(2)N的基态原子核外电子排布式为_______ ;Cu的基态原子最外层有_______ 个电子。
(3)钒(23V)是元素广泛用于催化及钢铁工业。钒在元素周期表中的位置为_______ ,其价层电子的轨道表示式为_______ 。
(4)Na位于元素周期表第_______ 周期第_______ 族;S的基态原子核外有_______ 个未成对电子;Si的基态原子核外电子排布式为_______ 。
(5)Cu+基态核外电子排布式为_______ 。
(6)基态Fe原子有_______ 个未成对电子,Fe3+的电子排布式为_______ 。
(7)31Ga基态原子的核外电子排布式是_______ 。
(8)铝原子核外电子云有_______ 种不同的伸展方向,有_______ 种不同运动状态的电子。
(9)基态Mn2+的核外电子排布式为_______ 。
(10)Se原子序数为_______ ,其核外M层电子的排布式为_______ 。
(11)可正确表示原子轨道的是_______。
(1)处于一定空间运动状态的电子在原子核外出现的概率密度分布可用
(2)N的基态原子核外电子排布式为
(3)钒(23V)是元素广泛用于催化及钢铁工业。钒在元素周期表中的位置为
(4)Na位于元素周期表第
(5)Cu+基态核外电子排布式为
(6)基态Fe原子有
(7)31Ga基态原子的核外电子排布式是
(8)铝原子核外电子云有
(9)基态Mn2+的核外电子排布式为
(10)Se原子序数为
(11)可正确表示原子轨道的是_______。
| A.2s | B.2d | C.3pz | D.3f |
您最近一年使用:0次
4 . 回答下列问题:
(1)1861年德国人基尔霍夫(r. Kirchhoff)和本生(R.w. Bunsen)研究锂云母的某谱时,发现在深红区有一新线,从而发现了铷元素,他们研究的是_______
(2)含有钾元素的盐的焰色试验为_______ 色。许多金属盐都可以发生焰色试验,其原因是_______
(1)1861年德国人基尔霍夫(r. Kirchhoff)和本生(R.w. Bunsen)研究锂云母的某谱时,发现在深红区有一新线,从而发现了铷元素,他们研究的是
(2)含有钾元素的盐的焰色试验为
您最近一年使用:0次
名校
5 . 回答下列问题:
(1)分子(CN)2中键与键之间的夹角为180°,并有对称性,分子中每个原子最外层均满足8电子稳定结构,其结构式为___ ,(CN)2称为“拟卤素”,具有类似Cl2的化学性质,则(CN)2与NaOH水溶液反应的化学方程式为___ 。
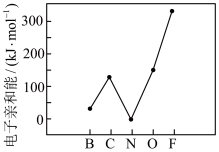
(2)元素的基态气态原子得到一个电子形成气态负一价离子时所放出的能量称作第一电子亲和能(E1)。第二周期部分元素的E1变化趋势如图所示,氮元素的E1呈现异常的原因是___ 。
(3)基态As原子中,核外电子占据最高能层的符号是___ ,占据该能层电子的电子云轮廓图形状为___ 。
(1)分子(CN)2中键与键之间的夹角为180°,并有对称性,分子中每个原子最外层均满足8电子稳定结构,其结构式为
(2)元素的基态气态原子得到一个电子形成气态负一价离子时所放出的能量称作第一电子亲和能(E1)。第二周期部分元素的E1变化趋势如图所示,氮元素的E1呈现异常的原因是

(3)基态As原子中,核外电子占据最高能层的符号是
您最近一年使用:0次
2021高三·全国·专题练习
解题方法
6 . 碳及其化合物广泛存在于自然界中,回答下列问题:
(1)处于一定空间运动状态的电子在原子核外出现的概率密度分布可用___________ 形象化描述。在基态原子中,核外存在___________ 对自旋相反的电子。
(2)碳在形成化合物时,其键型以共价键为主,原因是___________ 。
(1)处于一定空间运动状态的电子在原子核外出现的概率密度分布可用
(2)碳在形成化合物时,其键型以共价键为主,原因是
您最近一年使用:0次
名校
7 . 铅的合金可作轴承、电缆外皮之用,还可做体育器材铅球等。铅元素位于元素周期表第六周期IVA,IVA中原子序数最小的元素的原子有___ 种能量不同的电子,其次外层的电子云有___ 种不同的伸展方向。与铅同主族的短周期元素中,其最高价氧化物对应水化物酸性最强的是___ (填化学式),气态氢化物沸点最低的是___ (填化学式)。
您最近一年使用:0次
名校
解题方法
8 . I.2020年12月17日,我国“嫦娥五号”返回器携月壤成功着陆。研究发现,月壤中存在天然的铁、金、银、铅、锌、铜、锑、铼等矿物颗粒。
(1) 写出铜的基态原子的电子排布式:___________ 。
(2) 第四周期的元素原子中最外层电子数与铜原子的相同的元素有___________ (填元素符号)。
(3)Fe在周期表中位于___________ 周期___________ 族,属于___________ 区。
II.(1)s电子的原子轨道呈___________ 形,每个s能级有___________ 个原子轨道;p电子的原子轨道呈___________ 形,每个p能级有___________ 个原子轨道。
(2) 基态铝原子核外共有___________ 种不同能级的电子,有___________ 种不同运动状态的电子。
(1) 写出铜的基态原子的电子排布式:
(2) 第四周期的元素原子中最外层电子数与铜原子的相同的元素有
(3)Fe在周期表中位于
II.(1)s电子的原子轨道呈
(2) 基态铝原子核外共有
您最近一年使用:0次
9 . 处于一定空间运动状态的电子在原子核外出现的概率分布可用_______ 形象化描述;在基态 原子中,最高电子层的原子轨道有
原子中,最高电子层的原子轨道有_______ 个。
 原子中,最高电子层的原子轨道有
原子中,最高电子层的原子轨道有
您最近一年使用:0次
2021-02-21更新
|
150次组卷
|
2卷引用:高二选择性必修2(人教版2019)第一章 原子结构与性质 第一节 原子结构 课时2 构造原理与电子排布式 电子云与原子轨道
10 . (1)K层有___ 个能级,用符号表示为____ ;L层有___ 个能级,用符号分别表示为___ ;M层有__ 个能级,用符号分别表示为___ 。由此可推知,n电子层最多可能有___ 个能级,能量最低的两个能级的符号分别表示为___ 、___ ,它们的电子云轮廓图形状分别为___ 、___ 。
(2)比较下列多电子的原子轨道的能量高低(填“>”“<”或“=”)。
①2s___ 3s
②2s___ 3d
③2px___ 2py
④4f___ 6f
(2)比较下列多电子的原子轨道的能量高低(填“>”“<”或“=”)。
①2s
②2s
③2px
④4f
您最近一年使用:0次



