名校
1 . 第n电子层,其作为原子的最外层容纳的电子数最多与( )层的相同;当它作为次外层,其容纳的电子数比(
)层的相同;当它作为次外层,其容纳的电子数比( )层上电子数最多能多10个,第n层为
)层上电子数最多能多10个,第n层为
 )层的相同;当它作为次外层,其容纳的电子数比(
)层的相同;当它作为次外层,其容纳的电子数比( )层上电子数最多能多10个,第n层为
)层上电子数最多能多10个,第n层为| A.K层 | B.L层 | C.M层 | D.N层 |
您最近半年使用:0次
名校
解题方法
2 . 可容纳电子数目最多的能级(亚层)是
| A.3s | B.4f | C.2p | D.5d |
您最近半年使用:0次
3 . 总结:
(1)原子核外电子总是先排能力_______ 的电子层,然后有里向外,依次排布即排满了_______ 层才能排L层,排满了_______ 层才能排M层。
(2)原子核外每个电子层最多容纳_______ 个电子(n为电子层序数)
(3)原子最外层电子数不超过_______ 个电子(K层为最外层时,不超过_______ 个电子)。
(4)原子次外层电子数不超过_______ 个电子。
(5)倒数第三层不超过_______ 个电子
(1)原子核外电子总是先排能力
(2)原子核外每个电子层最多容纳
(3)原子最外层电子数不超过
(4)原子次外层电子数不超过
(5)倒数第三层不超过
您最近半年使用:0次
解题方法
4 . 明确宏观现象的微观本质是学习化学的重要思想方法。
(1)如图1是钾原子和硫原子的结构示意图,请回答:___________ 。
②钾原子在化学反应中易___________ 电子(填“得到”或“失去”)。
③钾素和硫元素形成的化合物硫化钾的化学式是___________ 。
(2)图2是硫酸铜溶液与锌粒反应前后溶液中主要离子变化示意图。_______
②反应中过量的物质是________ (写化学式)。
③该反应的化学方程式为_______ ,反应现象为_______
(1)如图1是钾原子和硫原子的结构示意图,请回答:

②钾原子在化学反应中易
③钾素和硫元素形成的化合物硫化钾的化学式是
(2)图2是硫酸铜溶液与锌粒反应前后溶液中主要离子变化示意图。
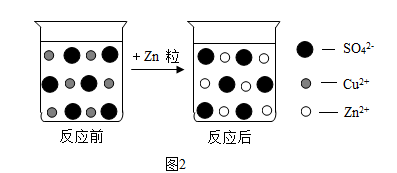
②反应中过量的物质是
③该反应的化学方程式为
您最近半年使用:0次
2021-10-22更新
|
153次组卷
|
2卷引用:新疆柯坪县柯坪湖州国庆中学2021-2022学年高一上学期开学考试理综化学试题
名校
解题方法
5 . 原子结构与元素周期表存在着内在联系。根据已学知识,请你回答下列问题:
(1)指出31号元素镓(Ga)在元素周期表中的位置:___ 。
(2)写出原子序数最小的第Ⅷ族元素原子的核外的价电子排布图:____ 。其正三价离子的未成对电子数为____
(3)写出3p轨道上有2个未成对电子的元素的符号:____ 。
(4)日常生活中广泛使用的不锈钢,在其生产过程中添加了某种元素,该元素的价电子排布式为3d54s1,该元素的名称为___ 。
(5)基态原子的4s能级中只有1个电子的元素共有___ 种
(6)元素基态原子的M层全充满,N层有且只有一个未成对电子,其基态原子的电子排布式为___ ,属于____ 区元素;[Cu(NH3)4]SO4中所含的化学键有___ ,,[Cu(NH3)4]SO4的外界离子的空间构型为____ 。
(1)指出31号元素镓(Ga)在元素周期表中的位置:
(2)写出原子序数最小的第Ⅷ族元素原子的核外的价电子排布图:
(3)写出3p轨道上有2个未成对电子的元素的符号:
(4)日常生活中广泛使用的不锈钢,在其生产过程中添加了某种元素,该元素的价电子排布式为3d54s1,该元素的名称为
(5)基态原子的4s能级中只有1个电子的元素共有
(6)元素基态原子的M层全充满,N层有且只有一个未成对电子,其基态原子的电子排布式为
您最近半年使用:0次
名校
解题方法
6 . 1956年,美籍华人科学家吴健雄用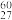 Co放射源进行实验验证了杨振宁和李政道的重要发现(此发现于1957年获得诺贝尔物理学奖)。
Co放射源进行实验验证了杨振宁和李政道的重要发现(此发现于1957年获得诺贝尔物理学奖)。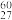 Co的衰变方程为:
Co的衰变方程为: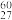 Co=
Co=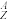 Ni+
Ni+ e-+
e-+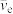 ,其中
,其中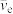 是反中微子,它的电荷数为0, 静止质量可认为是0。下列说法错误的是
是反中微子,它的电荷数为0, 静止质量可认为是0。下列说法错误的是
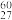 Co放射源进行实验验证了杨振宁和李政道的重要发现(此发现于1957年获得诺贝尔物理学奖)。
Co放射源进行实验验证了杨振宁和李政道的重要发现(此发现于1957年获得诺贝尔物理学奖)。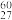 Co的衰变方程为:
Co的衰变方程为: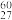 Co=
Co=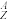 Ni+
Ni+ e-+
e-+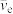 ,其中
,其中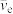 是反中微子,它的电荷数为0, 静止质量可认为是0。下列说法错误的是
是反中微子,它的电荷数为0, 静止质量可认为是0。下列说法错误的是| A.衰变产物Ni质量数是60 |
| B.Co与Ni同在元素周期表的d区 |
| C.Co与Ni基态原子核外电子占据的轨道数不同 |
| D.基态Ni原子的价电子排布为3d84s2 |
您最近半年使用:0次
2020-10-12更新
|
562次组卷
|
4卷引用:江苏省昆山中学2022-2023学年高一下学期期中考试化学试题
江苏省昆山中学2022-2023学年高一下学期期中考试化学试题山东省潍坊市五县2021届高三10月联考化学试题(已下线)押新高考卷08题 物质结构与性质-备战2022年高考化学临考题号押题(新高考通版)(已下线)专题33 物质结构与性质基础-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)
名校
解题方法
7 . 氮、磷、砷、铁等元素及其化合物在现代农业、科技、国防建设中有着许多独特的用途。
(1)基态砷原子中核外电子占据最高能层的符号为__ ,该能层的原子轨道数有__ 个。
(2)氮的一种氢化物N2H4是一种良好的火箭发射燃料,传统制备肼的方法是:NaClO+2NH3=N2H4+NaCl+H2O,又知肼的熔点、沸点分别为1.4℃、113.5℃,氨气的熔点、沸点分别为-77.7℃、-33.5℃。
①N2H4中氮原子的杂化轨道类型为__ 杂化,基态N原子电子占据最高能级的电子云轮廓图为___ 形。
②肼与氨气熔点、沸点差异最主要的原因是__ 。
(3)氨分子是一种常见配体,配离子[Co(NH3)6]3+中存在的化学键有__ (填序号)。
A.离子键 B.极性键 C.配位键 D.氢键
(1)基态砷原子中核外电子占据最高能层的符号为
(2)氮的一种氢化物N2H4是一种良好的火箭发射燃料,传统制备肼的方法是:NaClO+2NH3=N2H4+NaCl+H2O,又知肼的熔点、沸点分别为1.4℃、113.5℃,氨气的熔点、沸点分别为-77.7℃、-33.5℃。
①N2H4中氮原子的杂化轨道类型为
②肼与氨气熔点、沸点差异最主要的原因是
(3)氨分子是一种常见配体,配离子[Co(NH3)6]3+中存在的化学键有
A.离子键 B.极性键 C.配位键 D.氢键
您最近半年使用:0次
名校
解题方法
8 . 下列说法中正确的是( )
| A.同一原子中3s、3p、3d、4s能量依次升高 |
| B.某原子核外电子由1s22s22p63s23p1→1s22s22p63s13p2,原子放出能量 |
| C.p能级的原子轨道呈哑铃形,随着能层数的增加,p能级原子轨道数也在增多 |
| D.按照泡利原理,在同一个原子中不可能存在两个运动状态完全相同的电子 |
您最近半年使用:0次
2020-05-05更新
|
428次组卷
|
8卷引用:四川省攀枝花市第十五中学2019-2020学年高一下学期期中考试化学试题
四川省攀枝花市第十五中学2019-2020学年高一下学期期中考试化学试题四川省攀枝花市成都外国语学校2020-2021学年高一下学期期中考试化学(理)试题福建省厦门双十中学2018-2019学年高二下学期期中考试化学试题安徽省亳州市涡阳县第九中学2019-2020学年高二下学期期末考试化学试题(已下线)第34讲 原子结构与性质-2021年高考化学一轮复习名师精讲练(已下线)第30讲 原子结构与性质(练) — 2022年高考化学一轮复习讲练测(新教材新高考)(已下线)专题十 物质结构与性质(选择性必修2)能力提升检测卷(测)-2023年高考化学一轮复习讲练测(新教材新高考)(已下线)第五章 物质结构与性质元素周期律 第26练 原子结构 核外电子排布原理
9 . 下列有关M层的说法正确的是( )
| A.表示第二电子层 | B.最多能容纳8个电子 |
| C.表示第三电子层 | D.至少应该填充2个电子 |
您最近半年使用:0次
2019-09-22更新
|
157次组卷
|
3卷引用:黑龙江省哈尔滨市宾县第二中学2020-2021学年高一上学期第三次月考化学试题
名校
10 . 下列说法正确的是( )
| A.s电子云是在空间各个方向上伸展程度相同的对称形状 |
| B.p电子云是平面“8”字形的 |
| C.2p能级有一个未成对电子的基态原子的电子排布式一定为1s22s22p5 |
| D.2d能级包含5个原子轨道,最多容纳10个电子 |
您最近半年使用:0次
2018-12-22更新
|
199次组卷
|
8卷引用:高中化学人教版 选修三 第1章 原子结构与性质 电子云与原子轨道
高中化学人教版 选修三 第1章 原子结构与性质 电子云与原子轨道(已下线)同步君 选修3 第一章 第一节 电子云和原子轨道贵州省织金县第一中学2018-2019学年高二上学期期中考试化学试题云南省盐津县第二中学2018-2019学年高二上学期12月份考试化学试题云南省昭通市威信县第一中学2018-2019学年高二上学期12月份考试化学试题湖北省宜昌市葛洲坝中学2018-2019学年高二下学期期中考试化学试题(已下线)1.2.1 基态原子的核外电子排布-2020-2021学年高二化学课时同步练(鲁科2019选择性必修2)(已下线)BBWYhjhx1112.pdf



