名校
解题方法
1 . 据世界权威刊物《自然》最近报道, 选择碲化锆 (ZrTe5)为材料验证了三维量子霍尔效应, 并发现了金属-绝缘体的转换。Te属于ⅥA元素。回答下列问题:
(1)锆(Zr)的简化电子排布式为[Kr]4d25s2,锆原子中d轨道上的电子数是___ ,Zr2+的价电子排布图是___ 。
(2)O、Se、Te的第一电离能由大到小的顺序是___ ,H2O、H2Se、H2Te的沸点由高到低的顺序是___ 。
(3)H2Te和CO2均为三原子分子,但它们的键角差别较大,试用杂化轨道理论解释,理由是___ 。
(4) [Zr(C2H5O)2]2+是Zr4+形成的一种配离子,其中的配位原子是___ (填符号), 1个[Zr(C2H5O)2]2+离子中含共价键的数目是___ 。
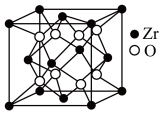
(5)立方氧化锆是一种人工合成的氧化物,其硬度极高,可用于陶瓷和耐火材料,其晶胞结构如图所示。Zr原子的配位数是___ 。若晶胞中距离最近的两个氧原子间的距离为anm,则立方氧化锆的密度为___ g/cm3。
(1)锆(Zr)的简化电子排布式为[Kr]4d25s2,锆原子中d轨道上的电子数是
(2)O、Se、Te的第一电离能由大到小的顺序是
(3)H2Te和CO2均为三原子分子,但它们的键角差别较大,试用杂化轨道理论解释,理由是
(4) [Zr(C2H5O)2]2+是Zr4+形成的一种配离子,其中的配位原子是
(5)立方氧化锆是一种人工合成的氧化物,其硬度极高,可用于陶瓷和耐火材料,其晶胞结构如图所示。Zr原子的配位数是

您最近一年使用:0次
2020-05-24更新
|
622次组卷
|
5卷引用:专题17 物质结构与性质(选修)-2020年高考真题和模拟题化学分项汇编
(已下线)专题17 物质结构与性质(选修)-2020年高考真题和模拟题化学分项汇编四川省泸州市2020届高三第三次教学质量诊断性考试理综化学试题宁夏银川一中2022届高三第一次月考理科综合化学试题宁夏青铜峡市高级中学2021-2022学年高三上学期第一次月考化学试题2020年全国卷Ⅲ化学真题变式题
名校
解题方法
2 . 现有七种元素,其中A、B、C、D、E为短周期主族元素,F、G为第4周期元素,它们的原子序数依次增大。请根据下列相关信息,回答问题。
(1)B基态原子中能量最高的电子,其电子云在空间有______ 个伸展方向,原子轨道呈________ 形。
(2)某同学根据上述信息,推断C基态原子的轨道表示式为 该同学所画的轨道表示式违背了
该同学所画的轨道表示式违背了________________ 。
(3)G位于______ 族__________ 区,价电子排布式为________________ 。
(4)检验F元素的方法是________ ,请用原子结构的知识解释产生此现象的原因:_____________ 。
(5)写出E的单质与水反应的离子方程式:_____________________________________
(6)写出DA3的电子式_______________________ (用元素符号)
| 元素 | 相关信息 |
| A | 元素的核外电子数和电子层数相等,也是宇宙中最丰富的元素 |
| B | 元素原子的核外p电子数比s电子数少1 |
| C | 原子的第一至第四电离能分别是I1=738 kJ·mol-1; I2=1 451 kJ·mol-1;I3=7 733 kJ·mol-1;I4=10 540 kJ·mol-1 |
| D | 原子核外所有p轨道全满或半满 |
| E | 元素的主族序数与周期数的差为4 |
| F | 是前四周期中电负性最小的元素 |
| G | 在周期表的第七列 |
(1)B基态原子中能量最高的电子,其电子云在空间有
(2)某同学根据上述信息,推断C基态原子的轨道表示式为
 该同学所画的轨道表示式违背了
该同学所画的轨道表示式违背了(3)G位于
(4)检验F元素的方法是
(5)写出E的单质与水反应的离子方程式:
(6)写出DA3的电子式
您最近一年使用:0次
2020-02-15更新
|
195次组卷
|
2卷引用:专题2 原子结构与元素性质 专题强化练2 元素周期律的应用及元素推断
3 . 下列电子排布图书写正确且能表明该粒子处于基态的是( )
A.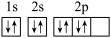 |
B.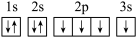 |
C. |
D. |
您最近一年使用:0次
2020-01-03更新
|
213次组卷
|
4卷引用:2020高三总复习二轮复习——物质结构与性质复习卷
4 . 根据原子核外电子排布规则,回答下列问题:
(1)写出基态S原子的核外电子排布式___________________________________ ,写出基态24Cr原子的价电子排布式________________________ ;
(2)写出基态N的原子核外电子排布图:__________________ ;
(3)若将基态14Si的电子排布式写成1s22s22p63s33p1,则它违背了_______________________ ;
(4)Fe3+比Fe2+的稳定性更________ (填“强”或“弱”),从结构上分析原因是____________________________________________________________________________ 。
(1)写出基态S原子的核外电子排布式
(2)写出基态N的原子核外电子排布图:
(3)若将基态14Si的电子排布式写成1s22s22p63s33p1,则它违背了
(4)Fe3+比Fe2+的稳定性更
您最近一年使用:0次
2018-09-26更新
|
844次组卷
|
5卷引用:第1讲 原子结构 核外电子排布



