解题方法
1 . 硫是组成生命的重要元素。回答下列问题:
(1)基态S原子含有___________ 种能量不同的电子,其价层电子排布图是___________ 。
(2)S单质的常见形式为 (
( ),其中S原子采用的轨道杂化方式是
),其中S原子采用的轨道杂化方式是___________ 。
(3)已知化合物 (
( )中键角α为124°,β为96°,α>β的原因主要是
)中键角α为124°,β为96°,α>β的原因主要是___________ 。
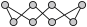
(4) 的结构简图如图所示,其中不存在的作用力有
的结构简图如图所示,其中不存在的作用力有___________ (填字母)。
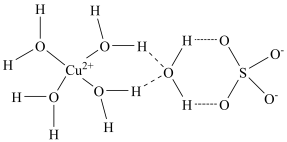
A.氢键 B.共价键 C.金属键 D.配位键
 的空间构型是
的空间构型是___________ ,写出一个与 互为等电子体的阴离子的化学式
互为等电子体的阴离子的化学式___________ 。
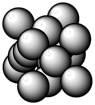
(5)ZnS在光导体材料、涂料等行业中应用广泛。立方ZnS晶体结构如图所示,其晶体密度为 ,若将a位置
,若将a位置 离子的分数坐标确定为(0,0,0),则b位置
离子的分数坐标确定为(0,0,0),则b位置 离子的分数坐标为
离子的分数坐标为___________ , 离子与
离子与 离子的最近距离为
离子的最近距离为___________ pm(列出计算式,阿伏加德罗常数用 表示)。
表示)。

(1)基态S原子含有
(2)S单质的常见形式为
 (
( ),其中S原子采用的轨道杂化方式是
),其中S原子采用的轨道杂化方式是(3)已知化合物
 (
( )中键角α为124°,β为96°,α>β的原因主要是
)中键角α为124°,β为96°,α>β的原因主要是(4)
 的结构简图如图所示,其中不存在的作用力有
的结构简图如图所示,其中不存在的作用力有
A.氢键 B.共价键 C.金属键 D.配位键
 的空间构型是
的空间构型是 互为等电子体的阴离子的化学式
互为等电子体的阴离子的化学式(5)ZnS在光导体材料、涂料等行业中应用广泛。立方ZnS晶体结构如图所示,其晶体密度为
 ,若将a位置
,若将a位置 离子的分数坐标确定为(0,0,0),则b位置
离子的分数坐标确定为(0,0,0),则b位置 离子的分数坐标为
离子的分数坐标为 离子与
离子与 离子的最近距离为
离子的最近距离为 表示)。
表示)。
您最近一年使用:0次
解题方法
2 . 【化学—选修3:物质结构与性质】
铁、铝、铜都是日常生活中常见的金属,它们的单质及其化合物在科学研究和工农业生产中具有广泛用途。请回答以下问题:
(1)超细铜粉可用作导电材料、催化剂等,其制备方法如下:
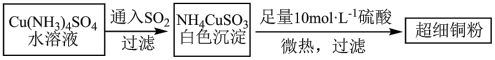
①铜元素位于周期表_________ 区;Cu+的基态价电子排布图_________ ;NH4CuSO3中N、S、O三种元素的第一电离能由大到小的顺序为_________ (元素符号表示)。
②SO42-中心原子的杂化方式为_________ ,SO32-的价层电子互斥模型为_________ 。
(2)请写出向Cu(NH3)4SO4水溶液中通入SO2时发生反应的离子方程式_________ 。
(3)某学生向CuSO4溶液中加入少量氨水生成蓝色沉淀,继续加入过量氨水沉淀溶解,得到深蓝色透明溶液,最后向该溶液中加入一定量乙醇,析出[Cu(NH3)4]SO4·H2O晶体。
①下列说法正确的是_________ 。
a.因NH3和H2O都为极性分子,且它们还存在分子内氢键,所以氨气极易溶于水
b.NH3分子和H2O分子,分子空间构型不同,氨气分子的键角小于水分子的键角
c.Cu(NH3)4SO4所含有的化学键有离子键、极性共价键和配位键
d.Cu(NH3)4SO4组成元素中电负性最大的是氮元素
②请解释加入乙醇后析出晶体的原因_________ 。
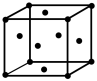
(4)下图所示为金属铜的一个晶胞,此晶胞立方体的边长为a pm,Cu的相对原子质量为64,金属铜的密度为ρ g/cm3,则晶胞中铜原子的配位数为_________ ,用含有a、ρ的代数式表示的阿伏伽德罗常数为:_________ mol-1。
铁、铝、铜都是日常生活中常见的金属,它们的单质及其化合物在科学研究和工农业生产中具有广泛用途。请回答以下问题:
(1)超细铜粉可用作导电材料、催化剂等,其制备方法如下:
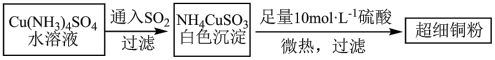
①铜元素位于周期表
②SO42-中心原子的杂化方式为
(2)请写出向Cu(NH3)4SO4水溶液中通入SO2时发生反应的离子方程式
(3)某学生向CuSO4溶液中加入少量氨水生成蓝色沉淀,继续加入过量氨水沉淀溶解,得到深蓝色透明溶液,最后向该溶液中加入一定量乙醇,析出[Cu(NH3)4]SO4·H2O晶体。
①下列说法正确的是
a.因NH3和H2O都为极性分子,且它们还存在分子内氢键,所以氨气极易溶于水
b.NH3分子和H2O分子,分子空间构型不同,氨气分子的键角小于水分子的键角
c.Cu(NH3)4SO4所含有的化学键有离子键、极性共价键和配位键
d.Cu(NH3)4SO4组成元素中电负性最大的是氮元素
②请解释加入乙醇后析出晶体的原因
(4)下图所示为金属铜的一个晶胞,此晶胞立方体的边长为a pm,Cu的相对原子质量为64,金属铜的密度为ρ g/cm3,则晶胞中铜原子的配位数为
您最近一年使用:0次



