解题方法
1 . O3和O2互为___________ (选填“同素异形体”或“同位素”)。氧元素位于元素周期表的___________ 区。
A.s B.p C.d D.f
A.s B.p C.d D.f
您最近一年使用:0次
解题方法
2 . 电负性与电离能是两种定量描述元素原子得失电子能力的参数,请根据下列数据回答问题。
(1)非金属性:S___________ (填“>”、“=”或“<”)F。
(2)依据电负性数值,上述元素中最容易形成离子键的是___________ 和___________ 。
(3)已知某主族元素Y,其基态原子核外有2个电子层,3个未成对电子,Y元素基态原子的轨道表示式为___________ ,通过分析电负性的变化规律,确定Y元素电负性的取值范围是___________ 。
(4)由电负性数据推断:化合物PBr3中P的化合价为___________ 。已知PBr3与水反应是非氧化还原反应,写出PBr3与水反应的化学方程式___________ 。
| 元素符号 | Li | Be | C | O | F | Na | Al | P | S | Br |
| 电负性 | 1.0 | 1.5 | 2.5 | 3.5 | 4.0 | 0.9 | 1.5 | 2.2 | 2.5 | 2.8 |
(2)依据电负性数值,上述元素中最容易形成离子键的是
(3)已知某主族元素Y,其基态原子核外有2个电子层,3个未成对电子,Y元素基态原子的轨道表示式为
(4)由电负性数据推断:化合物PBr3中P的化合价为
您最近一年使用:0次
3 . 基态铬原子核外有___________ 种不同运动状态的电子,其价电子的轨道表示式为___________ 。
您最近一年使用:0次
4 . 请回答下列问题:
(1)基态氟原子核外9个电子,这些电子的电子云形状有___________ 种;氟原子有___________ 种不同能量的电子,价层电子的轨道表示式为___________ 。
(2)已知锡位于第五周期,与C同主族,写出Sn2+的最外层电子排布式:___________ ;Cl-中有___________ 种运动状态不同的电子。
(3)某元素简化电子排布式为[Xe]4f46s2,其应在___________ 区。
(4)Li、B、H元素的电负性由大到小的排列顺序为___________ 。
(5)Li3N中氮以N3-存在,基态N3-的电子排布式为___________ ,外围电子排布为3d104s2的元素在周期表中的位置是 ___________ 。
(6)金属镍粉在CO气流中轻微加热,生成无色挥发性液体Ni(CO)4 ,呈正四面体结构。Ni(CO)4易溶于下列___________ 。
a.水 b.乙醇 c.C6H6(苯) d.NiSO4溶液
(1)基态氟原子核外9个电子,这些电子的电子云形状有
(2)已知锡位于第五周期,与C同主族,写出Sn2+的最外层电子排布式:
(3)某元素简化电子排布式为[Xe]4f46s2,其应在
(4)Li、B、H元素的电负性由大到小的排列顺序为
(5)Li3N中氮以N3-存在,基态N3-的电子排布式为
(6)金属镍粉在CO气流中轻微加热,生成无色挥发性液体Ni(CO)4 ,呈正四面体结构。Ni(CO)4易溶于下列
a.水 b.乙醇 c.C6H6(苯) d.NiSO4溶液
您最近一年使用:0次
2024-05-01更新
|
78次组卷
|
2卷引用:黑龙江省哈尔滨市第三十二中学校2023-2024学年高二下学期4月期中考试化学试题
5 . 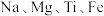 等元素的研究一直在进行中,其单质及化合物在诸多领域都有广泛的应用。请回答下列问题:
等元素的研究一直在进行中,其单质及化合物在诸多领域都有广泛的应用。请回答下列问题:
(1)钠在火焰上灼烧产生的黄光是一种___________ (填字母)。
A.吸收光谱 B.发射光谱
(2) 原子的核外电子,有
原子的核外电子,有___________ 种空间运动状态。
(3) 元素的下列微粒中,电离最外层一个电子所需能量最大的是___________(填标号)。
元素的下列微粒中,电离最外层一个电子所需能量最大的是___________(填标号)。
(4) 原子位于元素周期表中的
原子位于元素周期表中的___________ 区,其价电子排布式为___________ 。与 同周期的过渡元素中,未成对电子数最多的基态原子的价电子的轨道表示式为
同周期的过渡元素中,未成对电子数最多的基态原子的价电子的轨道表示式为___________ 。
(5) 与
与 的离子半径大小关系为
的离子半径大小关系为
___________  (填“大于”或“小于)。
(填“大于”或“小于)。
(6)下列各组多电子原子的能级能量比较不正确的是___________。
① ②
② ③
③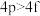 ④
④
(7)很多金属及其化合物在灼烧时会产生特殊的火焰颜色,请用原子结构的知识解释产生此现象的原因是___________ 。
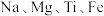 等元素的研究一直在进行中,其单质及化合物在诸多领域都有广泛的应用。请回答下列问题:
等元素的研究一直在进行中,其单质及化合物在诸多领域都有广泛的应用。请回答下列问题:(1)钠在火焰上灼烧产生的黄光是一种
A.吸收光谱 B.发射光谱
(2)
 原子的核外电子,有
原子的核外电子,有(3)
 元素的下列微粒中,电离最外层一个电子所需能量最大的是___________(填标号)。
元素的下列微粒中,电离最外层一个电子所需能量最大的是___________(填标号)。A.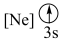 | B.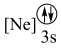 | C.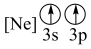 | D.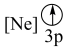 |
(4)
 原子位于元素周期表中的
原子位于元素周期表中的 同周期的过渡元素中,未成对电子数最多的基态原子的价电子的轨道表示式为
同周期的过渡元素中,未成对电子数最多的基态原子的价电子的轨道表示式为(5)
 与
与 的离子半径大小关系为
的离子半径大小关系为
 (填“大于”或“小于)。
(填“大于”或“小于)。(6)下列各组多电子原子的能级能量比较不正确的是___________。
①
 ②
② ③
③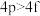 ④
④
| A.①④ | B.③④ | C.①③ | D.②③ |
(7)很多金属及其化合物在灼烧时会产生特殊的火焰颜色,请用原子结构的知识解释产生此现象的原因是
您最近一年使用:0次
2024-04-30更新
|
136次组卷
|
2卷引用:湖北省孝感市重点高中教科研协作体2023-2024学年高二下学期4月期中化学试题
6 . 聚氮化硫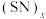 是重要的超导材料,目前已成为全球材料行业研究的热点。
是重要的超导材料,目前已成为全球材料行业研究的热点。
(1)基态S原子的原子核外能量最高的电子电子云轮廓图为___________ 形。
(2)下列电子排布图能表示氮原子的最低能量状态的是___________。
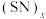 是重要的超导材料,目前已成为全球材料行业研究的热点。
是重要的超导材料,目前已成为全球材料行业研究的热点。(1)基态S原子的原子核外能量最高的电子电子云轮廓图为
(2)下列电子排布图能表示氮原子的最低能量状态的是___________。
A. | B.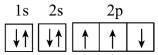 |
C.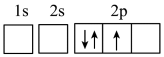 | D. |
您最近一年使用:0次
2024-04-23更新
|
87次组卷
|
2卷引用:上海市华东师范大学第三附属中学2023-2024学年高二下学期期中考试 化学试题(等级考)
7 . 画出基态硼原子的价电子层的轨道表示式___________ 。
您最近一年使用:0次
8 . 硅、锗(Ge)及其化合物广泛应用于光电材料领域。回答下列问题:
(1)基态硅原子最外层的轨道表示式为______ ,晶体硅和碳化硅熔点较高的是______ (填化学式);
(2)硅和卤素单质反应可以得到SiX4.SiX4的熔、沸点大小如下表所示:
①0℃时,SiF4、SiCl4、SiBr4、SiI4呈液态的是______ (填化学式),沸点依次升高的原因是______ ,气态SiX4分子的空间构型是______ ;
②SiCl4与N甲基咪唑(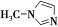 )反应可以得到M2+,其结构如图所示:
)反应可以得到M2+,其结构如图所示:
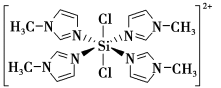
N甲基咪唑分子中碳原子的杂化轨道类型为______ ,H、C、N的电负性由大到小的顺序为______ ,1个M2+中含有______ 个σ键;
(1)基态硅原子最外层的轨道表示式为
(2)硅和卤素单质反应可以得到SiX4.SiX4的熔、沸点大小如下表所示:
| SiF4 | SiCl4 | SiBr4 | SiI4 | |
| 熔点/K | 183.0 | 203.2 | 278.6 | 393.7 |
| 沸点/K | 187.2 | 330.8 | 427.2 | 560.7 |
②SiCl4与N甲基咪唑(
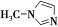 )反应可以得到M2+,其结构如图所示:
)反应可以得到M2+,其结构如图所示:
N甲基咪唑分子中碳原子的杂化轨道类型为
您最近一年使用:0次
9 . 回答下列问题。
(1)自然界中存在的碘的稳定性核素是碘-127(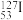 )。日本福岛第一核电站事故释放出的放射性物质中,含有人工放射性核素碘-131(
)。日本福岛第一核电站事故释放出的放射性物质中,含有人工放射性核素碘-131(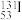 )。碘-131一旦被人体吸入,就可能会引发甲状腺疾病。下列关于这两种核素的说法正确的是___________(填字母)。
)。碘-131一旦被人体吸入,就可能会引发甲状腺疾病。下列关于这两种核素的说法正确的是___________(填字母)。
(2)核电站为防止发生核辐射事故,通常用含有铅的水泥做成屏蔽罩,内衬钢板,反应的压力容器用铁、铜、锰等具有反辐射合金材料制成。
①水泥中通常含有碳、氧、硅、铝等元素,则四种元素中3p能级上存在电子的是___________ (填元素符号)。
②写出二价铜离子的基态电子排布式:___________ 。
③铅的核电荷数为82,在周期表中___________ (填能级符号)区。
④基态锰原子价电子轨道表示式为___________ ,锰原子中能量最低的电子为___________ 轨道上的电子,其轨道呈___________ 形。
(1)自然界中存在的碘的稳定性核素是碘-127(
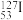 )。日本福岛第一核电站事故释放出的放射性物质中,含有人工放射性核素碘-131(
)。日本福岛第一核电站事故释放出的放射性物质中,含有人工放射性核素碘-131(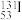 )。碘-131一旦被人体吸入,就可能会引发甲状腺疾病。下列关于这两种核素的说法正确的是___________(填字母)。
)。碘-131一旦被人体吸入,就可能会引发甲状腺疾病。下列关于这两种核素的说法正确的是___________(填字母)。A.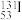 和 和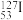 的价电子排布不相同 的价电子排布不相同 |
B.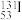 和 和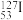 的电负性不相等 的电负性不相等 |
C.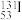 的基态电子排布式中只有1个能级未充满电子 的基态电子排布式中只有1个能级未充满电子 |
| D.碘元素的第一电离能大于氯元素 |
①水泥中通常含有碳、氧、硅、铝等元素,则四种元素中3p能级上存在电子的是
②写出二价铜离子的基态电子排布式:
③铅的核电荷数为82,在周期表中
④基态锰原子价电子轨道表示式为
您最近一年使用:0次
2024-03-12更新
|
60次组卷
|
2卷引用:甘肃省武威市天祝一中、民勤一中2023-2024学年高二下学期5月期中联考化学试题
名校
解题方法
10 . Goodenough等人因在锂离子电池及钴酸锂、磷酸铁锂等正极材料研究方面的卓越贡献而获得诺贝尔化学奖。回答下列问题:
(1)下列Li原子电子排布图表示的状态中,能量最低的为______ ,能量最高的为______ (填标号)。 与
与 离子中未成对的电子数之比为
离子中未成对的电子数之比为______ 。
(3) 与
与 具有相同的电子构型,
具有相同的电子构型,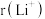 小于
小于 ,原因是
,原因是______ 。
(4)与铁同周期元素中,4s轨道半充满的元素______ (用元素符号表示)。
(5)已知:元素的一个气态原子获得电子成为气态阴离子时所放出的能量称为电子亲和能。下列有关说法正确的是______ (填字母)。
b.Na的第一电离能为603.4kJ/mol
c.Cl的第一电子亲和能为348.3kJ/mol
(1)下列Li原子电子排布图表示的状态中,能量最低的为
A. B.
B.
C. D.
D.
 与
与 离子中未成对的电子数之比为
离子中未成对的电子数之比为(3)
 与
与 具有相同的电子构型,
具有相同的电子构型,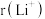 小于
小于 ,原因是
,原因是(4)与铁同周期元素中,4s轨道半充满的元素
(5)已知:元素的一个气态原子获得电子成为气态阴离子时所放出的能量称为电子亲和能。下列有关说法正确的是

b.Na的第一电离能为603.4kJ/mol
c.Cl的第一电子亲和能为348.3kJ/mol
您最近一年使用:0次
2024-01-03更新
|
259次组卷
|
2卷引用:陕西师范大学附属中学2023-2024学年高二上学期期中考试化学试题



