1 . 硼及其化合物在材料制造、有机合成等方面用途非常广泛。回答下列问题:
(1)VB2是一种导电陶瓷材料,基态钒原子的价电子排布图为_______ 。
(2)B、C、N三种元素第一电离能由小到大的顺序为________ 。
(3)硼的卤化物在工业中有重要作用,硼的四种卤化物的沸点如下表所示。
①四种卤化物沸点依次升高的原因是__________________ 。
②用BF3分子结构解释反应BF3(g)+NH4F(s)==NH4[BF4] (s)能够发生的原因:____________ 。
制备环硼氨烷的方法如下:

BCl3、LiBH4中硼原子的杂化轨道类型依次为_________ ;与B3N3H6互为等电子体的分子的结构简式为________________ 。
(4)立方氮化硼的熔点为3000℃,其晶胞结构如图所示,晶胞参数a=361.5pm。
①立方氮化硼的晶体类型为_______________ 。
②紧邻的两个硼原子间的距离为_______ (列出计算式即可) pm。
③立方氮化硼的密度为_____ (列出计算式即可)g•㎝-3。
(1)VB2是一种导电陶瓷材料,基态钒原子的价电子排布图为
(2)B、C、N三种元素第一电离能由小到大的顺序为
(3)硼的卤化物在工业中有重要作用,硼的四种卤化物的沸点如下表所示。
| BF3 | BCl3 | BBr3 | BI3 | |
| 沸点/K | 172 | 285 | 364 | 483 |
②用BF3分子结构解释反应BF3(g)+NH4F(s)==NH4[BF4] (s)能够发生的原因:
制备环硼氨烷的方法如下:

BCl3、LiBH4中硼原子的杂化轨道类型依次为
(4)立方氮化硼的熔点为3000℃,其晶胞结构如图所示,晶胞参数a=361.5pm。
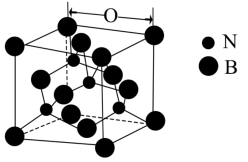
①立方氮化硼的晶体类型为
②紧邻的两个硼原子间的距离为
③立方氮化硼的密度为
您最近一年使用:0次
2017-04-20更新
|
308次组卷
|
2卷引用:2017届湖南省郴州市高三第四次质量检测理科综合化学试卷
2 . 【化学选修3:物质结构与性质】A、B、C、D、E五种元素的原子序数依次增大,其中非金属元素A的基态原子中成对电子数是未成时电子数的两倍,C元素在地壳中含量最高,D的单质是短周期中熔点最低的金属,E的合金是我国使用最早的合金。
(1)E元素的基态原子电子排布式为__________________ 。
(2)A的某种氢化物A2H2分子中含有___ 个σ键和____ 个π键。
(3)A 的含氧酸根离子AO3n-的空间构型是___________ 。
(4)B的最简单的氢化物的沸点比A 的最简单的氢化物的沸点高得多,其原因是_____ 。
(5)E的最高价氧化物对应的水化物溶解于氨水中生成的复杂化合物的化学式是______ 。
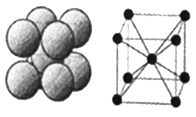
(6)下图是D单质的晶体堆积方式,这种堆积方式的晶胞中原子的配位数为____ ,若该原子的半径为rpm ,此晶体的密度ρ=______ g/cm3(用含r的代数式表示,阿伏伽德罗常数用NA表示)。
(1)E元素的基态原子电子排布式为
(2)A的某种氢化物A2H2分子中含有
(3)A 的含氧酸根离子AO3n-的空间构型是
(4)B的最简单的氢化物的沸点比A 的最简单的氢化物的沸点高得多,其原因是
(5)E的最高价氧化物对应的水化物溶解于氨水中生成的复杂化合物的化学式是
(6)下图是D单质的晶体堆积方式,这种堆积方式的晶胞中原子的配位数为

您最近一年使用:0次
2017-02-24更新
|
855次组卷
|
4卷引用:2017届湖南省郴州市高三第三次质量检测理科综合化学试卷



