1 . 呼吸面具中的Na2O2可吸收CO2放出O2,若用超氧化钾(KO2)代替Na2O2也可以得到类似的产物,起到同样的作用。
(1)标准状况下,若有30mL的CO2气体通过盛有足量的KO2的装置充分反应后,逸出气体的体积为_______ mL;
(2)标准状况下,若一定量的CO2(过量),通过盛有7.24gKO2和Na2O2的均匀混合物的装置充分反应后,逸出的气体中O2体积为1568mL,则混合物中KO2和Na2O2的物质的量分别为:KO2_______ mol、Na2O2_______ mol;
(3)比较Na2O2和KO2中氧氧键的键能大小,并说明理由:_______ 。
(1)标准状况下,若有30mL的CO2气体通过盛有足量的KO2的装置充分反应后,逸出气体的体积为
(2)标准状况下,若一定量的CO2(过量),通过盛有7.24gKO2和Na2O2的均匀混合物的装置充分反应后,逸出的气体中O2体积为1568mL,则混合物中KO2和Na2O2的物质的量分别为:KO2
(3)比较Na2O2和KO2中氧氧键的键能大小,并说明理由:
您最近一年使用:0次
解题方法
2 . (1)195K,三氧化二磷在二氯甲烷中与臭氧反应得到P4O18.画出P4O18分子的结构示意图_____ 。
(2)CH2SF4是一种极性溶剂,其分子几何构型符合价层电子对互斥(VSEPR)模型。画出CH2SF4的分子结构示意图(体现合理的成键及角度关系)_____ 。
(3)2018年足球世界杯比赛用球使用了生物基三元乙丙橡胶(EPDM)产品Keltan Eco。EPDM属三元共聚物,由乙烯、丙烯及第三单体经溶液共聚而成。
① EPDM具有优良的耐紫外光、耐臭氧、耐腐蚀等性能。写出下列分子中不可用于制备EPDM的第三单体(可能多选,答案中含错误选项不得分)_____ 。
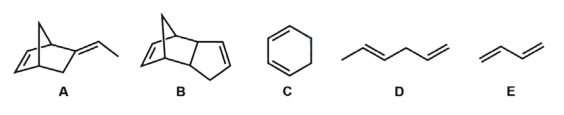
②合成高分子主要分为塑料、纤维和橡胶三大类,下列高分子中与EPDM同为橡胶的是:_____ 。
F.聚乙烯 G.聚丙烯腈 H.反式聚异戊二烯 I.聚异丁烯
(2)CH2SF4是一种极性溶剂,其分子几何构型符合价层电子对互斥(VSEPR)模型。画出CH2SF4的分子结构示意图(体现合理的成键及角度关系)
(3)2018年足球世界杯比赛用球使用了生物基三元乙丙橡胶(EPDM)产品Keltan Eco。EPDM属三元共聚物,由乙烯、丙烯及第三单体经溶液共聚而成。
① EPDM具有优良的耐紫外光、耐臭氧、耐腐蚀等性能。写出下列分子中不可用于制备EPDM的第三单体(可能多选,答案中含错误选项不得分)

②合成高分子主要分为塑料、纤维和橡胶三大类,下列高分子中与EPDM同为橡胶的是:
F.聚乙烯 G.聚丙烯腈 H.反式聚异戊二烯 I.聚异丁烯
您最近一年使用:0次
3 .
(1)分别将O2、KO2、 BaO2 和O2[AsF6]填入与O- O键长相对应的空格中。
(2)在配合物A和B中,O2为配体与中心金属离子配位。A的化学式为[Co2O2(NH3)10]4+,其O- O的键长为147 pm; B的化学式为Co(bzacen)PyO2,其O- O的键长为126 pm, Py 是吡啶(C5H5N),bzacen 是四齿配体[C6H5 -C(O-)=CH -C(CH3) =NCH2- ]2.B具有室温吸氧,加热脱氧的功能,可作为人工载氧体。画出A和B的结构简图(图中必须明确表明O-O与金属离子间的空间关系),并分别指出A和B中Co的氧化态。
(1)分别将O2、KO2、 BaO2 和O2[AsF6]填入与O- O键长相对应的空格中。
| O- O键长 | 112 pm | 121 pm | 128 pm | 149 pm |
| 化学式 |
(2)在配合物A和B中,O2为配体与中心金属离子配位。A的化学式为[Co2O2(NH3)10]4+,其O- O的键长为147 pm; B的化学式为Co(bzacen)PyO2,其O- O的键长为126 pm, Py 是吡啶(C5H5N),bzacen 是四齿配体[C6H5 -C(O-)=CH -C(CH3) =NCH2- ]2.B具有室温吸氧,加热脱氧的功能,可作为人工载氧体。画出A和B的结构简图(图中必须明确表明O-O与金属离子间的空间关系),并分别指出A和B中Co的氧化态。
| 配合物 | a | b |
| 结构简图 | ||
| Co的氧化态 |
您最近一年使用:0次
4 . 冰有+六种晶型。冰中每个水分子与周围4个水分子形成氢键,氢键键长可表示为通过氢键相连接的两个氧原子的核间距。
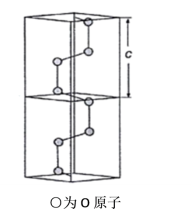
(1)自然界中最常见的冰是冰-Ih,属六方晶系(如图),晶胞参数a=b=449.75pm,c=732.24pm。
①设冰-Ih中键角均为109.5°,计算氢键键长_____ 。
②冰-Ih理想模型中与每个氧原子相连的4个氧原子构成正四面体。计算实际晶体与理想模型的晶胞参数c的相对偏差(用百分数表示)_______ 。
(2)冰-XI是冰-Ih在低温下的平衡结构,可在低于72K,常压下从KOH稀溶液中析出,其网状结构与冰-In相似,但氢原子位置是有序的。冰-XI属正交晶系,晶胞参数a=450.19pm,b=779.78pm,c=732.80pm,计算该晶胞中水分子的个数________ 。
(3)冰–Ic是一种亚稳态,在-80°C由水蒸气凝结而成,属立方晶系,晶体内所有氢键键长均相等,晶胞参数a=635.80pm。计算氢键键长并给出该晶体的点阵类型_____ (不考虑氢原子,须写出简要的分析过程)。
(4)在高压下,可得到立方晶系的冰-X,晶胞参数a=278.50pm。在冰-X中,所有氢键键长均相等,且氢原子在相邻两个氧原子的中点。求冰-X的密度与冰—Ic密度的比值并确定其点阵类型______ (须写出简要的分析过程)。
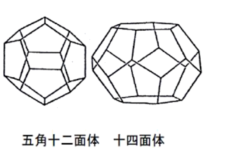
(5)水与一些气体形成笼状化合物晶体。气体A与水形成的晶体由五角十二面体和十四面体两种水笼(图4.2)构成,每个水笼中心均包含一个A分子(视为球形),X射线衍射表明该晶体属立方晶系,晶胞中心为对称中心,体对角线为3次旋转轴。已知其中两个A的分数坐标分别为0,0,0和0,1/2,1/4。写出该晶胞所有A的分数坐标及相应水笼的类型______ ;不考虑氢原子,写出该晶体的点阵类型(须写出简要的分析过程)______ 。
(1)自然界中最常见的冰是冰-Ih,属六方晶系(如图),晶胞参数a=b=449.75pm,c=732.24pm。

①设冰-Ih中键角均为109.5°,计算氢键键长
②冰-Ih理想模型中与每个氧原子相连的4个氧原子构成正四面体。计算实际晶体与理想模型的晶胞参数c的相对偏差(用百分数表示)
(2)冰-XI是冰-Ih在低温下的平衡结构,可在低于72K,常压下从KOH稀溶液中析出,其网状结构与冰-In相似,但氢原子位置是有序的。冰-XI属正交晶系,晶胞参数a=450.19pm,b=779.78pm,c=732.80pm,计算该晶胞中水分子的个数
(3)冰–Ic是一种亚稳态,在-80°C由水蒸气凝结而成,属立方晶系,晶体内所有氢键键长均相等,晶胞参数a=635.80pm。计算氢键键长并给出该晶体的点阵类型
(4)在高压下,可得到立方晶系的冰-X,晶胞参数a=278.50pm。在冰-X中,所有氢键键长均相等,且氢原子在相邻两个氧原子的中点。求冰-X的密度与冰—Ic密度的比值并确定其点阵类型
(5)水与一些气体形成笼状化合物晶体。气体A与水形成的晶体由五角十二面体和十四面体两种水笼(图4.2)构成,每个水笼中心均包含一个A分子(视为球形),X射线衍射表明该晶体属立方晶系,晶胞中心为对称中心,体对角线为3次旋转轴。已知其中两个A的分数坐标分别为0,0,0和0,1/2,1/4。写出该晶胞所有A的分数坐标及相应水笼的类型

您最近一年使用:0次
解题方法
5 . 好奇心是科学发展的内在动力一。P2O3 和P2O5是两种经典的化合物,其分子结构已经确定。自然而然会有如下问题:是否存在磷氧原子比介于二者之间的化合物?由此出发,化学家合成并证实了这些中间化合物的存在。
(1)写出这些中间化合物的分子式____ 。
(2)画出其中具有2重旋转轴的分子的结构图。根据键长不同,将P-O键分组并用阿拉伯数字标出(键长相同的用同一个数字标识)____ 。比较键角∠O-P(V)-O和∠O-P(III)-O的大小____ 。
(3)NH3分子独立存在时H-N-H键角为106.7°。如图是[Zn(NH3)6]2+离子的部分结构以及H-N-H键角的测量值。解释配合物中H-N-H键角变为109.5°的原因____ 。

(1)写出这些中间化合物的分子式
(2)画出其中具有2重旋转轴的分子的结构图。根据键长不同,将P-O键分组并用阿拉伯数字标出(键长相同的用同一个数字标识)
(3)NH3分子独立存在时H-N-H键角为106.7°。如图是[Zn(NH3)6]2+离子的部分结构以及H-N-H键角的测量值。解释配合物中H-N-H键角变为109.5°的原因

您最近一年使用:0次
解题方法
6 . 量子化学计算预测未知化合物是现代化学发展的途径之一。2016 年2月有人通过计算预言铁也存在四氧化物,其分子构型是四面体,但该分子中铁的氧化态是+6而不是+8。
(1)写出该分子中铁的价电子组态____ 。
(2)画出该分子结构的示意图(用元素符号表示原子,用短线表示原子间的化学键)____ 。
(1)写出该分子中铁的价电子组态
(2)画出该分子结构的示意图(用元素符号表示原子,用短线表示原子间的化学键)
您最近一年使用:0次



