20-21高二·全国·课时练习
1 . A、B、C、D、E五种元素原子序数依次增大,A元素原子的价电子排布为ns2np2,B元素的最外层电子数是其电子层数的3倍,E元素原子的价电子排布为3d64s2。C、D的电离能数据如下(kJ·mol-1):
(1)化合价是元素的一种性质。由C、D的电离能数据判断,C通常显___________ 价,D显___________ 价。
(2)某气态单质甲与化合物AB分子中电子总数相等,则甲分子中包含1个___________ 键,2个___________ 键。
(3)AB的总键能大于甲的总键能,但AB比甲容易参加化学反应。根据下表数据,说明AB比甲活泼的原因是___________ 。
| I1 | I2 | I3 | I4 | |
| C | 738 | 1451 | 7733 | 10540 |
| D | 577 | 1817 | 2745 | 11578 |
(2)某气态单质甲与化合物AB分子中电子总数相等,则甲分子中包含1个
(3)AB的总键能大于甲的总键能,但AB比甲容易参加化学反应。根据下表数据,说明AB比甲活泼的原因是
| 单键 | 双键 | 叁键 | |
| AB键能/(kJ·mol-1) | 357.7 | 798.9 | 1071.9 |
| 甲键能/(kJ·mol-1) | 154.8 | 418.4 | 941.7 |
您最近一年使用:0次
2 . Q、R、X、M、Y、Z是元素周期表前四周期的六种元素,原子序数依次递增。已知:
①Z位于 区,最外层没有单电子,其余的均为短周期主族元素;
区,最外层没有单电子,其余的均为短周期主族元素;
②基态Y原子的价电子排布式为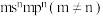 ;
;
③基态Q、X原子p轨道的未成对电子数都是2;
④基态M原子的 能级有1个单电子。
能级有1个单电子。
请回答下列问题:
(1)Z在周期表中的位置为______ 。
(2)Q、R、X、M四种元素第一电离能由大到小的顺序为______ (用对应元素的符号填写)。
(3)分析下表中两种物质的键能数据(单位: )。
)。
结合数据说明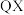 比
比 活泼的原因:
活泼的原因:__________________ 。
①Z位于
 区,最外层没有单电子,其余的均为短周期主族元素;
区,最外层没有单电子,其余的均为短周期主族元素;②基态Y原子的价电子排布式为
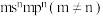 ;
;③基态Q、X原子p轨道的未成对电子数都是2;
④基态M原子的
 能级有1个单电子。
能级有1个单电子。请回答下列问题:
(1)Z在周期表中的位置为
(2)Q、R、X、M四种元素第一电离能由大到小的顺序为
(3)分析下表中两种物质的键能数据(单位:
 )。
)。 |  |  | |
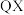 | 351 | 745 | 1076 |
 | 196 | 418 | 945 |
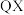 比
比 活泼的原因:
活泼的原因:
您最近一年使用:0次



