1 . 科研人员开发了一种生产药物中间体三氟甲苯的方法: 为阿伏加德罗常数的值,下列叙述正确的是
为阿伏加德罗常数的值,下列叙述正确的是
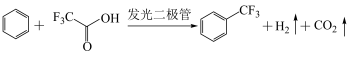
 为阿伏加德罗常数的值,下列叙述正确的是
为阿伏加德罗常数的值,下列叙述正确的是A.1mol三氟甲苯中 键数目为15 键数目为15 |
B.1mol  和 和 组成的混合物中原子总数为2 组成的混合物中原子总数为2 |
C.生成22.4L  时,需消耗1mol苯 时,需消耗1mol苯 |
D.1L 1 三氟乙酸溶液中, 三氟乙酸溶液中, 的数目为 的数目为 |
您最近半年使用:0次
解题方法
2 . 依据物质结构知识回答下列问题。
Ⅰ.硒是一种非金属,可以用作光敏材料、电解锰行业的催化剂。
(1)Se是元素周期表中第34号元素,其基态原子的核外电子简化电子排布式为___________ 。
(2)根据价层电子对互斥理论,可以推知 的空间构型为
的空间构型为___________ ,其中Se原子采用的轨道杂化方式为___________ 。
(3)已知 与
与 结构相似,①
结构相似,① 分子内的键角
分子内的键角 、②
、② 分子内的键角
分子内的键角 、③
、③ 分子内的键角
分子内的键角 ,三种键角由大到小的顺序为
,三种键角由大到小的顺序为___________ (填序号)。
Ⅱ.碳是一种重要元素,可形成多种单质及化合物。
(4)已知 与
与 结构相似,推算HCN分子中
结构相似,推算HCN分子中 键与
键与 键数目之比为
键数目之比为___________ 。氨基氰( )为原料可制得类石墨相氮化碳(
)为原料可制得类石墨相氮化碳( ),氨基氰(
),氨基氰( )分子中碳、氮原子均满足8电子稳定结构,则该分子的结构式为
)分子中碳、氮原子均满足8电子稳定结构,则该分子的结构式为___________ 。
(5)“C919”飞机机身使用的复合材料——碳纤维和环氧树脂。下列电子排布图能表示碳原子的最低能量状态的是___________。
Ⅰ.硒是一种非金属,可以用作光敏材料、电解锰行业的催化剂。
(1)Se是元素周期表中第34号元素,其基态原子的核外电子简化电子排布式为
(2)根据价层电子对互斥理论,可以推知
 的空间构型为
的空间构型为(3)已知
 与
与 结构相似,①
结构相似,① 分子内的键角
分子内的键角 、②
、② 分子内的键角
分子内的键角 、③
、③ 分子内的键角
分子内的键角 ,三种键角由大到小的顺序为
,三种键角由大到小的顺序为Ⅱ.碳是一种重要元素,可形成多种单质及化合物。
(4)已知
 与
与 结构相似,推算HCN分子中
结构相似,推算HCN分子中 键与
键与 键数目之比为
键数目之比为 )为原料可制得类石墨相氮化碳(
)为原料可制得类石墨相氮化碳( ),氨基氰(
),氨基氰( )分子中碳、氮原子均满足8电子稳定结构,则该分子的结构式为
)分子中碳、氮原子均满足8电子稳定结构,则该分子的结构式为(5)“C919”飞机机身使用的复合材料——碳纤维和环氧树脂。下列电子排布图能表示碳原子的最低能量状态的是___________。
A. | B. |
C.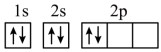 | D.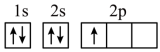 |
您最近半年使用:0次
名校
3 . 某实验小组为探究Fe3+配合物的性质,进行如下实验: 为浅紫色,
为浅紫色, 为红色,
为红色, 为无色
为无色 和
和 可发生电离,方程式如下:
可发生电离,方程式如下:
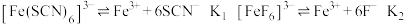
下列说法不正确的是

 为浅紫色,
为浅紫色, 为红色,
为红色, 为无色
为无色 和
和 可发生电离,方程式如下:
可发生电离,方程式如下: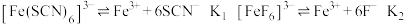
下列说法不正确的是
A.1个配离子 含有的 含有的 键数为12 键数为12 |
B.由上述实验现象可得出平衡常数 |
C.若 中的配体结构为 中的配体结构为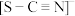 ,则配位原子为 ,则配位原子为 |
D.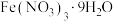 溶于水后溶液呈黄色而不是浅紫色,可能是因为 溶于水后溶液呈黄色而不是浅紫色,可能是因为 发生了水解 发生了水解 |
您最近半年使用:0次
名校
解题方法
4 . 下列分子中 键与
键与 键数目比为
键数目比为 的是
的是
 键与
键与 键数目比为
键数目比为 的是
的是A. | B. | C. | D. |
您最近半年使用:0次
名校
5 . 设NA为阿伏加德罗常数的值。砷化镓(GaAs)是半导体材料,气相生长法制备GaAs的原理如下,已知镓晶体与金刚石结构相似,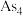 结构与白磷
结构与白磷 相似,下列叙述正确的是
相似,下列叙述正确的是
①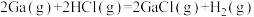
②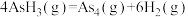
③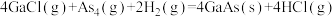
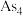 结构与白磷
结构与白磷 相似,下列叙述正确的是
相似,下列叙述正确的是①
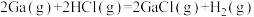
②
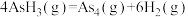
③
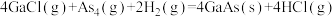
A.7.0 g镓(Ga)含共价键数目为 |
B.0.1 mol 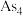 含σ键数目为 含σ键数目为 |
C.标准状况下,0.448 L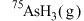 含中子的数目为 含中子的数目为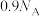 |
D.反应③中每生成1 mol GaAs转移的电子数目为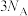 |
您最近半年使用:0次
解题方法
6 . 我国科学家在烷烃的羰基化方面进行了相关的研究,如乙烷在氯化1-戊基吡啶(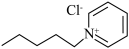 )与无水AlCl3等组成的超强酸性室温离子液体中与Co的直接羰基化反应,产物为丙酮(CH3COCH3)。下列说法正确的是
)与无水AlCl3等组成的超强酸性室温离子液体中与Co的直接羰基化反应,产物为丙酮(CH3COCH3)。下列说法正确的是
| A.丙酮中σ键与π键个数之比为8:1 |
| B.氯化1-戊基吡啶与丙酮的晶体类型相同 |
| C.氯化1-戊基吡啶中的碳原子与丙酮中的碳原子的杂化方式相同 |
D.吡啶(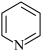 )与苯都是非极性分子 )与苯都是非极性分子 |
您最近半年使用:0次
名校
解题方法
7 . A、B、C、D、E、F、G、H是元素周期表前四周期常见元素,且原子序数依次增大,相关信息如下表:
请用化学用语填空:
(1)A元素在元素周期表中的位置___________ ;C元素和F元素的电负性比较,较小的是___________ (填元素符号)。
(2)B元素与宇宙中含量最丰富的元素形成的最简单化合物的电子式为___________ ,B元素所形成的单质分子中σ键与π键数目之比为___________ 。
(3)F元素原子的价电子的轨道表示式是___________ ;G的高价阳离子的溶液与H单质反应的离子方程式为___________ ;元素X与元素E在周期表中呈对角线关系,且元素X的最高价氧化物的水化物也具有两性,试写出X元素的最高价氧化物的水化物与D元素的最高价氧化物的水化物反应的化学方程式___________ 。
| 元素 | 元素相关信息 |
| A | 原子核外有6种不同运动状态的电子 |
| C | 基态原子中s电子总数与p电子总数相等 |
| D | 原子半径在同周期元素中最大 |
| E | 基态原子最外层电子排布式为 |
| F | 基态原子的最外层p轨道有两个电子的自旋方向与其他电子的自旋方向相反 |
| G | 基态原子核外有7个能级且能量最高的能级上有6个电子 |
| H | 是我国使用最早的合金中的最主要元素 |
(1)A元素在元素周期表中的位置
(2)B元素与宇宙中含量最丰富的元素形成的最简单化合物的电子式为
(3)F元素原子的价电子的轨道表示式是
您最近半年使用:0次
名校
8 . 设NA为阿佛加德罗常数的值,下列叙述正确的是
A.32gS8(分子结构: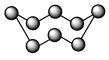 )中的共价键数目为2NA )中的共价键数目为2NA |
| B.100g质量分数为17%的H2O2水溶液中极性键数目为NA |
| C.18g重水中含有的中子数为10NA |
| D.30g二氧化硅晶体中含有的σ键数目为2NA |
您最近半年使用:0次
名校
解题方法
9 . 下列说法错误的是
| A.丙烯(CH3CH=CH2)分子中含有7个σ键1个π键 |
B. 离子中不存在π键结构 离子中不存在π键结构 |
| C.乙烯与乙烷化学性质不同,主要是因为乙烯中的π键不如σ键牢固 |
D.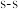 σ键与p—p σ键的电子云图像都呈轴对称 σ键与p—p σ键的电子云图像都呈轴对称 |
您最近半年使用:0次
名校
解题方法
10 . 已知 的结构如图,
的结构如图, 在KOH溶液中可发生反应:
在KOH溶液中可发生反应: ,设
,设 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
 的结构如图,
的结构如图, 在KOH溶液中可发生反应:
在KOH溶液中可发生反应: ,设
,设 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是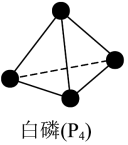
A.产物 分子中所有的原子可能共平面 分子中所有的原子可能共平面 |
B. 中P原子为 中P原子为 杂化 杂化 |
C.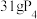 含有 含有 个P-P键(P的相对原子质量:31) 个P-P键(P的相对原子质量:31) |
D. 为非极性分子 为非极性分子 |
您最近半年使用:0次



