1 . 请回答下列问题。
(1)金属铝的卤化物熔点如下表:
请画出其中不属于分子晶体的卤化铝的电子式_______ ,加热分解某种铵盐X,可以1:3的物质的量比获得该卤化铝与一种离子化合物Y,Y的阳离子与阴离子具有相同的核外电子数,写出X的化学式_______ 。
(2)广义氢键理论认为除了与N、O、F原子形成氢键外,H原子还可以与很多带部分负电荷的原子形成氢键,请用广义氢键理论解释氮硼烷(H3N-BH3) 的沸点比乙烷(H3C-CH3)高285°C的原因________ 。
(1)金属铝的卤化物熔点如下表:
| 化学式 | AlF3 | AlCl3 | AlBr3 | AlI3 |
| 熔点/°C | 1290 | 180 | 97.5 | 188 |
请画出其中不属于分子晶体的卤化铝的电子式
(2)广义氢键理论认为除了与N、O、F原子形成氢键外,H原子还可以与很多带部分负电荷的原子形成氢键,请用广义氢键理论解释氮硼烷(H3N-BH3) 的沸点比乙烷(H3C-CH3)高285°C的原因
您最近一年使用:0次
解题方法
2 . 下列关于氢键X-H…Y的说法中,错误的是
| A.氢键是共价键的一种 |
| B.X、Y元素具有跟大的电负性,是氢键形成的基本条件 |
| C.同一分子内不可能形成氢键 |
| D.氢键能增大很多物质分子之间的作用力,导致沸点升高 |
您最近一年使用:0次
2022-04-24更新
|
289次组卷
|
6卷引用:浙江省诸暨市海亮高级中学2021-2022学年高二上学期期中考试化学试题
浙江省诸暨市海亮高级中学2021-2022学年高二上学期期中考试化学试题人教2019选择性必修2第二章第三节 分子结构与物质的性质课后习题(已下线)2.3.2 分子间作用力 分子的手性-2021-2022学年高二化学课后培优练(人教版2019选择性必修2)海南省儋州川绵中学2021-2022学年高二下学期期中考试化学试题新疆疏勒县实验学校2021-2022学年高二下学期期中考试化学试题海南省儋州川绵中学2021-2022学年高二下学期第二次月考化学试题
解题方法
3 . 填空。
(1)化合物A、B、C的熔点如下表:
化合物C的熔点明显高于A的原因是___________ 。
(2)20%的NaCl溶液中滴加乙醇会有白色固体析出,原因是___________ 。
(1)化合物A、B、C的熔点如下表:
| A | B | C | |
| 化学式 | CH3CH2Cl | CH3CH2CH2Cl | CH3NH3Cl |
| 熔点/℃ | -139 | -123 | 230 |
(2)20%的NaCl溶液中滴加乙醇会有白色固体析出,原因是
您最近一年使用:0次
名校
4 . 如图为冰晶体的结构模型,大球代表O原子,小球代表H原子,下列有关说法正确的是

| A.每个水分子与周围邻近的四个水分子间通过H-O键形成冰晶体 |
| B.冰晶体是四面体型的空间网状结构,属于原子晶体 |
| C.冰晶体熔化时,水分子之间的空隙增大 |
| D.lmol冰晶体中最多含有2mol氢键 |
您最近一年使用:0次
2022-02-25更新
|
484次组卷
|
7卷引用:浙江省名校协作体2021-2022学年高三下学期化学模拟试题
名校
解题方法
5 . 下列说法正确的是
A.用电子式表示CaCl2的形成: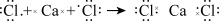 |
| B.HClO的结构式为H—Cl—O |
| C.NH4Cl中既有离子键,又有共价键,属于离子化合物 |
| D.HF、HCl、HBr、HI的沸点依次增大 |
您最近一年使用:0次
2022-02-20更新
|
195次组卷
|
2卷引用:浙江省桐乡市高级中学2021-2022学年高一12月阶段教学质量检测化学试题
名校
解题方法
6 . 化学与生活息息相关,下列说法不正确 的是
| A.在周期表的过渡元素区域可寻找各种半导体材料 |
| B.Al(OH)3是两性氢氧化物,可用于治疗胃酸过多 |
| C.氯气是重要的化工原料,可用于制造农药 |
| D.冰会浮在水面上与氢键有关 |
您最近一年使用:0次
名校
7 . 回答下列问题:
(1)CO2能与OH-结合生成HCO ,试写出HCO
,试写出HCO 的电子式
的电子式___ 。
(2)硼酸分子结构简式为B(OH)3,其晶体结构与石墨相似,为层型片状结构。其在冷水中的溶解度很小,在热水中的溶解度较大,原因是:___ 。
(1)CO2能与OH-结合生成HCO
 ,试写出HCO
,试写出HCO 的电子式
的电子式(2)硼酸分子结构简式为B(OH)3,其晶体结构与石墨相似,为层型片状结构。其在冷水中的溶解度很小,在热水中的溶解度较大,原因是:
您最近一年使用:0次
名校
8 . 对尼古丁和苯并芘的性质推测可能错误的是
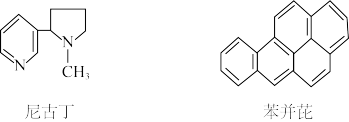

| A.尼古丁分子中的氮原子能与水中H+结合形成配位键,其水溶液可能呈碱性 |
| B.尼古丁可能既溶于水又溶于有机溶剂,苯并芘只溶于有机溶剂而不溶于水 |
| C.两者固态都属分子晶体,尼古丁分子间存在氢键,熔沸点较高 |
| D.尼古丁分子中的所有碳原子可能不在同一平面,苯并芘分子中的所有氢原子都在同一平面上 |
您最近一年使用:0次
名校
9 . 下列说法正确的是
A. 很稳定,与水分子间存在氢键有关 很稳定,与水分子间存在氢键有关 |
| B.HCl中,每个原子的最外层都具有8电子稳定结构 |
| C.熔融状态下能导电的物质一定是离子化合物 |
| D.NaOH溶于水的过程,破坏了离子键 |
您最近一年使用:0次
2021-12-28更新
|
119次组卷
|
3卷引用:浙江省精诚联盟2021-2022学年高一上学期12月普通高中学考适应性测试化学试题
名校
10 . 请回答以下问题:
(1)NH3BH3分子中,与N原子相连的H呈正电性(Hδ+),与B原子相连的H呈负电性(Hδ-),而与其原子总数相等的等电子体CH3CH3相比,NH3BH3熔点比CH3CH3高,其原因是__ 。
(2)已知高温下,冰晶石密度为2.1g/cm3,铝单质的密度为2.3g/cm3,工业上电解法制单质铝的过程中,冰晶石起到哪些作用__ 。
(1)NH3BH3分子中,与N原子相连的H呈正电性(Hδ+),与B原子相连的H呈负电性(Hδ-),而与其原子总数相等的等电子体CH3CH3相比,NH3BH3熔点比CH3CH3高,其原因是
(2)已知高温下,冰晶石密度为2.1g/cm3,铝单质的密度为2.3g/cm3,工业上电解法制单质铝的过程中,冰晶石起到哪些作用
您最近一年使用:0次



