名校
1 . 2018年7月5日《科学》杂志在线报道:合成一种新的具有超高热导率半导体材料——砷化硼(BAs)。通过反应4BI3(g) + As4(g) 4BAs(s,晶体) + 6I2(g)可制备BAs晶体。下列说法错误的是
4BAs(s,晶体) + 6I2(g)可制备BAs晶体。下列说法错误的是

 4BAs(s,晶体) + 6I2(g)可制备BAs晶体。下列说法错误的是
4BAs(s,晶体) + 6I2(g)可制备BAs晶体。下列说法错误的是
| A.图(a)表示As4结构,As4分子中成键电子对与孤电子对数目之比为3:1 |
| B.图(b)表示晶态单质硼的B12基本结构单元,该基本单元为正20面体 |
| C.图(b)所示晶态单质硼的熔点为2180℃,它属于原子晶体 |
| D.图(c)表示BAs晶胞结构,As原子的配位数为4 |
您最近一年使用:0次
2019-06-09更新
|
231次组卷
|
5卷引用:海南省儋州市第二中学2020-2021学年高二下学期3月月考化学试题
真题
名校
2 . 下列说法中错误的是:
| A.SO2、SO3都是极性分子 |
| B.在NH4+和[Cu(NH3)4]2+中都存在配位键 |
| C.元素电负性越大的原子,吸引电子的能力越强 |
| D.原子晶体中原子以共价键结合,具有键能大、熔点高、硬度大的特性 |
您最近一年使用:0次
2019-01-30更新
|
1427次组卷
|
20卷引用:2009年普通高等学校招生统一考试化学试题(海南卷)
2009年普通高等学校招生统一考试化学试题(海南卷)(已下线)吉林一中2009--2010学年度下学期期末考试第一次质量检测高二化学试卷(已下线)09—10年哈三中高二下学期期末考试化学卷(已下线)2011-2012年黑龙江龙东地区高二下学期期末考试化学试卷(已下线)2012-2013学年福建省福州文博中学高二上学期期末考试化学试卷(已下线)2014届高考化学二轮复习提分训练专题12物质结构与性质(选修)练习卷2014-2015学年山东省沂源县第一中高二下学期阶段性检测化学试卷2015-2016学年四川省成都市新都一中高二下4月月考化学试卷2016-2017学年宁夏银川市第二中学高二下学期第一次月考化学试卷江苏省射阳县盘湾中学、陈洋中学2017-2018学年高二上学期期末考试化学试题2016-2017学年高中化学选修3(人教版)模块综合测评【全国校级联考】福建省福州市八县(市)协作校2017-2018学年高二下学期期末联考化学试题新疆阿瓦提县多浪乡中学2019届高三第三次模拟考试理科综合化学试题2020年安徽省全省教学质量检测统一考试(练习检测一)四川省威远县龙会中学2019-2020学年高二12月月考化学试题湖北省武汉市黄陂区第六中学2019-2020学年高二下学期三月线上考试化学试题安徽省亳州市涡阳县第九中学2019-2020学年高二7月月考化学试题辽宁省大连市普兰店市第三十八中学2021届高三第一学期开学考试化学试题广东省惠州市第一中学2022-2023学年高二下学期3月月考化学试题河南省焦作市2022-2023学年第四中学高二下学期期中考试 化学试卷
真题
3 . NA代表阿伏伽德罗常数的值,下列说法正确的是
| A.12 g金刚石中含有化学键的数目为4NA |
| B.18 g的D2O中含有的质子数为10 |
| C.28 g的乙烯和环己烷混合气体中所含原子总数为6NA |
| D.1 L 1mol·L¯1的NH4Cl溶液中NH4+和Cl―的数目均为1NA |
您最近一年使用:0次
2018-11-28更新
|
3833次组卷
|
10卷引用:2018年普通高等学校招生全国统一考试化学(海南卷)
2018年普通高等学校招生全国统一考试化学(海南卷)辽宁省阜新市第二高级中学2018-2019学年高二下学期期末考试化学试题(已下线)专题1.1 物质的量 气体摩尔体积(练)-《2020年高考一轮复习讲练测》(已下线)专题三 化学常用计量与阿伏加德罗常数(真题汇编)-2020年高考二轮模块化复习之《化学基本概念》名师讲案与提分特训(已下线)小题必刷09 物质的量、气体摩尔体积——2021年高考化学一轮复习小题必刷(通用版)河南省开封市2019-2020学年高二下学期期末调研考试化学试题(已下线)小题必刷21 原子结构与化学键——2021年高考化学一轮复习小题必刷(通用版)(已下线)小题04 阿伏加德罗常数NA(根据陷阱类型分类)——备战2021年高考化学经典小题考前必刷(全国通用)(已下线)第二单元 化学物质及其变化(B卷 真题滚动练)-2022年高考化学一轮复习单元滚动双测卷(新高考地区专用)安徽省砀山县第四中学2022-2023学年高三上学期第一次月考化学试题
4 . 共价键、离子键和范德华力是构成物质粒子间的不同作用方式,下列物质中,只含有上述一种作用的是___________
| A.金刚石 | B.氯化钠 | C.氢氧化钠 | D.碘 |
您最近一年使用:0次
解题方法
5 . 下列数据是对应物质的熔点,有关的判断错误的是( )
A.只要含有金属阳离子的晶体就一定是离子晶体
B.在共价化合物中各原子都形成8电子结构
C.同族元素的氧化物可形成不同类型的晶体
D.金属晶体的熔点不一定比分子晶体的高
19-II如图为几种晶体或晶胞的构型示意图。
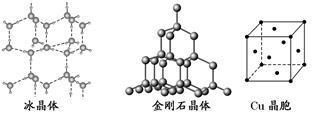

请回答下列问题:
(1)这些晶体中,粒子之间以共价键结合形成的晶体是____________ 。
(2)冰、金刚石、MgO、CaCl2、干冰5种晶体的熔点由高到低的顺序为_________________ 。
(3)NaCl晶胞与MgO晶胞相同,NaCl晶体的晶格能________ (填“大于”或“小于”)MgO晶体的晶格能,原因是_______________ 。
(4)每个铜晶胞中实际占有________ 个铜原子,CaCl2晶体中Ca2+的配位数为________ 。
(5)冰的熔点远高于干冰,除因为H2O是极性分子、CO2是非极性分子外,还有一个重要的原因是_________ 。
| Na2O | Na | AlF3 | AlCl3 | Al2O3 | BCl3 | CO2 | SiO2 |
| 920 ℃ | 97.8 ℃ | 1291 ℃ | 190 ℃ | 2073 ℃ | -107 ℃ | -57 ℃ | 1723 ℃ |
A.只要含有金属阳离子的晶体就一定是离子晶体
B.在共价化合物中各原子都形成8电子结构
C.同族元素的氧化物可形成不同类型的晶体
D.金属晶体的熔点不一定比分子晶体的高
19-II如图为几种晶体或晶胞的构型示意图。


请回答下列问题:
(1)这些晶体中,粒子之间以共价键结合形成的晶体是
(2)冰、金刚石、MgO、CaCl2、干冰5种晶体的熔点由高到低的顺序为
(3)NaCl晶胞与MgO晶胞相同,NaCl晶体的晶格能
(4)每个铜晶胞中实际占有
(5)冰的熔点远高于干冰,除因为H2O是极性分子、CO2是非极性分子外,还有一个重要的原因是
您最近一年使用:0次



