解题方法
1 . 能够解释CO2比SiO2的熔、沸点低的原因是
| A.C—O键能大于Si—O键能 |
| B.C—O键能小于Si—O键能 |
| C.破坏CO2晶体只需克服分子间作用力,破坏SiO2晶体要破坏Si—O共价键 |
| D.以上说法均不对 |
您最近一年使用:0次
2 . 航天飞机表层的防热瓦曾成为航天飞机能否安全着陆的制约因素,防热瓦是以石墨材料为主要成分的十分疏松的泡沫陶瓷。下列有关说法合理的是
| A.石墨成为该泡沫陶瓷主要成分的主要原因是石墨是共价晶体 |
| B.石墨成为该泡沫陶瓷主要成分的主要原因是石墨熔点很高 |
| C.石墨中碳碳键之间的夹角是109°28′ |
| D.C60也可代替石墨用作航天飞机表层的防热瓦材料 |
您最近一年使用:0次
3 . 共价晶体
| 概念 | 共价晶体是原子之间以 | |
| 构成粒子 | ||
| 微粒间的作用 | ||
| 物理性质 | 熔、沸点 | |
| 常见共价晶体 | 金刚石、单晶硅、碳化硅(SiC)、二氧化硅(SiO2)等。 | |
| 典型共价晶体 | 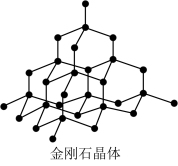 每个C原子形成4个C-C键,构成正四面体形成空间网状结构,其中n(C):n(C-C)=1:2 | 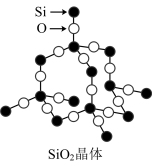 每个Si形成4个Si-O键,每个O形成2个O-Si键,向空间伸展形成网状结构,不存在单个分子,Si与O个数比为1:2,SiO2为化学式 |
您最近一年使用:0次
4 . 有关原子晶体的叙述,错误的是
| A.原子晶体中,原子不遵循紧密堆积原则 | B.原子晶体中不存在独立的分子 |
| C.原子晶体的熔点和硬度较高 | D.原子晶体熔化时不破坏化学键 |
您最近一年使用:0次
2022-05-11更新
|
567次组卷
|
5卷引用:3.3.2共价晶体 课前
3.3.2共价晶体 课前(已下线)第43练 分子晶体与共价晶体-2023年高考化学一轮复习小题多维练(全国通用)新疆乌苏市第一中学2021-2022学年高二下学期期中考试化学试题第二节 分子晶体与共价晶体 第2课时 共价晶体云南迪庆藏族自治州民族中学2022-2023学年高二下学期期末考试化学试题
5 . 常见晶体的结构分析
(1)金刚石晶体



①在晶体中每个碳原子以_______ 个共价单键与相邻的_______ 个碳原子相结合,成为正四面体。
②晶体中C-C-C夹角为_______ ,碳原子采取了_______ 杂化。
③最小环上有_______ 个碳原子。
④晶体中碳原子个数与C-C键数之比为_______ 。
⑤在一个晶胞中,碳原子位于立方体的8个顶点、6个面心以及晶胞内部,由“均摊法”可求出该晶胞中实际含有的碳原子数为_______ 。
(2)二氧化硅晶体

①每个硅原子与相邻的_______ 个氧原子以共价键相结合构成_______ 结构,硅原子在正四面体的中心,4个氧原子在正四面体的4个顶点。晶体中Si原子与O原子个数比为_______ 。
②每个Si原子与4个O原子成键,每个O原子与_______ 个Si原子成键,最小的环是_______ 元环。
③每个最小的环实际拥有的硅原子为_______ ,氧原子数为_______ 。
④1molSiO2晶体中含Si-O键数目为_______ ,在SiO2晶体中Si、O原子均采取_______ 杂化。
⑤SiO2具有许多重要用途,是制造水泥、玻璃、人造红宝石、单晶硅、硅光电池、芯片和光导纤维的原料。
(1)金刚石晶体



①在晶体中每个碳原子以
②晶体中C-C-C夹角为
③最小环上有
④晶体中碳原子个数与C-C键数之比为
⑤在一个晶胞中,碳原子位于立方体的8个顶点、6个面心以及晶胞内部,由“均摊法”可求出该晶胞中实际含有的碳原子数为
(2)二氧化硅晶体

①每个硅原子与相邻的
②每个Si原子与4个O原子成键,每个O原子与
③每个最小的环实际拥有的硅原子为
④1molSiO2晶体中含Si-O键数目为
⑤SiO2具有许多重要用途,是制造水泥、玻璃、人造红宝石、单晶硅、硅光电池、芯片和光导纤维的原料。
您最近一年使用:0次
6 . 观察对比晶体硅、碳化硅、二氧化硅的晶胞,并总结结构特征。_______ 。


您最近一年使用:0次
7 . 怎么从原子结构的角度理解金刚石、硅 、锗的熔点和硬度依次下降?_______ 。
您最近一年使用:0次
8 . “具有共价键的晶体叫做共价晶体”这种说法对吗?为什么?_______ 。
您最近一年使用:0次
9 . 分类:_______ 、_______ 、_______
您最近一年使用:0次
10 . 组成微粒:_______
您最近一年使用:0次



