1 . 元素的“价一类”二维图是我们学习元素及其化合物相关知识的重要模型和工具,它指的是以元素的化合价为纵坐标,以物质的类别为横坐标所绘制的二维平面图像。如图为铁元素的“价一类”二维图,箭头表示部分物质间的转化关系。
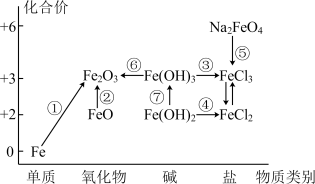
请回答一下问题:
(1) 中
中 的化合价为
的化合价为_______ 。
(2) 是否为碱性氧化物
是否为碱性氧化物_______ (填是或否),理由:_______ 。
(3)制备氢氧化亚铁时,现象由白色絮状沉淀最终转化为红褐色沉淀,请用化学方程式解释现象:_______ 。其中检验溶液中 的试剂是
的试剂是_______ 。
(4)电子工业常用 的
的 溶液腐蚀敷在绝缘板上的铜箔,从而制造印刷电路板,写出此过程的离子方程式
溶液腐蚀敷在绝缘板上的铜箔,从而制造印刷电路板,写出此过程的离子方程式_______ ;印刷电路板的废液中加入一定量铁粉,充分反应后,准备过滤并收集滤渣。此时,滤渣的成分不可能是_______ 。
aA.没有滤渣 B.有 也有
也有 C.只有
C.只有 D.只有
D.只有

请回答一下问题:
(1)
 中
中 的化合价为
的化合价为(2)
 是否为碱性氧化物
是否为碱性氧化物(3)制备氢氧化亚铁时,现象由白色絮状沉淀最终转化为红褐色沉淀,请用化学方程式解释现象:
 的试剂是
的试剂是(4)电子工业常用
 的
的 溶液腐蚀敷在绝缘板上的铜箔,从而制造印刷电路板,写出此过程的离子方程式
溶液腐蚀敷在绝缘板上的铜箔,从而制造印刷电路板,写出此过程的离子方程式aA.没有滤渣 B.有
 也有
也有 C.只有
C.只有 D.只有
D.只有
您最近一年使用:0次
2 . 航天员王亚平在“天宫课堂”中介绍了空间站中的生活,在轨演示了水球变气球等一系列炫酷又好玩的实验。
I.“天宫”中水和氧气的最大化利用是保障生活的重要措施。如图是空间站常用资源再利用模拟图。
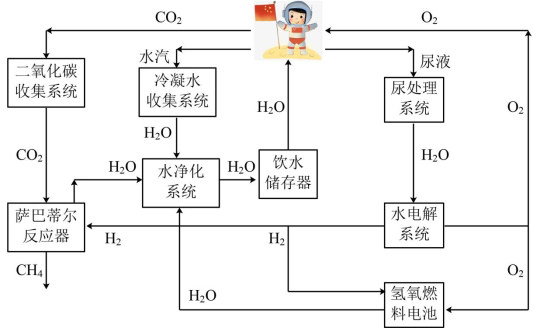
(1)“尿处理子系统”采用蒸馏方法对其中成分进行分离。此方法是根据尿液中各成分的____ 不同进行分离的。
(2)“水电解系统”中产生氧气的电极应接电池的____ 极(填“正”或“负”)。发生反应的化学方程式为____ 。
(3)在水净化系统中,用臭氧(O3)消毒,臭氧在一定条件下转化为氧气的化学方程式为____ 。
(4)在一定条件下,“萨巴蒂尔反应器”可以除去CO2,该反应的化学方程式为____ 。
II.王亚平将蓝色颜料注入水球中,整个水球变成蓝色,将泡腾片放入水球中,产生大量气泡向四面八方扩散,充满整个水球。气体并不溢出,使水球越来越大。
(5)泡腾片在水中发生了如下反应:H3C6H5O7+3NaHCO3=Na3C6H5O7+3H2O+3____ (补全化学方程式)。
(6)如果在空间站失重状态下收集制得的氧气,可以选用下列装置中的____ (填序号)。
I.“天宫”中水和氧气的最大化利用是保障生活的重要措施。如图是空间站常用资源再利用模拟图。

(1)“尿处理子系统”采用蒸馏方法对其中成分进行分离。此方法是根据尿液中各成分的
(2)“水电解系统”中产生氧气的电极应接电池的
(3)在水净化系统中,用臭氧(O3)消毒,臭氧在一定条件下转化为氧气的化学方程式为
(4)在一定条件下,“萨巴蒂尔反应器”可以除去CO2,该反应的化学方程式为
II.王亚平将蓝色颜料注入水球中,整个水球变成蓝色,将泡腾片放入水球中,产生大量气泡向四面八方扩散,充满整个水球。气体并不溢出,使水球越来越大。
(5)泡腾片在水中发生了如下反应:H3C6H5O7+3NaHCO3=Na3C6H5O7+3H2O+3
(6)如果在空间站失重状态下收集制得的氧气,可以选用下列装置中的
A. | B.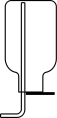 | C.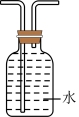 | D. |
您最近一年使用:0次
2022-08-22更新
|
375次组卷
|
3卷引用:福建省龙岩第一中学2022-2023学年高一上学期开学考试化学试题
名校
3 . 选择下列实验方法分离提纯物质,将分离提纯方法的字母序号填在横线上。
A.萃取分液 B.升华 C.重结晶 D.分液 E.蒸馏 F.过滤 G.洗气
(1)____ 分离氯化钾与固体碘的混合物。
(2)____ 提纯含有泥沙的苯甲酸固体。
(3)____ 分离水和CCl4的混合物。
(4)____ 分离石油中的各组分。
(5)____ 除去混在甲烷中的乙烯。
(6)____ 提取溴水中的溴。
A.萃取分液 B.升华 C.重结晶 D.分液 E.蒸馏 F.过滤 G.洗气
(1)
(2)
(3)
(4)
(5)
(6)
您最近一年使用:0次
4 . 海洋是一个巨大的宝藏,海水淡化是重要的化学研究课题。
(1)蒸馏法获取淡水,历史悠久,操作简单,图中符合模拟蒸馏海水的装置是___ (填序号)。
a.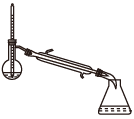 b.
b.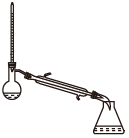
c.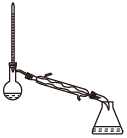 d.
d.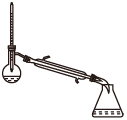
蒸馏前,应向烧瓶中加入沸石或碎瓷片,目的是___ ,冷凝水一般不采用“上进下出”,其原因是____ 。
(2)电渗析法的技术原理如图(两端为惰性电极,阳膜只允许阳离子通过,阴膜只允许阴离子通过):
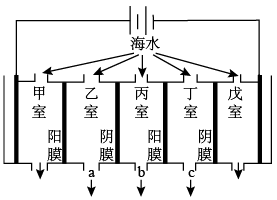
某地海水中主要含Na+、K+、Ca2+、Mg2+、Cl-、HCO 、SO
、SO 等,则淡化过程中,甲室的电极反应式为
等,则淡化过程中,甲室的电极反应式为___ ,产生水垢最多的是___ 室,淡水的出口为____ (填“a”、“b”或“c”)。
(3)离子交换法获取淡水模拟图如图:

经过阳离子交换树脂后水中阳离子数目____ (填“增加”“不变”或“减少”),阴离子交换树脂中发生了离子反应,其离子方程式为___ 。
(1)蒸馏法获取淡水,历史悠久,操作简单,图中符合模拟蒸馏海水的装置是
a.
 b.
b.
c.
 d.
d.
蒸馏前,应向烧瓶中加入沸石或碎瓷片,目的是
(2)电渗析法的技术原理如图(两端为惰性电极,阳膜只允许阳离子通过,阴膜只允许阴离子通过):

某地海水中主要含Na+、K+、Ca2+、Mg2+、Cl-、HCO
 、SO
、SO 等,则淡化过程中,甲室的电极反应式为
等,则淡化过程中,甲室的电极反应式为(3)离子交换法获取淡水模拟图如图:

经过阳离子交换树脂后水中阳离子数目
您最近一年使用:0次
2021-09-06更新
|
1253次组卷
|
5卷引用:安徽省A10联盟2022届高三上学期摸底考试化学试题
安徽省A10联盟2022届高三上学期摸底考试化学试题(已下线)3.3.1 粗盐提纯 从海水中提取溴-2021-2022学年高一化学课后培优练(苏教版2019必修第一册)(已下线)专题35 物质的检验、分离和提纯(限时精炼)-2022年高三毕业班化学常考点归纳与变式演练(已下线)第八章 化学与可持续发展(B卷·能力提升练)-【单元测试】2022-2023学年高一化学分层训练AB卷(人教版2019必修第二册)(已下线)第八章 化学与可持续发展【单元测试B卷】
名校
5 . 现代工业常以氯化钠为原料制备纯碱,部分工艺流程如下:

已知反应I为:NaCl+CO2+NH3+H2O NaHCO3↓+NH4Cl
NaHCO3↓+NH4Cl
(1)海水中含有大量的NaCl,以及少量的Ca2+、Mg2+、SO 等离子。为得到纯净的饱和NaCl溶液,进行了如下操作。请补全操作步骤:
等离子。为得到纯净的饱和NaCl溶液,进行了如下操作。请补全操作步骤:
a.向浓缩后的海水中加入过量的氢氧化钠溶液后,过滤;
b.向滤液中___________ ,过滤;
c.向滤液中___________ ,过滤;
d.向滤液中加入足量的稀盐酸;
e.加热煮沸一段时间,得到饱和NaCl溶液。
(2)反应II的化学方程式是___________ 。
(3)制得的纯碱中含有少量NaCl。取5.5g纯碱样品加入足量稀硫酸,得到标准状况下1120mLCO2.则样品中纯碱的质量分数是___________ %(保留1位小数)。

已知反应I为:NaCl+CO2+NH3+H2O
 NaHCO3↓+NH4Cl
NaHCO3↓+NH4Cl(1)海水中含有大量的NaCl,以及少量的Ca2+、Mg2+、SO
 等离子。为得到纯净的饱和NaCl溶液,进行了如下操作。请补全操作步骤:
等离子。为得到纯净的饱和NaCl溶液,进行了如下操作。请补全操作步骤:a.向浓缩后的海水中加入过量的氢氧化钠溶液后,过滤;
b.向滤液中
c.向滤液中
d.向滤液中加入足量的稀盐酸;
e.加热煮沸一段时间,得到饱和NaCl溶液。
(2)反应II的化学方程式是
(3)制得的纯碱中含有少量NaCl。取5.5g纯碱样品加入足量稀硫酸,得到标准状况下1120mLCO2.则样品中纯碱的质量分数是
您最近一年使用:0次
名校
解题方法
6 . 现有 NaCl、Na2SO4和 NaNO3 的混合物,选择适当的试剂除去杂质,从而得到纯净的NaNO3晶体,相应的实验流程如图所示。

(1)写出实验流程中下列物质的化学式:试剂 X___________ ,沉淀 A_________ 。
(2)上述实验流程中①②③步均要进行的实验操作是______________ (填操作名称),该过程中玻璃棒的作用是___________ 。
(3)上述实验流程中加入过量 Na2CO3 溶液的目的是_____________ 。
(4)按此实验方案得到的溶液3中肯定含有_________________ (填化学式)杂质。为了解决这个问题,可以向溶液3中加入适量的_________________ (填化学式)。

(1)写出实验流程中下列物质的化学式:试剂 X
(2)上述实验流程中①②③步均要进行的实验操作是
(3)上述实验流程中加入过量 Na2CO3 溶液的目的是
(4)按此实验方案得到的溶液3中肯定含有
您最近一年使用:0次
2020-06-12更新
|
1360次组卷
|
8卷引用:河北省沧州市盐山中学2023-2024学年高一下学期开学化学试题
河北省沧州市盐山中学2023-2024学年高一下学期开学化学试题江苏省江都中学2019-2020学年度高一期中考试化学试题(已下线)第二章 化学物质及其变化(基础过关)-2020-2021学年高一化学单元测试定心卷(人教版必修1)(已下线)第一章 物质及其变化(能力提升)-2020-2021学年高一化学单元测试定心卷(人教版2019必修第一册)安徽省六安市新安中学2022届高三上学期第二次月考化学试题(已下线)【苏州新东方】13 吴江区 高级中学江苏省宿迁市泗阳县实验高级中学2022-2023学年高一上学期第一次调研测试化学试题(已下线)第一章 化学物质及其变化 第3练 离子反应的应用
名校
7 . 食盐是人类生活中不可缺少的物质,海水中含有大量食盐。某地出产的粗盐中,所含杂质是CaCl2,通过下面的实验可制得纯净的NaCl。
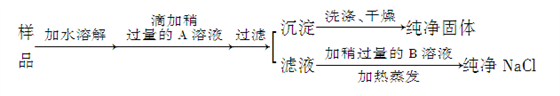
请回答:
(1)加入的A是__________ ,检验A已过量的方法是___________ 。
(2)加入的B是__________ ,加入稍过量B的目的是__________ 。
(3)为检验沉淀是否洗净,最好在最后几滴洗出液中加入_________________ 溶液。

请回答:
(1)加入的A是
(2)加入的B是
(3)为检验沉淀是否洗净,最好在最后几滴洗出液中加入
您最近一年使用:0次
2017-09-13更新
|
853次组卷
|
7卷引用:河南省周口市中英文学校2018届高三上学期开学摸底考试化学试题
河南省周口市中英文学校2018届高三上学期开学摸底考试化学试题江西省南昌市第十中学2019-2020学年高一上学期期中考试化学试题吉林省公主岭市范家屯镇第一中学2019-2020学年高一上学期期末考试化学试题人教版2019必修第二册 第五章 第一节 第2课时 硫酸 硫酸根离子的检验山西省晋中市寿阳县第一中学2019—2020学年高一上学期第二次月考化学试题内蒙古包头市一机一中2021-2022学年高一上学期10月月考化学试题(已下线)第03讲 硫酸根离子的检验 含硫物质的转化(word讲义)-【帮课堂】2021-2022学年高一化学同步精品讲义(人教版2019必修第二册)
名校
8 . 某研究所对含硫酸亚铁和硫酸铜的工业废料进行相关的研究。实验过程如下:
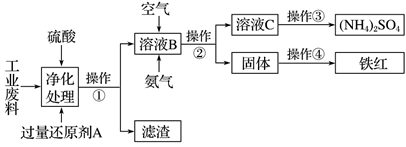
回答下列问题:
(1)滤渣的成分为________ ,操作②的名称为_____________________ 。
(2)上图溶液B中所发生反应的离子方程式为____________________________ 。
(3)实验要求先向溶液B中通入过量的空气,证明通入空气过量的方法是____________________________________________________ 。
(4)操作③第一步需要的仪器除了酒精灯、铁架台外,还需要_______________ 。
(5)某同学利用下面装置制备氢气并利用氢气还原某金属氧化物,根据要求回答问题。
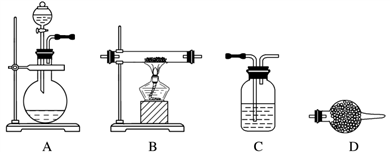
①请设计一个实验方案验证H2的还原性并检验其氧化产物,其装置连接顺序是A→________ →________ →________ →D(除D装置外,其他装置不能重复使用),最后D装置中所加药品为____________ ,其作用是________________________ 。
②点燃B处酒精灯之前必须进行的操作是____________________________ 。

回答下列问题:
(1)滤渣的成分为
(2)上图溶液B中所发生反应的离子方程式为
(3)实验要求先向溶液B中通入过量的空气,证明通入空气过量的方法是
(4)操作③第一步需要的仪器除了酒精灯、铁架台外,还需要
(5)某同学利用下面装置制备氢气并利用氢气还原某金属氧化物,根据要求回答问题。

①请设计一个实验方案验证H2的还原性并检验其氧化产物,其装置连接顺序是A→
②点燃B处酒精灯之前必须进行的操作是
您最近一年使用:0次
2017-06-27更新
|
1317次组卷
|
3卷引用:黑龙江省哈尔滨师范大学青冈实验中学校2020届高三上学期开学考试(8月)化学试题
9-10高一下·广东·期末
名校
9 . 海水是巨大的资源宝库,从海水中提取食盐和溴的过程如下:
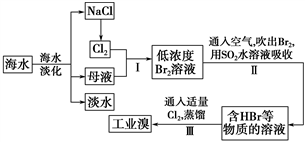
(1)请列举海水淡化的两种方法:________ 、________ 。
(2)步骤Ⅰ中已获得Br2,步骤Ⅱ中又将Br2还原为Br-,其目的是_________ 。
(3)步骤Ⅱ用SO2水溶液吸收Br2,吸收率可达95%,有关反应的离子方程式为_______ ,由此反应可知,除环境保护外,在工业生产中应解决的主要问题是_______ 。
(4)某化学研究性学习小组为了了解从工业溴中提纯溴的方法,查阅了有关资料知:Br2的沸点为59 ℃,微溶于水,有毒并有强腐蚀性。他们参观生产过程后,画了如下装置简图:

请你参与分析讨论:
①图中仪器B的名称是____________ 。
②整套实验装置中仪器连接均不能用橡胶塞和橡胶管,其原因是__________ 。
③实验装置气密性良好,要达到提纯溴的目的,操作中如何控制关键条件?___________ 。
④C中液体颜色为________________ 。为除去该产物中仍残留的少量Cl2,可向其中加入NaBr溶液,充分反应后,再进行的分离操作是________________ 。

(1)请列举海水淡化的两种方法:
(2)步骤Ⅰ中已获得Br2,步骤Ⅱ中又将Br2还原为Br-,其目的是
(3)步骤Ⅱ用SO2水溶液吸收Br2,吸收率可达95%,有关反应的离子方程式为
(4)某化学研究性学习小组为了了解从工业溴中提纯溴的方法,查阅了有关资料知:Br2的沸点为59 ℃,微溶于水,有毒并有强腐蚀性。他们参观生产过程后,画了如下装置简图:

请你参与分析讨论:
①图中仪器B的名称是
②整套实验装置中仪器连接均不能用橡胶塞和橡胶管,其原因是
③实验装置气密性良好,要达到提纯溴的目的,操作中如何控制关键条件?
④C中液体颜色为
您最近一年使用:0次
2016-09-06更新
|
1236次组卷
|
13卷引用:江西省九江市第一中学2017-2018学年高二上学期开学考试化学试题
江西省九江市第一中学2017-2018学年高二上学期开学考试化学试题云南省河口县一中2019-2020学年高二上学期开学考试化学试题云南省勐腊县一中2019-2020学年高二上学期开学考试化学试题江西省赣县第三中学2021-2022学年高二上学期入学考试化学试题(已下线)09—10年梅县东山中学高一下学期期末考试化学卷(已下线)2014年高一化学人教版必修2 4章化学与自然资源的开发利用练习卷2015-2016学年贵州省凯里一中高一下质检化学试卷2016-2017学年河北省邢台市第一中学高一下学期第二次月考化学试卷内蒙古北京八中乌兰察布分校2016-2017学年高一下学期期中考试化学试题福建省闽侯第六中学2017-2018学年高二上学期第一次月考化学试题人教版高中化学必修2第四章《化学与自然资源的开发利用》测试卷1人教版高中化学必修二第四章《化学与自然资源的开发利用》测试卷辽宁省营口市第二高级中学2020届高三上学期第一次月考化学试题



