名校
1 . 我国是世界产盐大国,海盐、湖盐和井盐的总产量居世界第二位。某同学进行粗盐的提纯并配制溶液、检验纯度实验。
(一)粗盐的提纯
(1)粗盐中含有泥沙、Ca2+、Mg2+、SO 杂质,请选择合适的操作补全实验流程。
杂质,请选择合适的操作补全实验流程。_______
将粗盐溶解→加入NaOH溶液→___________→___________→___________→___________→结晶得到精盐
加入稀盐酸 B.加入稀硫酸 C.过滤 D.加入BaCl2溶液 E.加入Na2CO3溶液
(2)以上流程中加酸的目的是(用离子方程式表示)___________
(二)一定浓度溶液的配制:用制得的精盐配制100 mL 1.00 mol/L NaCl溶液
(3)实验中用到的玻璃仪器,除了烧杯、量筒、胶头滴管外,还需要___________
(4)定容时的操作:当液面离容量瓶刻度线1~2cm时,___________ ,再将容量瓶塞盖好,反复上下颠倒,摇匀。
(5)下列操作会使配得的NaCl溶液浓度偏低的是___________。
(三)纯度测定
取25.00mL所配溶液于锥形瓶中,加入几滴K2CrO4溶液(指示反应终点),在不断摇动下,滴加1.00mol/L AgNO3溶液反应。平行测试3次,平均消耗AgNO3溶液23.50mL。
(6)制得的NaCl的纯度是___________ 。
(一)粗盐的提纯
(1)粗盐中含有泥沙、Ca2+、Mg2+、SO
 杂质,请选择合适的操作补全实验流程。
杂质,请选择合适的操作补全实验流程。将粗盐溶解→加入NaOH溶液→___________→___________→___________→___________→结晶得到精盐
加入稀盐酸 B.加入稀硫酸 C.过滤 D.加入BaCl2溶液 E.加入Na2CO3溶液
(2)以上流程中加酸的目的是(用离子方程式表示)
(二)一定浓度溶液的配制:用制得的精盐配制100 mL 1.00 mol/L NaCl溶液
(3)实验中用到的玻璃仪器,除了烧杯、量筒、胶头滴管外,还需要
(4)定容时的操作:当液面离容量瓶刻度线1~2cm时,
(5)下列操作会使配得的NaCl溶液浓度偏低的是___________。
| A.没有进行洗涤操作 |
| B.定容时俯视容量瓶的刻度线 |
| C.摇匀后发现液面低于容量瓶刻度线,再滴加蒸馏水至刻度线 |
| D.转移洗涤液时洒到容量瓶外,继续用该未清洗的容量瓶重新配制 |
(三)纯度测定
取25.00mL所配溶液于锥形瓶中,加入几滴K2CrO4溶液(指示反应终点),在不断摇动下,滴加1.00mol/L AgNO3溶液反应。平行测试3次,平均消耗AgNO3溶液23.50mL。
(6)制得的NaCl的纯度是
您最近一年使用:0次
2023-11-17更新
|
173次组卷
|
5卷引用:北京市首都师范大学附属中学2023-2024学年高一下学期开学化学试题
名校
解题方法
2 . 完成下列问题。
(1)下列做法中,符合“低碳”理念的是________ (填字母序号)
A.开发使用新能源汽车 B.“焚烧法”处理垃圾 C.大力发展火力发电
D.使用太阳能热水器 E.大力发展风力发电
(2)幼儿和青少年缺___________ 会患佝偻病和发育不良。
(3)如图是A、B、C三种物质的溶解度曲线图。请回答:

①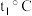 时,溶解度相等的两种物质是
时,溶解度相等的两种物质是________ 。
②B的饱和溶液中混有少量的物质A,要除去A得到较纯的B物质,可采用的结晶方法是___________ 。
③如图所示,在大烧杯中加入一定量的硝酸铵固体后,甲试管内出现的现象是___________ ,乙试管内的溶液为___________ (填“饱和”或“不饱和”)溶液。

(1)下列做法中,符合“低碳”理念的是
A.开发使用新能源汽车 B.“焚烧法”处理垃圾 C.大力发展火力发电
D.使用太阳能热水器 E.大力发展风力发电
(2)幼儿和青少年缺
(3)如图是A、B、C三种物质的溶解度曲线图。请回答:

①
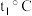 时,溶解度相等的两种物质是
时,溶解度相等的两种物质是②B的饱和溶液中混有少量的物质A,要除去A得到较纯的B物质,可采用的结晶方法是
③如图所示,在大烧杯中加入一定量的硝酸铵固体后,甲试管内出现的现象是

您最近一年使用:0次
解题方法
3 . 早在战国时期,《周礼·考工记》就记载了我国劳动人民制取氢氧化钾以漂洗丝帛的工艺。大意是:先将干燥的木头烧成灰(含 ),用其灰汁浸泡丝帛,再加入石灰即可。其反应过程如图。
),用其灰汁浸泡丝帛,再加入石灰即可。其反应过程如图。

(1)操作a要用到的玻璃仪器有烧杯、玻璃棒和________ 。
(2)反应过程中未涉及的基本反应类型是________ 。
(3)反应过程中能够循环利用的物质是________ (填化学式)。
(4)氢氧化钙与灰汁(含 )反应的化学方程式为
)反应的化学方程式为________ 。
(5)古人不提前制备大量氢氧化钾的原因是________ (用化学方程式表达)。
 ),用其灰汁浸泡丝帛,再加入石灰即可。其反应过程如图。
),用其灰汁浸泡丝帛,再加入石灰即可。其反应过程如图。
(1)操作a要用到的玻璃仪器有烧杯、玻璃棒和
(2)反应过程中未涉及的基本反应类型是
(3)反应过程中能够循环利用的物质是
(4)氢氧化钙与灰汁(含
 )反应的化学方程式为
)反应的化学方程式为(5)古人不提前制备大量氢氧化钾的原因是
您最近一年使用:0次
名校
解题方法
4 . 水是生命之源。
(1)自然界中的天然水通常含有许多杂质。要除去水中的不溶性杂质,可以进行___________ 操作,该操作使用的玻璃仪器有烧杯、玻璃棒和___________ 其中玻璃棒的作用是___________ ;要吸附掉一些有色有味的可溶性杂质,可以用___________ 净水。
(2)工业上和科学实验中软化硬水的方法很多,生活中通过___________ 也可以降低水的硬度。
(3)“天宫课堂”直播中宇航员告诉我们天宫中所用的氧气来自于电解水。
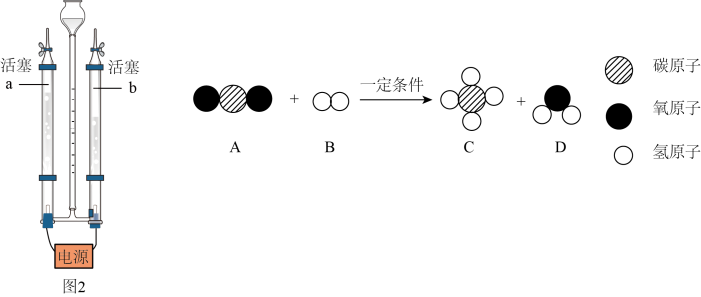
①联系到化学课上的电解水实验,如图2所示:产生 的玻璃管是
的玻璃管是___________ (填“a”或“b”),该反应的基本反应类型为___________ 。
②生成的 还可以与人呼出的
还可以与人呼出的 在一定条件下进行反应,实现了舱内物质循环利用,反应的微观过程如图所示。该反应中涉及到的氧化物有
在一定条件下进行反应,实现了舱内物质循环利用,反应的微观过程如图所示。该反应中涉及到的氧化物有___________ 种,写出C物质的化学式___________ 。
(4)爱护水资源是每个公民应尽的义务,请你写出一个防止水体污染的做法:___________ 。
(1)自然界中的天然水通常含有许多杂质。要除去水中的不溶性杂质,可以进行
(2)工业上和科学实验中软化硬水的方法很多,生活中通过
(3)“天宫课堂”直播中宇航员告诉我们天宫中所用的氧气来自于电解水。

①联系到化学课上的电解水实验,如图2所示:产生
 的玻璃管是
的玻璃管是②生成的
 还可以与人呼出的
还可以与人呼出的 在一定条件下进行反应,实现了舱内物质循环利用,反应的微观过程如图所示。该反应中涉及到的氧化物有
在一定条件下进行反应,实现了舱内物质循环利用,反应的微观过程如图所示。该反应中涉及到的氧化物有(4)爱护水资源是每个公民应尽的义务,请你写出一个防止水体污染的做法:
您最近一年使用:0次
解题方法
5 . 以盐湖锂矿(主要成分为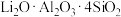 ,还含有
,还含有 及少量有机物等)为原料制备
及少量有机物等)为原料制备 的方法如下:
的方法如下:
(1)酸化:将适量盐湖锂矿粉与水混合,加入一定量浓 ,充分反应后加水稀释,过滤。酸化过程会产生少量
,充分反应后加水稀释,过滤。酸化过程会产生少量 ,原因是
,原因是___________ 。
(2)净化:
①加碱调节滤液的 至弱碱性,使
至弱碱性,使 沉淀;将再加入适量
沉淀;将再加入适量 溶液将
溶液将 转化为沉淀,过滤。
转化为沉淀,过滤。 与
与 反应的离子方程式为
反应的离子方程式为___________ 。
②调节滤液的 ,再加入适量
,再加入适量 粉末,过滤,得
粉末,过滤,得 溶液。过滤所得滤渣的主要成分是
溶液。过滤所得滤渣的主要成分是___________ 。
(3)沉锂:80℃时将饱和 溶液与饱和
溶液与饱和 溶液混合充分反应,过滤,得
溶液混合充分反应,过滤,得 晶体。“沉锂”时选择较高温度,所得
晶体。“沉锂”时选择较高温度,所得 的产率及纯度较高。原因是
的产率及纯度较高。原因是___________ 。
已知 三种物质在不同温度下的溶解度如下表:
三种物质在不同温度下的溶解度如下表:
(4) 样品纯度测定:称取
样品纯度测定:称取 样品置于锥形瓶中,加入
样品置于锥形瓶中,加入 盐酸,搅拌,充分反应(杂质不与酸反应)。再加入几滴酚酞,用
盐酸,搅拌,充分反应(杂质不与酸反应)。再加入几滴酚酞,用 溶液滴定至终点,消耗
溶液滴定至终点,消耗 溶液的体积为
溶液的体积为 。计算
。计算 样品的纯度
样品的纯度___________ (写出计算过程)。
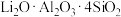 ,还含有
,还含有 及少量有机物等)为原料制备
及少量有机物等)为原料制备 的方法如下:
的方法如下:(1)酸化:将适量盐湖锂矿粉与水混合,加入一定量浓
 ,充分反应后加水稀释,过滤。酸化过程会产生少量
,充分反应后加水稀释,过滤。酸化过程会产生少量 ,原因是
,原因是(2)净化:
①加碱调节滤液的
 至弱碱性,使
至弱碱性,使 沉淀;将再加入适量
沉淀;将再加入适量 溶液将
溶液将 转化为沉淀,过滤。
转化为沉淀,过滤。 与
与 反应的离子方程式为
反应的离子方程式为②调节滤液的
 ,再加入适量
,再加入适量 粉末,过滤,得
粉末,过滤,得 溶液。过滤所得滤渣的主要成分是
溶液。过滤所得滤渣的主要成分是(3)沉锂:80℃时将饱和
 溶液与饱和
溶液与饱和 溶液混合充分反应,过滤,得
溶液混合充分反应,过滤,得 晶体。“沉锂”时选择较高温度,所得
晶体。“沉锂”时选择较高温度,所得 的产率及纯度较高。原因是
的产率及纯度较高。原因是已知
 三种物质在不同温度下的溶解度如下表:
三种物质在不同温度下的溶解度如下表:温度/℃ 物质 | 0 | 20 | 40 | 60 | 80 |
 | 7.0 | 21.5 | 49.0 | 46.0 | 43.9 |
 | 36.1 | 34.8 | 33.7 | 32.6 | 31.4 |
 | 1.54 | 1.33 | 1.17 | 1.01 | 0.85 |
 样品纯度测定:称取
样品纯度测定:称取 样品置于锥形瓶中,加入
样品置于锥形瓶中,加入 盐酸,搅拌,充分反应(杂质不与酸反应)。再加入几滴酚酞,用
盐酸,搅拌,充分反应(杂质不与酸反应)。再加入几滴酚酞,用 溶液滴定至终点,消耗
溶液滴定至终点,消耗 溶液的体积为
溶液的体积为 。计算
。计算 样品的纯度
样品的纯度
您最近一年使用:0次
名校
6 . 二硫化钼(MoS2,难溶于水)具有良好的光、电性能,可由钼精矿(主要含MoS2,还含NiS、CaMoO4等)为原料经过如下过程制得。
(1)“浸取”。向钼精矿中加入NaOH溶液,再加入NaClO溶液,充分反应后的溶液中含有Na2MoO4、Na2SO4、NiSO4、NaCl。
①写出浸取时MoS2发生反应的离子方程式:_______ 。
②浸取后的滤渣中含CaMoO4。若浸取时向溶液中加入Na2CO3溶液,可提高浸出液中Mo元素的含量,原因是_______ 。
③浸取时,Mo元素的浸出率与时间的变化如图1所示。已知生成物对反应无影响,则反应3~4min时,Mo元素的浸出率迅速上升的原因是_______ 。

(2)“制硫代钼酸铵[(NH4)2MoS4,摩尔质量260g•mol-1]”。向浸出液中加入NH4NO3和HNO3,析出(NH4)2Mo4O13,将(NH4)2Mo4O13溶于水,向其中加入(NH4)2S溶液,可得(NH4)2MoS4,写出生成(NH4)2MoS4反应的化学方程式:________ 。
(3)“制MoS2”。(NH4)2MoS4可通过如下两种方法制取MoS2:
方法一:将(NH4)2MoS4在一定条件下加热,可分解得到MoS2、NH3、H2S和硫单质。其中NH3、H2S和硫单质的物质的量之比为8:4:1。
方法二:将(NH4)2MoS4在空气中加热可得MoS2,加热时所得剩余固体的质量与原始固体质量的比值与温度的关系如图2所示。
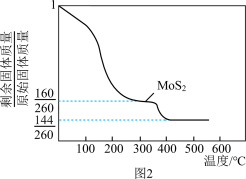
①方法一中,所得硫单质的分子式为_______ 。
②方法二中,500℃可得到Mo的一种氧化物,该氧化物的化学式为_______ 。
(1)“浸取”。向钼精矿中加入NaOH溶液,再加入NaClO溶液,充分反应后的溶液中含有Na2MoO4、Na2SO4、NiSO4、NaCl。
①写出浸取时MoS2发生反应的离子方程式:
②浸取后的滤渣中含CaMoO4。若浸取时向溶液中加入Na2CO3溶液,可提高浸出液中Mo元素的含量,原因是
③浸取时,Mo元素的浸出率与时间的变化如图1所示。已知生成物对反应无影响,则反应3~4min时,Mo元素的浸出率迅速上升的原因是

(2)“制硫代钼酸铵[(NH4)2MoS4,摩尔质量260g•mol-1]”。向浸出液中加入NH4NO3和HNO3,析出(NH4)2Mo4O13,将(NH4)2Mo4O13溶于水,向其中加入(NH4)2S溶液,可得(NH4)2MoS4,写出生成(NH4)2MoS4反应的化学方程式:
(3)“制MoS2”。(NH4)2MoS4可通过如下两种方法制取MoS2:
方法一:将(NH4)2MoS4在一定条件下加热,可分解得到MoS2、NH3、H2S和硫单质。其中NH3、H2S和硫单质的物质的量之比为8:4:1。
方法二:将(NH4)2MoS4在空气中加热可得MoS2,加热时所得剩余固体的质量与原始固体质量的比值与温度的关系如图2所示。

①方法一中,所得硫单质的分子式为
②方法二中,500℃可得到Mo的一种氧化物,该氧化物的化学式为
您最近一年使用:0次
2023-05-29更新
|
500次组卷
|
3卷引用:江苏省常州高级中学2023-2024学年高三上学期开学考试化学试题
名校
7 . Ⅰ.下列各组物质的分离或提纯,应选用下述方法的哪一种?(填标号)
A.萃取 B.加热 C.结晶 D.分液 E.过滤 F.蒸馏
(1)除去食盐水中的泥沙___________ 。
(2)从含有少量氯化钠的硝酸钾溶液中提取硝酸钾___________ 。
(3)分离水和汽油___________ 。
(4)分离 (沸点为76.75℃)和甲苯(沸点为110.6℃)的液体混合物
(沸点为76.75℃)和甲苯(沸点为110.6℃)的液体混合物___________ 。
Ⅱ.现有下列物质:①高锰酸钾 ②镁 ③氧气 ④氢氧化钠 ⑤硫酸 ⑥甲烷 ⑦ 胶体 ⑧硫酸铜
胶体 ⑧硫酸铜
(5)以上物质属于电解质的是___________ 属于非电解质的是___________ (填序号)。
(6)属于有机物的是___________ (填序号)。
(7)鉴别胶体和溶液最简单有效的物理方法是___________ ,分离胶体和溶液常用的物理方法是___________ 。
A.萃取 B.加热 C.结晶 D.分液 E.过滤 F.蒸馏
(1)除去食盐水中的泥沙
(2)从含有少量氯化钠的硝酸钾溶液中提取硝酸钾
(3)分离水和汽油
(4)分离
 (沸点为76.75℃)和甲苯(沸点为110.6℃)的液体混合物
(沸点为76.75℃)和甲苯(沸点为110.6℃)的液体混合物Ⅱ.现有下列物质:①高锰酸钾 ②镁 ③氧气 ④氢氧化钠 ⑤硫酸 ⑥甲烷 ⑦
 胶体 ⑧硫酸铜
胶体 ⑧硫酸铜(5)以上物质属于电解质的是
(6)属于有机物的是
(7)鉴别胶体和溶液最简单有效的物理方法是
您最近一年使用:0次
名校
8 . 下图是初中化学实验的几种常用仪器,请按要求填空。
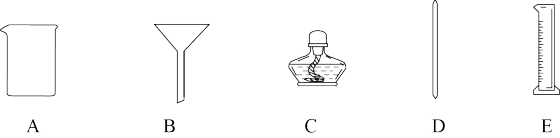
(1)①仪器C的名称叫_______ 。
②在读取E中液体体积时,视线应与凹液面的最低处_______ 。
(2)①进行过滤操作,除铁架台、A和D外,还需要用到上述仪器中的_______ (填字母)。
②配制一定质量分数的NaCl溶液,还必须补充的一种仪器是_______ 。

(1)①仪器C的名称叫
②在读取E中液体体积时,视线应与凹液面的最低处
(2)①进行过滤操作,除铁架台、A和D外,还需要用到上述仪器中的
②配制一定质量分数的NaCl溶液,还必须补充的一种仪器是
您最近一年使用:0次
2022-09-07更新
|
70次组卷
|
2卷引用:山东省临沂市重点中学2022-2023学年高一上学期9月入学考试化学试题
9 . 航天员王亚平在“天宫课堂”中介绍了空间站中的生活,在轨演示了水球变气球等一系列炫酷又好玩的实验。
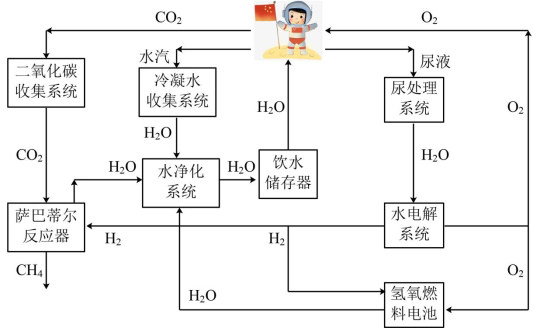
I.“天宫”中水和氧气的最大化利用是保障生活的重要措施。如图是空间站常用资源再利用模拟图。
(1)“尿处理子系统”采用蒸馏方法对其中成分进行分离。此方法是根据尿液中各成分的____ 不同进行分离的。
(2)“水电解系统”中产生氧气的电极应接电池的____ 极(填“正”或“负”)。发生反应的化学方程式为____ 。
(3)在水净化系统中,用臭氧(O3)消毒,臭氧在一定条件下转化为氧气的化学方程式为____ 。
(4)在一定条件下,“萨巴蒂尔反应器”可以除去CO2,该反应的化学方程式为____ 。
II.王亚平将蓝色颜料注入水球中,整个水球变成蓝色,将泡腾片放入水球中,产生大量气泡向四面八方扩散,充满整个水球。气体并不溢出,使水球越来越大。
(5)泡腾片在水中发生了如下反应:H3C6H5O7+3NaHCO3=Na3C6H5O7+3H2O+3____ (补全化学方程式)。
(6)如果在空间站失重状态下收集制得的氧气,可以选用下列装置中的____ (填序号)。
I.“天宫”中水和氧气的最大化利用是保障生活的重要措施。如图是空间站常用资源再利用模拟图。

(1)“尿处理子系统”采用蒸馏方法对其中成分进行分离。此方法是根据尿液中各成分的
(2)“水电解系统”中产生氧气的电极应接电池的
(3)在水净化系统中,用臭氧(O3)消毒,臭氧在一定条件下转化为氧气的化学方程式为
(4)在一定条件下,“萨巴蒂尔反应器”可以除去CO2,该反应的化学方程式为
II.王亚平将蓝色颜料注入水球中,整个水球变成蓝色,将泡腾片放入水球中,产生大量气泡向四面八方扩散,充满整个水球。气体并不溢出,使水球越来越大。
(5)泡腾片在水中发生了如下反应:H3C6H5O7+3NaHCO3=Na3C6H5O7+3H2O+3
(6)如果在空间站失重状态下收集制得的氧气,可以选用下列装置中的
A. | B.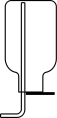 | C.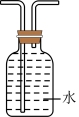 | D. |
您最近一年使用:0次
2022-08-22更新
|
375次组卷
|
3卷引用:福建省龙岩第一中学2022-2023学年高一上学期开学考试化学试题
名校
10 . 化学就在我们身边,它与我们的日常生活生产密切相关,按要求回答以下问题
(1)煎中药时用水在煮沸条件下提取中药中的有效成分相当于化学实验中的_______ 操作(填操作名称)
(2)维生素C又称“抗坏血酸”,在人体内有重要功能,具有还原性,能帮助人体将食物中摄取的不易吸收的 转化为
转化为_______ 。
(3)印刷电路板是由高分子材料和铜箔复合而成,刻制印刷电路时,常用FeCl3作“腐蚀液”,生成 和
和 ,其反应的离子方程式为
,其反应的离子方程式为_______ 。
(4)洪水过后,饮用水的消毒杀菌成为抑制大规模传染性疾病爆发的有效方法之一。漂白粉是常用的消毒剂,工业上将氯气通入石灰乳中制取漂白粉,其化学方程式为_______ ;漂白粉敞放在空气中会变质,其发生的化学方程式为_______ 。
(5)某同学需帮助水质检测站配制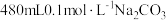 溶液以备使用。
溶液以备使用。
①该同学选择托盘天平、药匙、量筒、烧杯、玻璃棒、胶头滴管、_______ 。
②该同学应称取 固体
固体_______ g
③在转移完溶液后未洗涤玻璃棒和烧杯,会使浓度_______ (填“偏大”、“偏小”或“不变”)。
(1)煎中药时用水在煮沸条件下提取中药中的有效成分相当于化学实验中的
(2)维生素C又称“抗坏血酸”,在人体内有重要功能,具有还原性,能帮助人体将食物中摄取的不易吸收的
 转化为
转化为(3)印刷电路板是由高分子材料和铜箔复合而成,刻制印刷电路时,常用FeCl3作“腐蚀液”,生成
 和
和 ,其反应的离子方程式为
,其反应的离子方程式为(4)洪水过后,饮用水的消毒杀菌成为抑制大规模传染性疾病爆发的有效方法之一。漂白粉是常用的消毒剂,工业上将氯气通入石灰乳中制取漂白粉,其化学方程式为
(5)某同学需帮助水质检测站配制
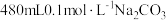 溶液以备使用。
溶液以备使用。①该同学选择托盘天平、药匙、量筒、烧杯、玻璃棒、胶头滴管、
②该同学应称取
 固体
固体③在转移完溶液后未洗涤玻璃棒和烧杯,会使浓度
您最近一年使用:0次



