名校
1 . 下列除杂方案错误的是( )
| 选项 | 被提纯的物质 | 杂质 | 除杂试剂 | 除杂方法 |
| A |  (g) (g) |  (g) (g) | 酸性 溶液、浓 溶液、浓 | 洗气 |
| B |  (aq) (aq) |  (aq) (aq) | NaOH溶液 | 过滤 |
| C |  (g) (g) | HCl(g) | 饱和食盐水、浓 | 洗气 |
| D |  (s) (s) |  (s) (s) | — | 灼烧 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
2 . 为提纯下列物质(括号内为杂质),选用的除杂试剂或分离方法不正确的( )
| 物质 | 试剂 | 分离方法 | |
| A | 乙烷(乙烯) | 溴水 | 洗气 |
| B | 苯甲酸(可溶性杂质) | 水 | 重结晶 |
| C | 乙醇(水) | 生石灰 | 蒸馏 |
| D | 溴苯(Br2) | CCl4 | 萃取分液 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
3 . 电镀废水沉泥中含Cu、Ni、Ag和Fe等多种元素的有机金属盐,采用焙烧一浸出—分离回收的工艺流程可有效分离电镀废水沉泥中的金属,其流程如下:
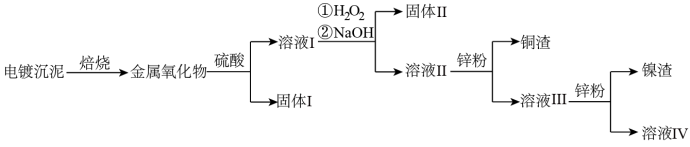
下列叙述错误的是

下列叙述错误的是
| A.上述流程中硫酸可以用稀盐酸代替 |
| B.“固体Ⅱ”为Fe(OH)2 |
| C.溶液III中含有Na+、Ni2+、Zn2+等金属离子 |
| D.合理处理电镀废沉泥可实现资源的回收与可持续利用 |
您最近一年使用:0次
2019-02-05更新
|
423次组卷
|
2卷引用:【市级联考】广东省茂名市2019届高三上学期第一次综合测试理科综合化学试题
2019高三·全国·专题练习
名校
解题方法
4 . 除去粗盐中的杂质MgCl2、CaCl2和Na2SO4,过程如下: 不正确 的是
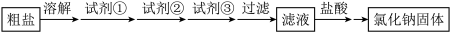
| A.试剂①、②、③分别是NaOH、Na2CO3、BaCl2 |
| B.除去Ca2+的主要反应:Ca2+ + CO32-=CaCO3↓ |
| C.检验SO42-是否除净的方法:取适量滤液,加稀盐酸酸化,再加BaCl2溶液 |
| D.加稀盐酸调节pH后,采用蒸发结晶的方法得到NaCl固体 |
您最近一年使用:0次
2019-01-24更新
|
834次组卷
|
9卷引用:考点20 化学基础实验——《备战2020年高考精选考点专项突破题集》
(已下线)考点20 化学基础实验——《备战2020年高考精选考点专项突破题集》(已下线)【南昌新东方】南昌三中2019-2020 高一(上)期末(已下线)内蒙古赤峰市宁城县2018-2019学年高一上学期期末考试化学试题广西壮族自治区桂林市七星区桂林市第十八中学2020-2021学年高一上学期期中考试化学试题2024届重庆市乌江新高考协作体高三下学期模拟预测化学试题广东省广州市白云中学2022-2023学年高一下学期期中考试化学试题天津市2022-2023学年高一下学期学业水平合格考模拟化学试题北京师范大学附属中学2022-2023学年高一下学期期中考试化学试题天津市武清区黄花店中学2023-2024学年高一下学期第一次月考化学试题(文科)
名校
5 . 工业上以某软锰矿(主要成分为MnO2,还含有SiO2、Al2O3等杂质)为原料,利用烟道气中的SO2制备MnSO4·H2O的流程如下:
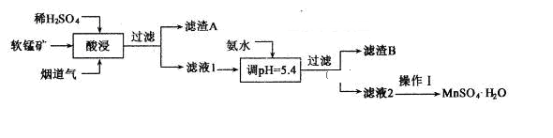
下列说法不正确的是

下列说法不正确的是
| A.滤渣A的主要成分能导电,可制备光导纤维 |
| B.“酸浸”主要反应的离子方程式为MnO2+SO2=Mn2++SO42- |
| C.加氨水调节pH的目的是除Al3+ |
| D.操作I为结晶、过滤、洗涤、干燥 |
您最近一年使用:0次
2019-01-14更新
|
280次组卷
|
5卷引用:【市级联考】山东省济宁市2019届高三上学期期末考试化学试题
【市级联考】山东省济宁市2019届高三上学期期末考试化学试题福建2020届高三化学总复习专题训练——无极工艺流程选择填空题重庆市第八中学校2021-2022学年高三上学期期中考试化学试题2020高考化学二轮总复习高分必备 题型专题1 选择题专练(已下线)专题十 能力提升检测卷 (测) — 2022年高考化学一轮复习讲练测(新教材新高考)
名校
6 . 巴蜀中学某化学兴趣实验小组的同学欲通过某氯化钠样品来获得纯净的氯化钠固体(杂质:含有 少量泥沙、Na2SO4 和碘化钠),该小组的同学设计了如下图所示的实验流程:
【查阅资料】氯气可以从碘化钠溶液中置换出碘单质。
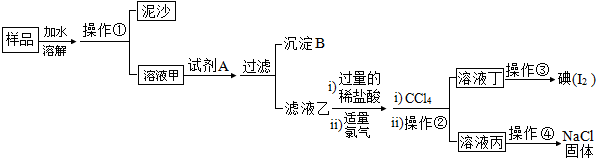
阅读上述实验流程,完成下列填空:
(1)操作①的名称_____ ;操作④的名称_____ 。
(2)在实验室进行操作②时,要用到的玻璃仪器有_____ (填仪器名称)
(3)若沉淀 B 中含有 BaSO4,由上述实验操作流程可知,A 中所包含的化学试剂有_____ (请 按加入的顺序填上相应试剂的化学式),请写出生成 BaSO4 的化学方程式_____ 。
(4)操作③目的是从含碘的 CCl4 溶液中分离出单质碘和回收 CCl4,该步操作应选择的实验装置是_______ 。
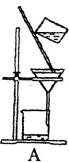
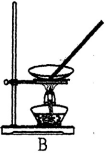
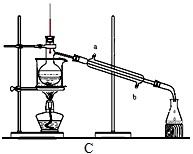
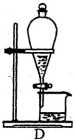
(5)如何检验所得 NaCl 固体中所含杂质 Na2SO4 已经除尽,请简述该实验操作和现象____________ 。
【查阅资料】氯气可以从碘化钠溶液中置换出碘单质。

阅读上述实验流程,完成下列填空:
(1)操作①的名称
(2)在实验室进行操作②时,要用到的玻璃仪器有
(3)若沉淀 B 中含有 BaSO4,由上述实验操作流程可知,A 中所包含的化学试剂有
(4)操作③目的是从含碘的 CCl4 溶液中分离出单质碘和回收 CCl4,该步操作应选择的实验装置是




(5)如何检验所得 NaCl 固体中所含杂质 Na2SO4 已经除尽,请简述该实验操作和现象
您最近一年使用:0次
名校
7 . 为了除去粗盐中的 Ca2+、Mg2+、SO42-和泥沙,可将粗盐溶于水,再进行下列操作:①过滤 ②加过量的NaOH 溶液 ③加适量的盐酸 ④加过量的 Na2CO3 溶液 ⑤加过量的 BaCl2 溶液。正确的排列顺序是
| A.①②⑤④①③ | B.①⑤③①②④ | C.①②④⑤①③ | D.①④⑤②①③ |
您最近一年使用:0次
名校
8 . 现有一瓶甲和乙的混合物,已知甲和乙的某些性质如下表所示:
据此,将甲和乙互相分离的方法是
| 物质 | 熔点/ ℃ | 沸点/ ℃ | 密度/ g·cm−3 | 水中的溶解性 |
| 甲 | -98 | 57.5 | 0.93 | 可溶 |
| 乙 | -84 | 77 | 0.90 | 可溶 |
| A.蒸馏法 | B.升华法 | C.萃取法 | D.过滤法 |
您最近一年使用:0次
2018-11-18更新
|
142次组卷
|
5卷引用:重庆市黔江新华中学校2019—2020学年高一上学期期中考试化学试题
名校
9 . 下表中,除去物质所含杂质的方法正确的是( )
| 选项 | 物质 | 所含物质 | 除去杂质的方法 |
| A | HCl气体 | CO2 | 通过氢氧化钠溶液 |
| B | 氢氧化钠溶液 | 碳酸钠 | 加入适量稀盐酸 |
| C | 氧化钙 | 碳酸钙 | 高温煅烧 |
| D | 硫酸铜溶液 | 硫酸亚铁 | 加入足量铁粉过滤 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
10 . 硫酸镁还原热解制备高纯氧化镁是一种新的探索,以解决氧化镁在医药、建筑等行业的应用广泛。现以菱镁矿(主要成分为MgCO3,含少量FeCO3)为原料制备高纯氧化镁的实验流程如下:
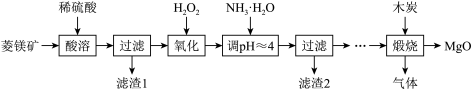
(1)酸溶所涉及反应的离子方程式为_________________________________________ 、_________________________________________________________ 。
(2)加入H2O2氧化的作用是_________________ ,滤渣2的成分是___________ (填化学式)。
(3)煅烧过程存在以下反应:
2MgSO4+C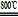 2MgO+2SO2↑+CO2↑
2MgO+2SO2↑+CO2↑
MgSO4+C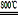 MgO+SO2↑+CO↑
MgO+SO2↑+CO↑
MgSO4+3C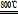 MgO+S↑+3CO↑
MgO+S↑+3CO↑
利用下图装置对煅烧产生的气体进行分步吸收或收集。
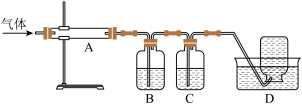
①B中盛放的溶液可以是______ (填字母)。
a.NaOH 溶液 b.Na2CO3溶液 c. KMnO4溶液 d. 稀硝酸
②C装置的作用是______________________ ,D中收集的气体可以是 _______ (填化学式)。
③A中得到的淡黄色固体与热的NaOH溶液反应,产物中元素最高价态为+4,写出该反应的离子方程式:________________________________________________ 。

(1)酸溶所涉及反应的离子方程式为
(2)加入H2O2氧化的作用是
(3)煅烧过程存在以下反应:
2MgSO4+C
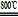 2MgO+2SO2↑+CO2↑
2MgO+2SO2↑+CO2↑MgSO4+C
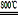 MgO+SO2↑+CO↑
MgO+SO2↑+CO↑MgSO4+3C
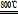 MgO+S↑+3CO↑
MgO+S↑+3CO↑利用下图装置对煅烧产生的气体进行分步吸收或收集。

①B中盛放的溶液可以是
a.NaOH 溶液 b.Na2CO3溶液 c. KMnO4溶液 d. 稀硝酸
②C装置的作用是
③A中得到的淡黄色固体与热的NaOH溶液反应,产物中元素最高价态为+4,写出该反应的离子方程式:
您最近一年使用:0次



