解题方法
1 . 工业上碳酸钠大多采用侯氏制碱法制取,所得碳酸钠样品中往往含有少量的NaCl,现欲测定某碳酸钠样品中Na2CO3的质量分数,某探究性学习小组设计以下两种方案。
Ⅰ.取样品bg,设计如下实验方案,操作步骤如下:
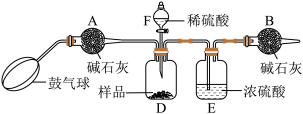
①如图连接装置(除B外)并加入所需药品。
②称量并记录B的质量(a1g)。
③按动鼓气球,持续约1分钟。
④连接上B。
⑤打开分液漏斗F的活塞,将稀硫酸快速加入D中后,关闭活塞。
⑥按动鼓气球,持续约1分钟。
⑦称量并记录B的质量(a2g)。
⑧计算
(1)操作③中,鼓入空气的作用是_______ ;操作⑥中,鼓入空气的作用是_______ ;
(2)根据题干所给的数据列出样品中Na2CO3的质量分数表达式_______ 。
(3)经实验发现最终所得的 Na2CO3的质量分数超过100%,其可能的原因是_______ 。
Ⅱ.现有碳酸钠和氯化钠的混合物样品25g,将其放入干净的烧杯中,加入一定量的水,使其完全溶解得到200mL溶液。向所得溶液中慢慢加入4mol•L-1的盐酸,烧杯中溶液的质量与加入盐酸的体积关系曲线如图所示。请回答下列问题。
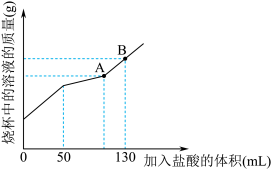
(4)加入50mL盐酸时,写出反应的离子反应方程式_______ 。
(5)在这个样品中,含碳酸钠的质量分数为_______ 。
(6)A点时,溶液溶质是_______ ,所得溶质质量分数为_______ 。(忽略体积的微小变化,结果保留小数点后两位)。
Ⅰ.取样品bg,设计如下实验方案,操作步骤如下:

①如图连接装置(除B外)并加入所需药品。
②称量并记录B的质量(a1g)。
③按动鼓气球,持续约1分钟。
④连接上B。
⑤打开分液漏斗F的活塞,将稀硫酸快速加入D中后,关闭活塞。
⑥按动鼓气球,持续约1分钟。
⑦称量并记录B的质量(a2g)。
⑧计算
(1)操作③中,鼓入空气的作用是
(2)根据题干所给的数据列出样品中Na2CO3的质量分数表达式
(3)经实验发现最终所得的 Na2CO3的质量分数超过100%,其可能的原因是
Ⅱ.现有碳酸钠和氯化钠的混合物样品25g,将其放入干净的烧杯中,加入一定量的水,使其完全溶解得到200mL溶液。向所得溶液中慢慢加入4mol•L-1的盐酸,烧杯中溶液的质量与加入盐酸的体积关系曲线如图所示。请回答下列问题。

(4)加入50mL盐酸时,写出反应的离子反应方程式
(5)在这个样品中,含碳酸钠的质量分数为
(6)A点时,溶液溶质是
您最近一年使用:0次
名校
2 . (1)FeS与一定浓度的HNO3反应,生成Fe(NO3)3、Fe2(SO4)3、NO2、N2O4、NO和H2O,当NO2、N2O4、NO的物质的量之比为1﹕1﹕1时,实际参加反应的FeS与HNO3的物质的量之比为____________ 。
(2)在P+CuSO4+H2O→Cu3P+H3PO4+H2SO4(未配平)的反应中,7.5 mol CuSO4可氧化P的物质的量为____________ mol。
(3)足量铜与一定量浓硝酸反应,得到硝酸铜溶液和NO2、N2O4、NO的混合气体,将这些气体与1.68 L O2(标准状况)混合后通入水中,所有气体完全被水吸收生成硝酸。若向所得硝酸铜溶液中加入5 mol·L-1 NaOH溶液至Cu2+恰好完全沉淀,则消耗NaOH溶液的体积是___________ mL。
(4)利用钴渣[含Co(OH)3、Fe(OH)3等]制备钴氧化物的工艺流程如下:

Co(OH)3溶解还原反应的离子方程式为_______________________________ ,在空气中煅烧CoC2O4生成钴氧化物和CO2,测得充分煅烧后固体质量为2.41g,CO2的体积为1.344L(标准状况),则钴氧化物的化学式为______________ 。
(2)在P+CuSO4+H2O→Cu3P+H3PO4+H2SO4(未配平)的反应中,7.5 mol CuSO4可氧化P的物质的量为
(3)足量铜与一定量浓硝酸反应,得到硝酸铜溶液和NO2、N2O4、NO的混合气体,将这些气体与1.68 L O2(标准状况)混合后通入水中,所有气体完全被水吸收生成硝酸。若向所得硝酸铜溶液中加入5 mol·L-1 NaOH溶液至Cu2+恰好完全沉淀,则消耗NaOH溶液的体积是
(4)利用钴渣[含Co(OH)3、Fe(OH)3等]制备钴氧化物的工艺流程如下:

Co(OH)3溶解还原反应的离子方程式为
您最近一年使用:0次
11-12高一上·浙江宁波·期中
3 . 某工厂化验室为测定某黄铁矿(主要成分是FeS2)的纯度,取1.00 g矿石样品(所含杂质不挥发且不与氧气反应),在氧气流中充分灼烧,完全反应后,冷却,称量固体残留物,质量为0.75g。
(1)该黄铁矿中FeS2的质量分数为多少?
(2)该工厂用这种黄铁矿制硫酸,在FeS2燃烧过程中损失2%,由SO2氧化成SO3时,SO2的利用率为80%,吸收塔中SO3完全吸收。若煅烧10 .0t上述黄铁矿,则可制得98%的硫酸多少吨?
(1)该黄铁矿中FeS2的质量分数为多少?
(2)该工厂用这种黄铁矿制硫酸,在FeS2燃烧过程中损失2%,由SO2氧化成SO3时,SO2的利用率为80%,吸收塔中SO3完全吸收。若煅烧10 .0t上述黄铁矿,则可制得98%的硫酸多少吨?
您最近一年使用:0次



