1 . 在测定Na2SO4和NaCl的混合物中Na2SO4的质量分数时,可以在混合物中加入过量BaCl2溶液,沉淀SO ,然后过滤、洗涤、烘干、称量得到BaSO4的质量,试问:
,然后过滤、洗涤、烘干、称量得到BaSO4的质量,试问:
(1)怎样判断SO 是否沉淀完全
是否沉淀完全_______ 。
(2)沉淀的洗涤方法_______ 。
(3)怎样判断沉淀是否洗净_______ 。
 ,然后过滤、洗涤、烘干、称量得到BaSO4的质量,试问:
,然后过滤、洗涤、烘干、称量得到BaSO4的质量,试问:(1)怎样判断SO
 是否沉淀完全
是否沉淀完全(2)沉淀的洗涤方法
(3)怎样判断沉淀是否洗净
您最近一年使用:0次
2 . 食盐是日常生活的必需品,也是重要的化工原料。粗食盐常含有少量K+、Ca2+、Mg2+、Fe3+、SO 等杂质离子,实验室提纯NaCl的流程如下:
等杂质离子,实验室提纯NaCl的流程如下:

提供的试剂:饱和Na2CO3溶液、饱和K2CO3溶液、NaOH溶液、BaCl2溶液、Ba(NO3)2溶液、75%乙醇、四氯化碳。选择最好的试剂洗涤除去NaCl晶体表面附带的少量KCl,洗涤的操作为_______ 。
 等杂质离子,实验室提纯NaCl的流程如下:
等杂质离子,实验室提纯NaCl的流程如下:
提供的试剂:饱和Na2CO3溶液、饱和K2CO3溶液、NaOH溶液、BaCl2溶液、Ba(NO3)2溶液、75%乙醇、四氯化碳。选择最好的试剂洗涤除去NaCl晶体表面附带的少量KCl,洗涤的操作为
您最近一年使用:0次
21-22高一·全国·课时练习
解题方法
3 . 选择合适的实验方法完成下列操作:
(1)分离KCl和MnO2的混合物_______ 。
(2)除去KNO3固体中少量的KCl_______ 。
(3)从碘水中提取碘单质_______ 。
(4)从NaCl水溶液中提取NaCl固体_______ 。
(5)从海水中得到淡水_______ 。
(6)分离柴油和水的混合物_______ 。
(7)分离乙酸(沸点118℃)与乙酸乙酯(沸点77.1℃)_______ 。
(1)分离KCl和MnO2的混合物
(2)除去KNO3固体中少量的KCl
(3)从碘水中提取碘单质
(4)从NaCl水溶液中提取NaCl固体
(5)从海水中得到淡水
(6)分离柴油和水的混合物
(7)分离乙酸(沸点118℃)与乙酸乙酯(沸点77.1℃)
您最近一年使用:0次
2021高一·全国·专题练习
解题方法
4 . 在实验室利用胆矾晶体(CuSO4·5H2O)和烧碱溶液制备氧化铜固体,其实验过程可分为如下几个步骤:①混合;②过滤;③加热分解;④溶解;⑤洗涤。完成下列填空:
(1)实验正确的操作顺序是___________ (填序号)。
(2)步骤②中所用到的玻璃仪器有___________ 。
(3)在实验过程中多次用到玻璃棒,其作用有___________ 、___________ 。
(1)实验正确的操作顺序是
(2)步骤②中所用到的玻璃仪器有
(3)在实验过程中多次用到玻璃棒,其作用有
您最近一年使用:0次
2021高一·全国·专题练习
5 . 有一包从海水中获得的的粗盐(杂质可能为CaCl2或MgCl2),现对它的成分进行探究,并测定粗盐中NaCl的质量分数。
探究一:这包粗盐中究竟有什么杂质?
实验步骤:取样并溶解,加入数滴NaOH溶液,无明显现象,接着再加入数滴Na2CO3溶液,有白色沉淀生成。
(1)证明粗盐中的杂质是_______ 。
探究二:这包粗盐中NaCl的质量分数是多少?
实验步骤:①称取一定质量的样品;②将样品加水溶解制成粗盐溶液;③向粗盐溶液中加入过量的Na2CO3溶液,过滤;④将沉淀充分洗涤干净后小心烘干,得到纯净固体A.称量沉淀质量,由此进一步计算出粗盐中NaCl的质量分数。
(2)步骤②③中都用到同一仪器(填名称)_______ ,目的分别是_______ 、_______ 。
(3)步骤④中洗涤沉淀目的是为了洗去沉淀表面吸附的_______ 。
【反思与交流】有同学认为,向滤出沉淀得到的滤液中加入稀盐酸,调节pH=7,然后移入蒸发皿蒸发,得到纯净NaCl固体。由此也可计算出粗盐中NaCl的质量分数。
(4)这个方案如果可行,浓缩蒸发溶液时要用到玻璃棒,其作用是_______ ,如果不可行,理由是_______ (若认为可行,可不填)。
探究一:这包粗盐中究竟有什么杂质?
实验步骤:取样并溶解,加入数滴NaOH溶液,无明显现象,接着再加入数滴Na2CO3溶液,有白色沉淀生成。
(1)证明粗盐中的杂质是
探究二:这包粗盐中NaCl的质量分数是多少?
实验步骤:①称取一定质量的样品;②将样品加水溶解制成粗盐溶液;③向粗盐溶液中加入过量的Na2CO3溶液,过滤;④将沉淀充分洗涤干净后小心烘干,得到纯净固体A.称量沉淀质量,由此进一步计算出粗盐中NaCl的质量分数。
(2)步骤②③中都用到同一仪器(填名称)
(3)步骤④中洗涤沉淀目的是为了洗去沉淀表面吸附的
【反思与交流】有同学认为,向滤出沉淀得到的滤液中加入稀盐酸,调节pH=7,然后移入蒸发皿蒸发,得到纯净NaCl固体。由此也可计算出粗盐中NaCl的质量分数。
(4)这个方案如果可行,浓缩蒸发溶液时要用到玻璃棒,其作用是
您最近一年使用:0次
6 . 下图所示的装置是化学实验中常见混合物分离和提纯的方法,也是学生应具备的实验基本技能。回答下列问题(填代表装置图的字母):

(1)从氯化钾溶液中得到氯化钾固体,选择______ 装置。
(2)氯化钠固体中混有碘,选择______ 装置。
(3)河水样品中加了少量明矾,选择______ 装置。
(4)除去自来水中的 、
、 杂质离子,选择
杂质离子,选择______ 装置。
(5)装置E在分液时为使液体顺利滴下,除打开活塞外,还应进行的具体操作是______ 。

(1)从氯化钾溶液中得到氯化钾固体,选择
(2)氯化钠固体中混有碘,选择
(3)河水样品中加了少量明矾,选择
(4)除去自来水中的
 、
、 杂质离子,选择
杂质离子,选择(5)装置E在分液时为使液体顺利滴下,除打开活塞外,还应进行的具体操作是
您最近一年使用:0次
名校
7 . 海洋化学资源的综合利用对人类的发展意义重大。
(1)以海水为原料获得的粗盐中含有CaCl2、MgCl2、Na2SO4和难溶性杂质。
①除去难溶性杂质,实验室常用的分离操作是___________ 。
②除去可溶性杂质,所选试剂及加入的顺序依次是NaOH、___________ 、___________ 、稀盐酸。
(2)从海带中提取碘的工业生产过程如下:
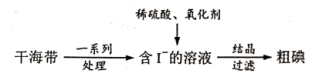
①氧化剂将 。下列氧化剂中,最好选用
。下列氧化剂中,最好选用___________ (填字母)。
a.酸性KMnO4 b. H2O2 c.浓硫酸
②实验室中常用CCl4从氧化后的溶液中萃取I2,其原理是___________ 。
(3)从海水中提取镁的过程是将海水中的Mg2+转变为无水MgCl2,电解熔融MgCl2得到金属镁。该过程中属于氧化还原反应的化学方程式为___________ 。
(1)以海水为原料获得的粗盐中含有CaCl2、MgCl2、Na2SO4和难溶性杂质。
①除去难溶性杂质,实验室常用的分离操作是
②除去可溶性杂质,所选试剂及加入的顺序依次是NaOH、
(2)从海带中提取碘的工业生产过程如下:

①氧化剂将
 。下列氧化剂中,最好选用
。下列氧化剂中,最好选用a.酸性KMnO4 b. H2O2 c.浓硫酸
②实验室中常用CCl4从氧化后的溶液中萃取I2,其原理是
(3)从海水中提取镁的过程是将海水中的Mg2+转变为无水MgCl2,电解熔融MgCl2得到金属镁。该过程中属于氧化还原反应的化学方程式为
您最近一年使用:0次
2021-01-27更新
|
927次组卷
|
6卷引用:第4章 化学与自然资源的开发利用(培优提升卷)-2020-2021学年高一化学必修2章末集训必刷卷(人教版)
(已下线)第4章 化学与自然资源的开发利用(培优提升卷)-2020-2021学年高一化学必修2章末集训必刷卷(人教版)(已下线)专题11 自然资源的开发利用【专项训练】-2020-2021学年高一化学下学期期末专项复习(人教版2019必修第二册)福建省福州第二中学2021-2022学年高一上学期12月月考化学试题福建省福州第一中学2021-2022学年高一上学期期末考试化学试题四川省甘孜州2021-2022学年高一下学期学业质量统一监测期末统考化学试题江苏省连云港市2020-2021学年高一上学期期末调研考试化学试题
解题方法
8 . 观察下列实验装置图,按要求作答:
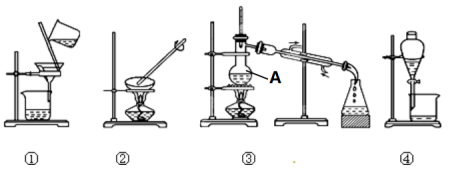
(1)写出图中实验操作的名称:①_______ ,③中仪器A的名称_______
(2)装置④中所有玻璃仪器的名称:_______ ,_______
(3)下列实验需要在哪套装置中进行:(填序号,每套装置仅使用一次)
①从 KCl溶液中获取KCl晶体_______ ;
②从海水中提取淡水_______ ;
③分离CaCO3和水_______ ;
④分离植物油和水_______ 。

(1)写出图中实验操作的名称:①
(2)装置④中所有玻璃仪器的名称:
(3)下列实验需要在哪套装置中进行:(填序号,每套装置仅使用一次)
①从 KCl溶液中获取KCl晶体
②从海水中提取淡水
③分离CaCO3和水
④分离植物油和水
您最近一年使用:0次
2021-01-24更新
|
342次组卷
|
3卷引用:专题13 化学实验基础-备战2021届高考化学二轮复习题型专练
(已下线)专题13 化学实验基础-备战2021届高考化学二轮复习题型专练广西北流市实验中学2020-2021学年高一上学期期中考试化学试题西藏林芝市第二高级中学2021-2022学年高三下学期第四次月考理综化学试题
解题方法
9 . NaCl溶液中混有 、
、 和淀粉胶体,选择适当的试剂和方法从中提纯出NaCl晶体。相应的实验过程如图所示:
和淀粉胶体,选择适当的试剂和方法从中提纯出NaCl晶体。相应的实验过程如图所示:
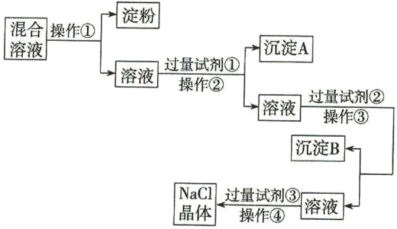
(1)写出上述实验过程中所用试剂的化学式:试剂①为_______ ;试剂③为_______ 。
(2)判断试剂①已过量的方法是_______ 。
(3)操作①是利用半透膜进行分离提纯,操作①的实验结果:淀粉胶体_______ (填“能”或“不能”)透过半透膜;
_______ (填“能”或“不能”)透过半透膜。
(4)操作④的名称是_______ 。
(5)实验室用制得的NaCl晶体配制480mL 1.0mol/L的NaCl溶液,用托盘天平称量的氯化钠固体的质量是_______ ,配制过程用到的玻璃仪器除烧杯、玻璃棒、胶头滴管外,还有_______ 。
 、
、 和淀粉胶体,选择适当的试剂和方法从中提纯出NaCl晶体。相应的实验过程如图所示:
和淀粉胶体,选择适当的试剂和方法从中提纯出NaCl晶体。相应的实验过程如图所示:
(1)写出上述实验过程中所用试剂的化学式:试剂①为
(2)判断试剂①已过量的方法是
(3)操作①是利用半透膜进行分离提纯,操作①的实验结果:淀粉胶体

(4)操作④的名称是
(5)实验室用制得的NaCl晶体配制480mL 1.0mol/L的NaCl溶液,用托盘天平称量的氯化钠固体的质量是
您最近一年使用:0次
10 . 将分离、提纯下列物质的方法的序号填在横线上。
①过滤 ②蒸馏 ③加热 ④分液 ⑤萃取⑥结晶
(1)除去石灰水中悬浮的 CaCO3颗粒∶___________ 。
(2)除去NaCl晶体中混有的碘单质∶___________ 。
(3)分离汽油和煤油的混合物∶___________ 。
(4)分离水和苯的混合物∶___________ 。
(5)用四氯化碳提取溴水中的溴单质∶___________
(6)从含有少量氯化钠的硝酸钾溶液中提取硝酸钾∶___________
①过滤 ②蒸馏 ③加热 ④分液 ⑤萃取⑥结晶
(1)除去石灰水中悬浮的 CaCO3颗粒∶
(2)除去NaCl晶体中混有的碘单质∶
(3)分离汽油和煤油的混合物∶
(4)分离水和苯的混合物∶
(5)用四氯化碳提取溴水中的溴单质∶
(6)从含有少量氯化钠的硝酸钾溶液中提取硝酸钾∶
您最近一年使用:0次



