23-24高一上·全国·期中
名校
解题方法
1 . 钠的化合物在日常生活中的应用非常广泛。回答下列问题:
Ⅰ.为了测定Na2CO3和NaHCO3的混合物中Na2CO3的质量分数,某同学用如下实验装置完成实验。
(1)实验前首先要进行的操作是___________ 。
(2)某同学称取65.4 g混合物于锥形瓶中,打开止水夹,通入N2,一段时间后,关闭止水夹,打开旋塞,当锥形瓶中没有气泡生成时,关闭旋塞,再次打开止水夹,通入一段时间N2。停止通N2,装置C的质量增加30.8 g。
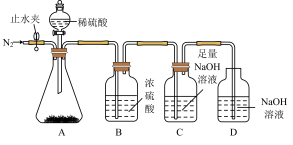
①两次通入N2的目的分别是___________ 、___________ 。
②混合物中Na2CO3的物质的量为___________ mol。
Ⅱ.侯德榜“联合制碱法”将制碱技术发展到一个新的水平。该工艺以氯化钠为原料制取纯碱,主要流程如图所示(部分物质已略去)。
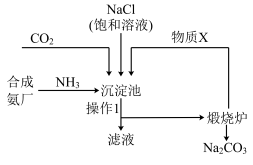
资料:沉淀池中的反应为NaCl+CO2+NH3+H2O=NaHCO3↓+NH4Cl。
(3)操作1的名称为___________ ;煅烧炉中反应的化学方程式为___________ 。
(4)物质X可循环利用,其化学式为___________ 。
(5)某同学提出制得的纯碱中可能含有氯化钠,请设计实验鉴别:___________ (写出步骤、现象和结论)。
Ⅰ.为了测定Na2CO3和NaHCO3的混合物中Na2CO3的质量分数,某同学用如下实验装置完成实验。
(1)实验前首先要进行的操作是
(2)某同学称取65.4 g混合物于锥形瓶中,打开止水夹,通入N2,一段时间后,关闭止水夹,打开旋塞,当锥形瓶中没有气泡生成时,关闭旋塞,再次打开止水夹,通入一段时间N2。停止通N2,装置C的质量增加30.8 g。

①两次通入N2的目的分别是
②混合物中Na2CO3的物质的量为
Ⅱ.侯德榜“联合制碱法”将制碱技术发展到一个新的水平。该工艺以氯化钠为原料制取纯碱,主要流程如图所示(部分物质已略去)。

资料:沉淀池中的反应为NaCl+CO2+NH3+H2O=NaHCO3↓+NH4Cl。
(3)操作1的名称为
(4)物质X可循环利用,其化学式为
(5)某同学提出制得的纯碱中可能含有氯化钠,请设计实验鉴别:
您最近一年使用:0次
解题方法
2 . 碳酸亚铁(FeCO3)可用于制备补血剂。某兴趣小组对FeCO3的制备与性质进行如图探究。回答下列问题:
(1)利用图1装置制备FeCO3:向装置C的碳酸钠溶液中通入一段时间CO2至pH约为7,再滴加一定量FeSO4溶液,产生白色沉淀,经过滤、洗涤、干燥,得到FeCO3固体。
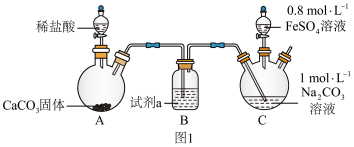
①图1中装有稀盐酸的仪器名称为______ 。
②向碳酸钠溶液中通入CO2的目的有______ 、_____ 。
③试剂a是_____ (填“饱和食盐水”或“NaOH稀溶液”),装置C中制取FeCO3的离子方程式为______ 。
(2)称取一定质量的纯净FeCO3放入硬质玻璃管中(装置如图2),打开K,通入氧气,加热硬质玻璃管。乙瓶中澄清石灰水不再产生沉淀时,停止加热,继续通入氧气至玻璃管冷却,称量剩余固体的质量。
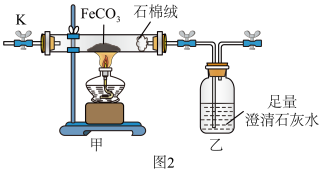
若开始时称取23.2gFeCO3固体,反应后称得剩余固体质量为16.0g,写出硬质玻璃管中发生反应的化学方程式:______ 。
(1)利用图1装置制备FeCO3:向装置C的碳酸钠溶液中通入一段时间CO2至pH约为7,再滴加一定量FeSO4溶液,产生白色沉淀,经过滤、洗涤、干燥,得到FeCO3固体。

①图1中装有稀盐酸的仪器名称为
②向碳酸钠溶液中通入CO2的目的有
③试剂a是
(2)称取一定质量的纯净FeCO3放入硬质玻璃管中(装置如图2),打开K,通入氧气,加热硬质玻璃管。乙瓶中澄清石灰水不再产生沉淀时,停止加热,继续通入氧气至玻璃管冷却,称量剩余固体的质量。

若开始时称取23.2gFeCO3固体,反应后称得剩余固体质量为16.0g,写出硬质玻璃管中发生反应的化学方程式:
您最近一年使用:0次
名校
解题方法
3 . 富马酸亚铁又称反丁烯二酸亚铁,是良好的动物铁营养元素补充剂,它以富马酸、碳酸钠和硫酸亚铁作为反应单体,先由富马酸和碳酸钠合成富马酸二钠再与硫酸亚铁反应所得,某化学兴趣小组在实验室中模拟制备富马酸亚铁,实验流程及装置如下图:

(1)仪器A的名称是_______ ,仪器A的作用是_______ 。
(2)称取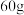 富马酸(反丁烯二酸
富马酸(反丁烯二酸 ,式量为116)置于右边的三颈烧瓶中,根据计算的浓度,称取一定量的水加入三颈烧瓶中,开启搅拌桨搅拌,并开启调温型电热套使温度达到
,式量为116)置于右边的三颈烧瓶中,根据计算的浓度,称取一定量的水加入三颈烧瓶中,开启搅拌桨搅拌,并开启调温型电热套使温度达到 时,加入预先溶解好的
时,加入预先溶解好的 溶液,在生成富马酸二钠约
溶液,在生成富马酸二钠约 后,调节
后,调节 在6.8~7.0之间,继续加热升温,反应
在6.8~7.0之间,继续加热升温,反应 ,即可得到富马酸二钠溶液。写出碳酸钠与富马酸反应的化学方程式:
,即可得到富马酸二钠溶液。写出碳酸钠与富马酸反应的化学方程式:_______ ;富马酸二钠溶液中离子浓度由大到小的顺序是_______ (除 )。
)。

(3)在富马酸二钠溶液中,缓慢加入 溶液,维持温度
溶液,维持温度 ,充分搅拌
,充分搅拌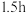 ;在回流过程中一直通入氮气的目的是
;在回流过程中一直通入氮气的目的是_______ 。冷却、过滤,洗涤沉淀,然后水浴干燥,得到粗产品 。若(2)中调节的
。若(2)中调节的 太小,最后得到的粗产品的质量会
太小,最后得到的粗产品的质量会_______ (填“不变”“偏大”或“偏小”,下同),若不通氮气,最后得到的粗产品的质量会_______ 。
(4)洗涤沉淀时的操作为_______ 。
(5)准确称取粗产品 ,加入煮沸过的
,加入煮沸过的 硫酸溶液
硫酸溶液 ,待样品完全溶解后,加煮沸过的冷水配制成
,待样品完全溶解后,加煮沸过的冷水配制成 溶液,取溶液
溶液,取溶液 滴入3滴邻二氮菲-亚铁指示剂,立即用
滴入3滴邻二氮菲-亚铁指示剂,立即用 硫酸高铈铵)
硫酸高铈铵) 标准溶液进行滴定。平行3次实验,用去标准液的体积平均值
标准溶液进行滴定。平行3次实验,用去标准液的体积平均值 (反应方程式为
(反应方程式为 )。计算产品中富马酸亚铁(相对分子质量为170)的质量分数为
)。计算产品中富马酸亚铁(相对分子质量为170)的质量分数为_______ 。

(1)仪器A的名称是
(2)称取
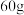 富马酸(反丁烯二酸
富马酸(反丁烯二酸 ,式量为116)置于右边的三颈烧瓶中,根据计算的浓度,称取一定量的水加入三颈烧瓶中,开启搅拌桨搅拌,并开启调温型电热套使温度达到
,式量为116)置于右边的三颈烧瓶中,根据计算的浓度,称取一定量的水加入三颈烧瓶中,开启搅拌桨搅拌,并开启调温型电热套使温度达到 时,加入预先溶解好的
时,加入预先溶解好的 溶液,在生成富马酸二钠约
溶液,在生成富马酸二钠约 后,调节
后,调节 在6.8~7.0之间,继续加热升温,反应
在6.8~7.0之间,继续加热升温,反应 ,即可得到富马酸二钠溶液。写出碳酸钠与富马酸反应的化学方程式:
,即可得到富马酸二钠溶液。写出碳酸钠与富马酸反应的化学方程式: )。
)。
(3)在富马酸二钠溶液中,缓慢加入
 溶液,维持温度
溶液,维持温度 ,充分搅拌
,充分搅拌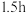 ;在回流过程中一直通入氮气的目的是
;在回流过程中一直通入氮气的目的是 。若(2)中调节的
。若(2)中调节的 太小,最后得到的粗产品的质量会
太小,最后得到的粗产品的质量会(4)洗涤沉淀时的操作为
(5)准确称取粗产品
 ,加入煮沸过的
,加入煮沸过的 硫酸溶液
硫酸溶液 ,待样品完全溶解后,加煮沸过的冷水配制成
,待样品完全溶解后,加煮沸过的冷水配制成 溶液,取溶液
溶液,取溶液 滴入3滴邻二氮菲-亚铁指示剂,立即用
滴入3滴邻二氮菲-亚铁指示剂,立即用 硫酸高铈铵)
硫酸高铈铵) 标准溶液进行滴定。平行3次实验,用去标准液的体积平均值
标准溶液进行滴定。平行3次实验,用去标准液的体积平均值 (反应方程式为
(反应方程式为 )。计算产品中富马酸亚铁(相对分子质量为170)的质量分数为
)。计算产品中富马酸亚铁(相对分子质量为170)的质量分数为
您最近一年使用:0次
2021-09-24更新
|
453次组卷
|
5卷引用:青海省西宁市大通回族土族自治县2022届高三开学摸底考试化学试题



