名校
解题方法
1 . 今有一混合物的水溶液,只可能含有以下离子中的若干种:K+、Al3+、Fe3+、Mg2+、Ba2+、NH 、Cl﹣、CO
、Cl﹣、CO 、SO
、SO ,现取三份100mL溶液进行如下实验:
,现取三份100mL溶液进行如下实验:
第一份加入AgNO3溶液有沉淀产生;
第二份加足量NaOH溶液加热后,只收集到气体0.02mol,无沉淀生成,同时得到溶液甲;在甲溶液中通入过量CO2,生成白色沉淀,沉淀经过滤、洗涤、灼烧,质量为1.02g。
第三份加足量BaCl2溶液后,得白色沉淀,沉淀经足量盐酸洗涤、干燥后,质量为11.65g.{已知:NaAlO2+2H2O+CO2═NaHCO3+Al(OH)3↓}。根据上述实验回答:
(1)一定不存在的离子是____________ ,不能确定是否存在的离子是____________ .
(2)试确定溶液中肯定存在的离子及其浓度:
离子符号_________ ,浓度________________ ;
离子符号_________ ,浓度________________ ;
离子符号_________ ,浓度________________ .
(3)试确定K+是否存在________ ,判断的理由是________________________________
 、Cl﹣、CO
、Cl﹣、CO 、SO
、SO ,现取三份100mL溶液进行如下实验:
,现取三份100mL溶液进行如下实验:第一份加入AgNO3溶液有沉淀产生;
第二份加足量NaOH溶液加热后,只收集到气体0.02mol,无沉淀生成,同时得到溶液甲;在甲溶液中通入过量CO2,生成白色沉淀,沉淀经过滤、洗涤、灼烧,质量为1.02g。
第三份加足量BaCl2溶液后,得白色沉淀,沉淀经足量盐酸洗涤、干燥后,质量为11.65g.{已知:NaAlO2+2H2O+CO2═NaHCO3+Al(OH)3↓}。根据上述实验回答:
(1)一定不存在的离子是
(2)试确定溶液中肯定存在的离子及其浓度:
离子符号
离子符号
离子符号
(3)试确定K+是否存在
您最近一年使用:0次
2 . 某强酸性溶液X,可能含有Al3+、Ba2+、NH4+、Fe2+、Na+、CO32﹣、SO42﹣、SiO32﹣、NO3﹣中的一种或几种离子,取该溶液进行实验,其现象及转化如下图所示。
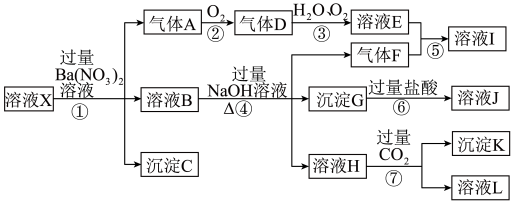
请回答下列问题:
(1)由整体的实验过程可判断溶液X中一定不存在的阴离子有______ 。
(2)产生气体A的离子方程式为____________ 。
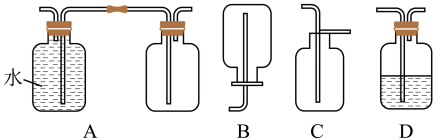
(3)在实验室中收集气体A,可选择如图装置中的______ 。
(4)写出④反应中生成溶液H的离子方程式____________ 。
(5)对不能确定是否存在的离子,请简述检测实验方案__________ 。

请回答下列问题:
(1)由整体的实验过程可判断溶液X中一定不存在的阴离子有
(2)产生气体A的离子方程式为
(3)在实验室中收集气体A,可选择如图装置中的

(4)写出④反应中生成溶液H的离子方程式
(5)对不能确定是否存在的离子,请简述检测实验方案
您最近一年使用:0次
2019-02-12更新
|
392次组卷
|
2卷引用:【全国百强校】陕西省西安市长安区第一中学2018-2019学年高一上学期期末考试化学试题
3 . 下列有关离子检验的操作及结论均正确的是
| A.向无色溶液中先加适量盐酸酸化,再加AgNO3溶液,产生白色沉淀,则该溶液中一定含有Cl- |
| B.向无色溶液中加入BaCl2溶液有白色沉淀出现,再加盐酸,沉淀不消失,则该溶液中一定含有SO42- |
| C.向无色溶液中加入稀盐酸,产生能使澄清石灰水变浑浊的无色气体,则该溶液中一定含有CO32- |
| D.向某溶液中加入氢氧化钠溶液并加热,产生能使湿润的红色石蕊试纸变蓝的气体,则该溶液中一定含有NH4+ |
您最近一年使用:0次
2019-01-29更新
|
554次组卷
|
3卷引用:【市级联考】江苏省扬州市2018-2019学年高一第一学期期末调研化学试题
名校
4 . 某澄清溶液可能含有K+、Al3+、Mg2+、NH4+、Fe2+、Fe3+、Cu2+、SO42-、CO32-中的一种或几种,为确定其成分,进行如下实验:①取部分溶液,逐滴滴入用HCl酸化的BaCl2溶液,产生白色沉淀;②另取部分溶液,缓慢加入足量的Na2O2固体并加热,产生无色无味的气体,同时产生白色沉淀后白色沉淀部分溶解。下列推断正确的是
| A.肯定有Al3+、SO42-,可能有K+、NH4+ |
| B.肯定无Fe2+、Mg2+、CO32-,可能有Al3+ |
| C.原溶液一定是明矾和MgSO4的混合溶液 |
| D.不能确定的离子只能通过焰色反应来确定 |
您最近一年使用:0次
2018-07-26更新
|
430次组卷
|
2卷引用:辽宁省盘锦市高级中学2017-2018学年高二下学期期末考试化学试题
5 . 氯化铁和高铁酸钾都是常见的水处理剂。某兴趣小组以铁屑为原料模拟工业上制备氯化铁及进一步氧化制备高铁酸钾的流程如下:
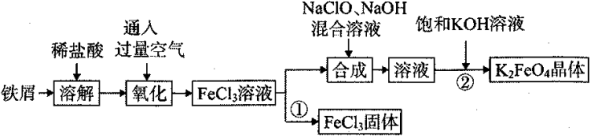
请回答下列问题:
(1)“氧化”阶段通入过量空气比用氯气作氧化剂具有的优点是____________ 。
(2)“合成”阶段生成Na2FeO4的离子方程式为___________________________ 。
(3)为了检验“氧化”过程中所得FeCl3 溶液中是否含有Fe2+,某同学取少量溶液于试管中,选用下列试剂可以达到目的的是_______ (填字母)。
a.KSCN溶液 b.NaOH溶液 c.K3[Fe(CN)6]溶液 d.苯酚溶液
若选用酸性KMnO4溶液进行检验,请分析方案是否合理,并说明理由:____________ 。
(4)过程①制取FeCl3固体的具体操作步骤是__________________________ 。若使6.4mol/LFeCl3饱和溶液不析出Fe(OH)3,需控制溶液的pH小于____ 。{已知该实验条件下,Ksp[(Fe(OH)3]=8.5×10-36,Kw=1.1×10-13,1.13≈1.33}
(5)在不同温度和不同pH 下,FeO42-的稳定性如下图所示:
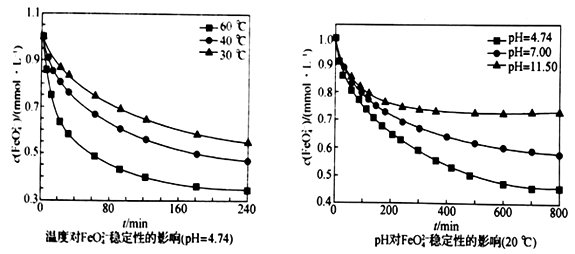
从上图分析,为了提高“合成”阶段Na2FeO4的产率,可采取的实验条件范围为______________________ 。

请回答下列问题:
(1)“氧化”阶段通入过量空气比用氯气作氧化剂具有的优点是
(2)“合成”阶段生成Na2FeO4的离子方程式为
(3)为了检验“氧化”过程中所得FeCl3 溶液中是否含有Fe2+,某同学取少量溶液于试管中,选用下列试剂可以达到目的的是
a.KSCN溶液 b.NaOH溶液 c.K3[Fe(CN)6]溶液 d.苯酚溶液
若选用酸性KMnO4溶液进行检验,请分析方案是否合理,并说明理由:
(4)过程①制取FeCl3固体的具体操作步骤是
(5)在不同温度和不同pH 下,FeO42-的稳定性如下图所示:

从上图分析,为了提高“合成”阶段Na2FeO4的产率,可采取的实验条件范围为
您最近一年使用:0次
2018-03-15更新
|
773次组卷
|
3卷引用:河北省衡水中学2018年高三下学期期初考试(3月)理综化学试题
6 . 下列有关离子检验的操作、现象及结论均正确的是
| A.用洁净的铂丝蘸取少量溶液在酒精灯火焰上灼烧,火焰呈黄色,则该溶液中一定不含K+ |
| B.向无色溶液中加入盐酸酸化的BaCl2溶液有白色沉淀出现,则该溶液中一定含有SO42﹣ |
| C.向无色溶液中加入盐酸产生能使澄清石灰水变浑浊的气体,则该溶液中一定含有CO32﹣ |
| D.向某溶液中加入KSCN溶液无现象,再滴入少量H2O2 , 呈血红色,则该溶液中一定含有Fe2+ |
您最近一年使用:0次
2018-01-10更新
|
222次组卷
|
3卷引用:河北省唐山一中2017-2018学年高一上学期第二次月考化学试题
名校
7 . 某无色溶液可能含有NH4+、Ba2+、Fe2+、Ag+、OH-、SO42-、CO32-、NO3-中的一种或几种。现用该溶液进行一下实验:
①取此溶液少许,加足量盐酸,无明现象
②另取少许溶液加入足量Na2SO4溶液,有白色沉淀生成
③将②中的沉淀过滤,取滤液加入NaOH溶液微热,有无色刺激性气体放出,该气体能使湿润红色石蕊试纸变蓝。下列推断正确的是
①取此溶液少许,加足量盐酸,无明现象
②另取少许溶液加入足量Na2SO4溶液,有白色沉淀生成
③将②中的沉淀过滤,取滤液加入NaOH溶液微热,有无色刺激性气体放出,该气体能使湿润红色石蕊试纸变蓝。下列推断正确的是
| A.溶液中一定不存在Fe2+、CO32-、Ag+、OH-、SO42- |
| B.溶液中一定存在NH 4 +、Ba 2+ 、NO3 - |
| C.溶液中一定存在NH4+、Ba2+可能存在NO3- |
| D.溶液中一定存在OH-、NH4+、Ba2+、NO3- |
您最近一年使用:0次
8 . 确定某无色溶液中含某离子,下列结论正确的是( )
| A.加AgNO3溶液,生成白色沉淀,加稀盐酸沉淀不消失,可确定有Cl﹣存在 |
| B.加BaCl2溶液,生成白色沉淀,加稀盐酸沉淀不消失,可确定有SO42﹣存在 |
| C.加盐酸,生成的气体能使澄清石灰水变浑浊,可确定有大量CO32﹣存在 |
| D.通入Cl2后,溶液变为黄色,加入淀粉溶液后溶液变蓝,可确定有I﹣存在 |
您最近一年使用:0次
2017-11-28更新
|
660次组卷
|
4卷引用:陕西省西安市长安区第一中学2017-2018学年高一上学期期中考试化学试题
陕西省西安市长安区第一中学2017-2018学年高一上学期期中考试化学试题北京市海淀区19中2019-2020学年高一下学期期末考试化学试题河北省石家庄市正定中学2022-2023学年高一上学期第二次月考化学试题(已下线)【2023】【高一下】【其他】【余高2】【高中化学】【刘尼尼收集】
名校
解题方法
9 . 某无色溶液中可能含有下列几种离子中的某几种:Ca2+、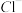 、
、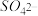 、
、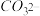 、
、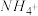 、
、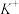 、Cu2+。为确认溶液组成进行如下实验:(1)200mL上述溶液,加入足量
、Cu2+。为确认溶液组成进行如下实验:(1)200mL上述溶液,加入足量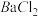 溶液,反应后将沉淀过滤、洗涤、干燥,得沉淀4.30g,向沉淀中加入过量的盐酸,有2.33g沉淀不溶。(2)向(1)的滤液中加入足量的
溶液,反应后将沉淀过滤、洗涤、干燥,得沉淀4.30g,向沉淀中加入过量的盐酸,有2.33g沉淀不溶。(2)向(1)的滤液中加入足量的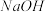 溶液,加热,产生能促使湿润红色石蕊试纸变蓝的气体1.12L(已换算成标准状况,假定产生的气体全部逸出)。由此可以得出关于原溶液组成的正确结论是
溶液,加热,产生能促使湿润红色石蕊试纸变蓝的气体1.12L(已换算成标准状况,假定产生的气体全部逸出)。由此可以得出关于原溶液组成的正确结论是
(1)溶液中一定不存在的离子是__ ,不能确定是否存在的离子是__ .为确定该离子,应当补充的实验名称是______________
(2)溶液中肯定存在的阴离子有哪些?通过计算求出它们的物质的量浓度(或范围)。______________
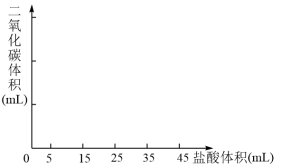
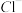 、
、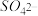 、
、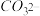 、
、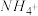 、
、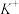 、Cu2+。为确认溶液组成进行如下实验:(1)200mL上述溶液,加入足量
、Cu2+。为确认溶液组成进行如下实验:(1)200mL上述溶液,加入足量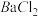 溶液,反应后将沉淀过滤、洗涤、干燥,得沉淀4.30g,向沉淀中加入过量的盐酸,有2.33g沉淀不溶。(2)向(1)的滤液中加入足量的
溶液,反应后将沉淀过滤、洗涤、干燥,得沉淀4.30g,向沉淀中加入过量的盐酸,有2.33g沉淀不溶。(2)向(1)的滤液中加入足量的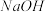 溶液,加热,产生能促使湿润红色石蕊试纸变蓝的气体1.12L(已换算成标准状况,假定产生的气体全部逸出)。由此可以得出关于原溶液组成的正确结论是
溶液,加热,产生能促使湿润红色石蕊试纸变蓝的气体1.12L(已换算成标准状况,假定产生的气体全部逸出)。由此可以得出关于原溶液组成的正确结论是(1)溶液中一定不存在的离子是
(2)溶液中肯定存在的阴离子有哪些?通过计算求出它们的物质的量浓度(或范围)。

您最近一年使用:0次
10 . 根据下列实验操作和现象所得到的结论正确的是
| 选项 | 实验操作和现象 | 结论 |
| A | 向硝酸溶液中加入碳酸钠,有大量气泡产生 | 酸性:碳酸 > 硝酸 |
| B、 | 向1mL 某溶液中,滴入2 mL 0.1 mol·L-1 NaOH溶液,加热,产生使湿润的红色石蕊试纸变蓝的气体 | 某溶液中含NH4+ |
| C、 | 取5 mL 0.1 mol·L-1FeCl3溶液,滴加5滴0.1 mol·L-1KI溶液,振荡,再加入5 mL CCl4,振荡,静置,取上层液体,向取出来的溶液中滴加KSCN溶液,显血红色。 | KI和FeCl3反应有一定的限度 |
| D、 | 加热使冰化成液态水 | 分子内H-O键发生断裂 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次



