名校
1 . 通过对实验现象的观察、分析推理得出正确的结论是化学学习的方法之一。对下列实验事实的解释正确的是
| 选项 | 现象 | 解释 |
| A | KI淀粉溶液中通入Cl2,溶液变蓝 | Cl2能与淀粉发生显色反应 |
| B | 测得饱和NaA溶液的pH大于饱和NaB溶液 | 常温下水解程度:A->B- |
| C | 往乙醇中加入适量浓硫酸制备乙烯,并将产生的气体直接通入酸性高锰酸钾溶液中,溶液紫红色褪去 | 证明乙烯能被酸性高锰酸钾氧化 |
| D | 常温下,SO2能使酸性高锰酸钾溶液褪色 | SO2具有还原性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2 . 下列对实验的分析不合理的是
| 实验1 | 实验2 | 实验3 | |
| 装置 | 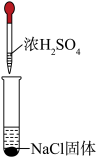 | 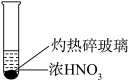 | 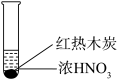 |
| 现象 | 溶液颜色无明显变化;把蘸浓氨水的玻璃棒靠近试管口,产生白烟 | 产生红棕色气体 | 产生红棕色气体 |
| A.实验1中的白烟是NH4Cl的固体小颗粒 |
| B.由实验2中的红棕色气体可以推断产生的气体一定是混合气体 |
| C.实验3中的红棕色气体不一定能说明木炭与浓硝酸发生了反应 |
| D.上述实验体现了浓H2SO4的难挥发性和浓硝酸的强氧化性 |
您最近一年使用:0次
3 . 乙醇与浓硫酸在装置A中反应制取乙烯,因温度控制不当而发生副反应生成SO2、CO2、水蒸气等,设计如图实验装置以验证反应生成的混合气体中含乙烯、SO2和水蒸气。该实验限用试剂(试剂足量)包括:品红溶液、氢氧化钠溶液、酸性高锰酸钾溶液、溴水。下列说法错误的是
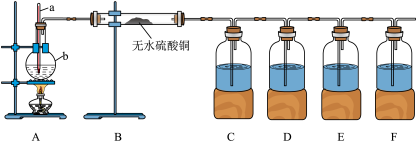
| A.仪器b的名称为圆底烧瓶 |
| B.洗气瓶D中的试剂为氢氧化钠溶液,其作用为除去SO2 |
| C.洗气瓶C中的试剂为品红溶液,可用来检验SO2 |
| D.装置B用来检验混合气体中的水蒸气,也可置于C、D之间 |
您最近一年使用:0次
4 . 用试纸检验气体性质是一种重要的实验方法.如表所示的实验中 可加热
可加热 ,下列试纸的选用、现象、对应结论都正确的一项是
,下列试纸的选用、现象、对应结论都正确的一项是
 可加热
可加热 ,下列试纸的选用、现象、对应结论都正确的一项是
,下列试纸的选用、现象、对应结论都正确的一项是
| 序号 | 试剂B | 湿润的试纸A | 结论 |
| A | 碘水 | 淀粉试纸变蓝 | 碘具有氧化性 |
| B | 浓氨水、生石灰 | 蓝色石蕊试纸变红 | 氨气为碱性气体 |
| C |  、硫酸 、硫酸 | 品红试纸褪色 |  具有漂白性 具有漂白性 |
| D | Cu、浓硝酸 | 淀粉KI试纸变蓝 |  为酸性气体 为酸性气体 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2020-01-21更新
|
334次组卷
|
12卷引用:2011-2012学年赤峰市第二实验中学高一下学期期末考试化学试卷
(已下线)2011-2012学年赤峰市第二实验中学高一下学期期末考试化学试卷2014-2015天津市和平区高一上学期期末考试化学试卷2016届江西省吉安一中高三上学期期中测试化学试卷2016届广东省东莞市松山湖莞美学校高三上学期12月月考理综化学试卷陕西省西安市第一中学2017-2018学年高一上学期期末考试化学试题山东省师范大学附中2020届高三第三次月考化学试题河北省辛集中学2020届高三第三次阶段考试化学试题2020届高三化学二轮冲刺新题专练——药品的保存和使用、指示剂试纸的使用(提升练)江西省宜春市奉新县第一中学2020届高三上学期第四次月考化学试题辽宁省抚顺市抚顺县高级中学2021-2022学年高三10月月考化学试题陕西省西安市第一中学2022-2023学年高一下学期5月月考化学试题天津市军粮城中学2023-2024学年高一下学期第一次月考化学试卷
名校
解题方法
5 . 已知硫酸亚铁铵[ ](俗称莫尔盐)可溶于水,在
](俗称莫尔盐)可溶于水,在 时分解,其探究其化学性质,甲、乙两同学设计了如下实验。
时分解,其探究其化学性质,甲、乙两同学设计了如下实验。
Ⅰ. 探究莫尔盐晶体加热时的分解产物。
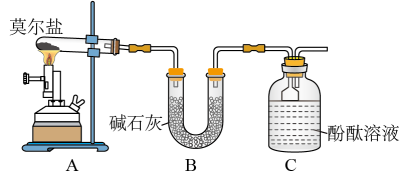
(1)甲同学设计如图所示的装置进行实验。装置C中可观察到的现象是_______ ,由此可知分解产物中有_______ (填化学式)。
(2)乙同学认为莫尔盐晶体分解的产物中还可能含有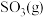 、
、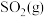 及
及 。为验证产物的存在,用下列装置进行实验。
。为验证产物的存在,用下列装置进行实验。
①乙同学的实验中,装置依次连按的合理顺序为:A→H→→→→G。_______
②证明含有 的实验现象是
的实验现象是_______ 。
Ⅱ. 为测定硫酸亚铁铵纯度,称取mg莫尔盐样品,配成 溶液。甲、乙两位同学设计了如下两个实验方案。
溶液。甲、乙两位同学设计了如下两个实验方案。
甲方案:取 样品溶液用
样品溶液用 的酸性
的酸性 溶液分三次进行测定。
溶液分三次进行测定。
乙方案(通过 测定):实验设计装置如图所示。取
测定):实验设计装置如图所示。取 样品溶液进行该实验。
样品溶液进行该实验。
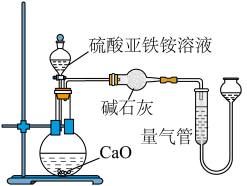
请回答:
(3)乙方案中量气管中最佳试剂是_______ 。
a. 水 b. 饱和 溶液 c.
溶液 c.  d. 饱和
d. 饱和 溶液
溶液
(4)乙方案中收集完气体并恢复至室温,为了减小实验误差,读数前应进行的操作是_______ 。
(5)若测得 为VL(已折算为标准状况下),则硫酸亚铁铵纯度为
为VL(已折算为标准状况下),则硫酸亚铁铵纯度为_______ (列出计算式)。
 ](俗称莫尔盐)可溶于水,在
](俗称莫尔盐)可溶于水,在 时分解,其探究其化学性质,甲、乙两同学设计了如下实验。
时分解,其探究其化学性质,甲、乙两同学设计了如下实验。Ⅰ. 探究莫尔盐晶体加热时的分解产物。
(1)甲同学设计如图所示的装置进行实验。装置C中可观察到的现象是

(2)乙同学认为莫尔盐晶体分解的产物中还可能含有
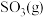 、
、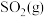 及
及 。为验证产物的存在,用下列装置进行实验。
。为验证产物的存在,用下列装置进行实验。 | 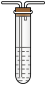 |  | 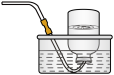 |  |
| D. 品红溶液 | E.  溶液 溶液 | F.  溶液和足量盐酸 溶液和足量盐酸 | G. 排水集气法 | H.安全瓶 |
②证明含有
 的实验现象是
的实验现象是Ⅱ. 为测定硫酸亚铁铵纯度,称取mg莫尔盐样品,配成
 溶液。甲、乙两位同学设计了如下两个实验方案。
溶液。甲、乙两位同学设计了如下两个实验方案。甲方案:取
 样品溶液用
样品溶液用 的酸性
的酸性 溶液分三次进行测定。
溶液分三次进行测定。乙方案(通过
 测定):实验设计装置如图所示。取
测定):实验设计装置如图所示。取 样品溶液进行该实验。
样品溶液进行该实验。
请回答:
(3)乙方案中量气管中最佳试剂是
a. 水 b. 饱和
 溶液 c.
溶液 c.  d. 饱和
d. 饱和 溶液
溶液(4)乙方案中收集完气体并恢复至室温,为了减小实验误差,读数前应进行的操作是
(5)若测得
 为VL(已折算为标准状况下),则硫酸亚铁铵纯度为
为VL(已折算为标准状况下),则硫酸亚铁铵纯度为
您最近一年使用:0次
2023-01-21更新
|
754次组卷
|
3卷引用:山东省青岛第五十八中学2022-2023学年高一上学期期末考试化学试题
6 . 室温下(20oC))课外小组用下列装置探究铁和硝酸反应情况,过程如下图所示:
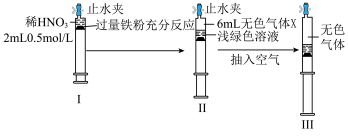
将Ⅲ中液面上的气体排入小试管中点燃,有尖锐爆鸣声,小试管壁出现液滴。取反应后溶液,加入足量NaOH 溶液得到灰绿色沉淀。煮沸时,蒸气带有刺激性气味并能使湿润红色石蕊试纸变蓝。
(1)X气体是______ (填化学式),证据是________ 。
(2)实验中硝酸被还原成另一种产物的化学方程式_____ 。
(3)甲同学对产生的气体原因提出假设并设计方案:
假设1:该浓度的硝酸中H+的氧化性大于NO3-
假设2:H+还原反应速率大于NO3-的还原反应速率
I. 验证假设1:可用____ (选 “ Cu” 或“Zn”)粉与同浓度硝酸反应,依据 ____________ ,则假设1不成立。
II. 验证假设2:改变条件重复上图过程实验,结果如下:(所用试剂的量、气体成分与实验上图相同)
上表实验结果_____ (填“能”或“否”)判断假设2成立。由实验数据结果分析温度对铁粉与硝酸反应时对生成X体积的影响的原因___________ 。
(4)常温下(20℃),乙同学改用3mol·L–1 HNO3进行图1过程实验,Ⅱ中仍为无色气体,在Ⅲ中气体变红色。由此得出的相关结论正确的是______ 。
a. 该实验产生的无色气体只有NO
b. 若改用浓硝酸时,反应会更剧烈还原产物为NO2
c. 硝酸的浓度不同时,其主要还原产物不同
(5)综上所述,金属与硝酸生成X气体,需要控制的条件是___________ 。

将Ⅲ中液面上的气体排入小试管中点燃,有尖锐爆鸣声,小试管壁出现液滴。取反应后溶液,加入足量NaOH 溶液得到灰绿色沉淀。煮沸时,蒸气带有刺激性气味并能使湿润红色石蕊试纸变蓝。
(1)X气体是
(2)实验中硝酸被还原成另一种产物的化学方程式
(3)甲同学对产生的气体原因提出假设并设计方案:
假设1:该浓度的硝酸中H+的氧化性大于NO3-
假设2:H+还原反应速率大于NO3-的还原反应速率
I. 验证假设1:可用
II. 验证假设2:改变条件重复上图过程实验,结果如下:(所用试剂的量、气体成分与实验上图相同)
| 序号 | 反应温度 | 实验结果 |
| a | 40oC | 溶液浅绿色,收集气体为3.4mL |
| b | 60oC | 溶液浅绿色,收集气体为2.6mL |
上表实验结果
(4)常温下(20℃),乙同学改用3mol·L–1 HNO3进行图1过程实验,Ⅱ中仍为无色气体,在Ⅲ中气体变红色。由此得出的相关结论正确的是
a. 该实验产生的无色气体只有NO
b. 若改用浓硝酸时,反应会更剧烈还原产物为NO2
c. 硝酸的浓度不同时,其主要还原产物不同
(5)综上所述,金属与硝酸生成X气体,需要控制的条件是
您最近一年使用:0次
2019-03-28更新
|
393次组卷
|
2卷引用:【区级联考】北京市平谷区2019届高三下学期质量监控化学试题
7 . 下列有关实验装置、操作,不能实现相应实验目的的是
| A | B | C | D | |
| 装置 | 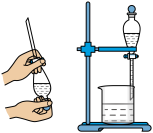 | 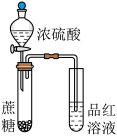 |  | 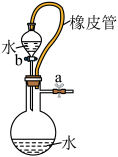 |
| 目的 | 用KOH溶液除去溴苯中单质溴 | 证明浓硫酸有脱水性、强氧化性 | 先出现白色沉淀,后出现砖红色沉淀,证明Ksp(AgCl)< Ksp(Ag2CrO4) | 不能通过观察水能否全部流下来判断装置气密性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
8 . 摩尔盐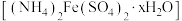 比一般的亚铁盐更稳定,是一种重要的定量分析化学试剂。回答下列问题:
比一般的亚铁盐更稳定,是一种重要的定量分析化学试剂。回答下列问题:
(1)制备摩尔盐采用的方法是先在封闭体系中利用铁和稀硫酸反应制备硫酸亚铁溶液,再用新制的硫酸亚铁溶液和硫酸按饱和溶液反应制得。配制硫酸按饱和溶液的蒸馏水,需经煮沸并迅速冷却后再使用,目的是___________ 。
(2)可以采用热重分析法测定摩尔盐样品中所含结晶水的个数,加热其晶体需要使用的实验仪器除了玻璃棒、三脚架、泥三角、酒精灯外,还需要的仪器有___________ 。取样品 加热至两次质量恒重为
加热至两次质量恒重为 (假设减少的质量仅仅是晶体失水),则x的表达式为
(假设减少的质量仅仅是晶体失水),则x的表达式为___________ (用含a、b的代数式表示)。
(3)利用摩尔盐分解产生的 ,可制取氯化亚砜
,可制取氯化亚砜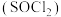 :
: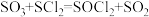 。已知
。已知 是一种液态化合物,遇水产生白雾和一种刺激性气体。利用如图装置制取
是一种液态化合物,遇水产生白雾和一种刺激性气体。利用如图装置制取 并检验生成的
并检验生成的 。
。
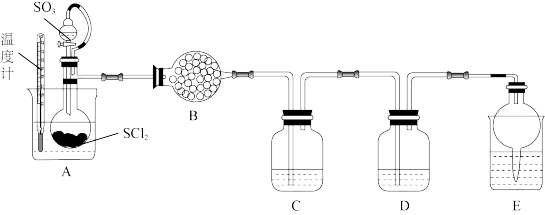
①装置B为无水 ,其作用是
,其作用是___________ 。
②装置C和装置D中的试剂分别是___________ 、___________ (填小写字母)。
a. 溶液 b.
溶液 b. 和
和 溶液 c.
溶液 c. 溶液 d.饱和的
溶液 d.饱和的 溶液
溶液
(4)利用摩尔盐分解产生的 ,设计实验探究亚硫酸与次氯酸的酸性强弱。
,设计实验探究亚硫酸与次氯酸的酸性强弱。
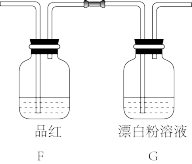
①将少量 气体直接通入装置G中,不能根据装置G中现象判断亚硫酸与次氯酸的酸性强弱,理由是
气体直接通入装置G中,不能根据装置G中现象判断亚硫酸与次氯酸的酸性强弱,理由是___________ (用化学反应方程式表示)。
②为了验证亚硫酸与次氯酸的酸性强弱,需要制备一种中间酸,装置F中另一种试剂是___________ ,其作用是___________ ,通过___________ (填现象)即可证明亚硫酸的酸性强于次氯酸。
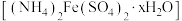 比一般的亚铁盐更稳定,是一种重要的定量分析化学试剂。回答下列问题:
比一般的亚铁盐更稳定,是一种重要的定量分析化学试剂。回答下列问题:(1)制备摩尔盐采用的方法是先在封闭体系中利用铁和稀硫酸反应制备硫酸亚铁溶液,再用新制的硫酸亚铁溶液和硫酸按饱和溶液反应制得。配制硫酸按饱和溶液的蒸馏水,需经煮沸并迅速冷却后再使用,目的是
(2)可以采用热重分析法测定摩尔盐样品中所含结晶水的个数,加热其晶体需要使用的实验仪器除了玻璃棒、三脚架、泥三角、酒精灯外,还需要的仪器有
 加热至两次质量恒重为
加热至两次质量恒重为 (假设减少的质量仅仅是晶体失水),则x的表达式为
(假设减少的质量仅仅是晶体失水),则x的表达式为(3)利用摩尔盐分解产生的
 ,可制取氯化亚砜
,可制取氯化亚砜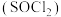 :
: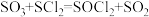 。已知
。已知 是一种液态化合物,遇水产生白雾和一种刺激性气体。利用如图装置制取
是一种液态化合物,遇水产生白雾和一种刺激性气体。利用如图装置制取 并检验生成的
并检验生成的 。
。
①装置B为无水
 ,其作用是
,其作用是②装置C和装置D中的试剂分别是
a.
 溶液 b.
溶液 b. 和
和 溶液 c.
溶液 c. 溶液 d.饱和的
溶液 d.饱和的 溶液
溶液(4)利用摩尔盐分解产生的
 ,设计实验探究亚硫酸与次氯酸的酸性强弱。
,设计实验探究亚硫酸与次氯酸的酸性强弱。
①将少量
 气体直接通入装置G中,不能根据装置G中现象判断亚硫酸与次氯酸的酸性强弱,理由是
气体直接通入装置G中,不能根据装置G中现象判断亚硫酸与次氯酸的酸性强弱,理由是②为了验证亚硫酸与次氯酸的酸性强弱,需要制备一种中间酸,装置F中另一种试剂是
您最近一年使用:0次
2022-07-15更新
|
302次组卷
|
2卷引用:河南省开封市五县2021-2022学年高二下学期期末考试化学试题
9 . 下列物质性质与应用对应关系正确的是
| A.二氧化锰具有还原性,可用于实验室制备氯气 |
| B.Na2O2能与水或二氧化碳反应生成氧气,可用作供氧剂 |
| C.碳酸氢钠能与碱反应,可用作食品的膨松剂 |
| D.证明一瓶红棕色气体是溴蒸气还是二氧化氮,可用湿润的碘化钾-淀粉试纸检验,观察试纸颜色的变化 |
您最近一年使用:0次
10 . 已知草酸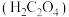 是一种弱酸,
是一种弱酸,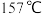 升华,
升华, 以上分解可放出
以上分解可放出 和CO;可与酸性
和CO;可与酸性 溶液反应;其钠盐易溶于水,钙盐难溶于水。下列说法正确的是
溶液反应;其钠盐易溶于水,钙盐难溶于水。下列说法正确的是

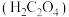 是一种弱酸,
是一种弱酸,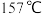 升华,
升华, 以上分解可放出
以上分解可放出 和CO;可与酸性
和CO;可与酸性 溶液反应;其钠盐易溶于水,钙盐难溶于水。下列说法正确的是
溶液反应;其钠盐易溶于水,钙盐难溶于水。下列说法正确的是

| A.草酸受热产生的气体,用足量的NaOH溶液充分吸收后,可收集得到纯净的CO |
| B.草酸受热产生的气体通过灼热的氧化铜,若出现黑色变红色现象,则说明产生的气体中一定有CO |
C.草酸受热产生的气体直接通入足量的澄清石灰水中,若能产生白色浑浊现象,则说明产生的气体中一定有 |
D.将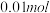 草酸晶体 草酸晶体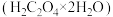 加入到 加入到 的NaOH溶液中充分反应,测得反应后溶液呈碱性,其原因是 的NaOH溶液中充分反应,测得反应后溶液呈碱性,其原因是 水解 水解 |
您最近一年使用:0次
2019-08-10更新
|
306次组卷
|
2卷引用:浙江省温州市十校联合体2018-2019学年高二上学期期末化学试题



