1 . 为探究 的性质,进行了如下实验(
的性质,进行了如下实验( 和
和 溶液浓度均为
溶液浓度均为 )。
)。
依据上述实验现象,结论不合理的是
 的性质,进行了如下实验(
的性质,进行了如下实验( 和
和 溶液浓度均为
溶液浓度均为 )。
)。| 实验 | 操作与现象 |
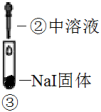
| ① | 在 水中滴加2滴 水中滴加2滴 溶液,呈棕黄色;煮沸,溶液变红褐色。 溶液,呈棕黄色;煮沸,溶液变红褐色。 |
| ② | 在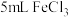 溶液中滴加2滴 溶液中滴加2滴 溶液,变红褐色; 溶液,变红褐色;再滴加  溶液,产生蓝色沉淀。 溶液,产生蓝色沉淀。 |
| ③ | 在 溶液中滴加2滴 溶液中滴加2滴 溶液,变红褐色; 溶液,变红褐色;将上述混合液分成两份,一份滴加  溶液,无蓝色沉淀生成; 溶液,无蓝色沉淀生成;另一份煮沸,产生红褐色沉淀。 |
A.实验①说明加热促进 水解反应 水解反应 |
B.实验②说明 既发生了水解反应,又发生了还原反应 既发生了水解反应,又发生了还原反应 |
C.实验③说明 发生了水解反应,但没有发生还原反应 发生了水解反应,但没有发生还原反应 |
D.整个实验说明 对 对 的水解反应无影响,但对还原反应有影响 的水解反应无影响,但对还原反应有影响 |
您最近一年使用:0次
2022-06-10更新
|
12788次组卷
|
48卷引用:山西省运城市河津中学2023-2024学年高二下学期开学考试化学试题
山西省运城市河津中学2023-2024学年高二下学期开学考试化学试题2022年新高考湖南化学高考真题(已下线)2022年湖南卷高考真题变式题(11-14)(已下线)专题10 水溶液中的离子平衡-2022年高考真题模拟题分项汇编(已下线)专题11 化学实验基础-2022年高考真题模拟题分项汇编(已下线)专题11 化学实验基础-三年(2020-2022)高考真题分项汇编(已下线)专题12 化学实验方案的设计与评价-三年(2020-2022)高考真题分项汇编(已下线)考点14 铁及其化合物-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)第06讲 氧化还原反应(练)-2023年高考化学一轮复习讲练测(全国通用)(已下线)考点28 盐类的水解-备战2023年高考化学一轮复习考点帮(全国通用)内蒙古通辽市开鲁县第一中学2021-2022学年高二下学期6月检测化学试题(已下线)第03讲 氧化还原反应(讲)-2023年高考化学一轮复习讲练测(新教材新高考)(已下线)考点53 化学实验方案设计与评价-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)第07练 铁及其化合物-2023年高考化学一轮复习小题多维练(全国通用)湖北省荆州市公安县第三中学2022-2023学年高三上学期8月月考化学试题山东省枣庄市第三中学2022-2023学年高三上学期开学考试化学试题(已下线)第23讲 盐类水解 (讲)-2023年高考化学一轮复习讲练测(新教材新高考)湖南省株洲市攸县第三中学2022-2023学年高三上学期第一次月考化学试题广东省广州市海珠外国语实验中学2022-2023学年高三上学期第二次阶段性考试化学试题(已下线)易错点34 化学实验方案的设计与评价-备战2023年高考化学考试易错题河北省石家庄市第二中学2022-2023学年高二上学期10月月考化学试题(已下线)专题06 水溶液中的离子平衡(讲)-2023年高考化学二轮复习讲练测(新高考专用)宁夏银川外国语实验学校2023届高三上学期第二次月考化学试题(已下线)专题九 物质结构与性质-实战高考·二轮复习核心突破河南省顶级名校2022-2023学年高三上学期12月摸底考试化学试题辽宁省大连市滨城高中联盟2022-2023学年高二上学期期中考试化学试题坚持素养导向 突出创新命题湖南省长沙市第一中学2022-2023学年高三上学期月考卷(五)化学试题(已下线)第一部分 二轮专题突破 专题18 物质检验、鉴别简单实验方案的设计及评价湖南省攸县第三中学2022-2023学年高三第六次月考化学试题趋势1 创新命题形式河南省商丘市第一高级中学2022-2023学年高二上学期期末考试化学试题(已下线)题型181 “实验-现象-结论”微型实验方案的设计与评价(已下线)题型45 物质性质探究型综合实验(已下线)专题14 化学实验方案的设计与评价(已下线)专题14 化学实验方案的设计与评价(已下线)考点14 铁及其化合物(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)(已下线)考点巩固卷12 化学实验基础(一)(3大考点67题)-2024年高考化学一轮复习考点通关卷(新高考通用)(已下线)专题09 水溶液中的离子平衡-2023年高考化学真题题源解密(新高考专用)(已下线)专题05 化学实验基础-2023年高考化学真题题源解密(全国通用)辽宁省沈阳市第二中学2023-2024学年高三上学期开学暑假阶段验收化学测试题河北省石家庄市第二中学2022-2023学年高三下学期2月月考化学试题(已下线)考点48 实验方案设计与评价(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)(已下线)考点3 盐类水解(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)(已下线)第4讲 盐类的水解山东省枣庄市第三中学2023-2024学年高三上学期10月月考化学试题辽宁省沈阳市第二中学2023-2024学年高三上学期开学考试化学试题(已下线)第04讲 氧化还原反应的基本概念和规律(练习)-【上好课】2025年高考化学一轮复习讲练测(新教材新高考)
2 . 为探究Na2SO3的性质,实验小组同学进行了如下实验:

| A.③和④中产生的气体成分完全相同 | B.②和⑥中沉淀的主要成分不同 |
| C.①→②和④→⑥均只发生了复分解反应 | D. 的还原性在酸性条件下增强 的还原性在酸性条件下增强 |
您最近一年使用:0次
2023-04-06更新
|
2581次组卷
|
11卷引用:山西省晋城一中2022-2023学年高一下学期第三次调研考试化学试题
山西省晋城一中2022-2023学年高一下学期第三次调研考试化学试题北京市海淀区2022-2023学年高三下学期期中练习化学试题山东省东营市第一中学2023届高三下学期二模化学试题浙江省杭州第四中学2022-2023学年高一下学期期中考试化学试题(已下线)【2023】【高一下】【期中考】【杭四下沙】【高中化学】【罗梦宇收集】(已下线)题型35 微型成套装置实验流程(已下线)题型45 物质性质探究型综合实验天津市滨海新区2023-2024学年塘沽第一中学高三上学期第二次月考化学试题(已下线)热点19 化学微型实验北京一零一中2023-2024学年高三上学期第一次月考(开学考)化学试卷 北京市顺义区第二中学2023-2024学年高三下学期开学测化学试题
3 . 用图所示装置进行实验,探究硝酸与铁反应的产物。
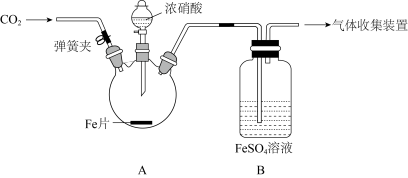
已知:FeSO4+NO=Fe(NO)SO4(棕色) ∆H<0 。
下列说法正确的是

| 主要实验操作 | 实验现象 |
| 打开弹簧夹,通入一段时间CO2后,滴入浓硝酸后无明显现象,加热烧瓶,反应开始后停止加热。 | ①A 中有红棕色气体产生,一段时间后,气体颜色逐渐变浅;反应停止后,A 中无固体剩余。 ②B 中溶液变棕色。 |
| 取少量A 中溶液,加几滴氯水,再滴入硫氰化钾溶液 | ③溶液变为红色 |
| 取少量 B 中溶液,加热 | ④B中棕色溶液变浅,有无色气体逸出,且在空气中变为红棕色 |
下列说法正确的是
| A.滴入浓硝酸加热前没有明显现象的原因是:温度低,反应速率太慢 |
| B.实验现象③说明反应后A 中溶液含有 Fe2+ |
| C.实验现象④说明 A 中有 NO 生成 |
D.可用浓 NaOH 溶液和湿润的红色石蕊试纸检验硝酸的还原产物中是否有 NH |
您最近一年使用:0次
2021-05-21更新
|
1905次组卷
|
8卷引用:山西省长治市2022届高三上学期九月份质量监测化学试题
山西省长治市2022届高三上学期九月份质量监测化学试题湖北省武汉市汉阳一中2021届高三下学期三模化学试题(已下线)第29讲 化学综合实验(精讲)-2022年一轮复习讲练测(已下线)考点12 氮及其化合物-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点12 氮及其化合物-备战2022年高考化学一轮复习考点帮(浙江专用)(已下线)专题13 氮及其化合物 (热点讲义)-2022年高三毕业班化学常考点归纳与变式演练 辽宁省实验中学2021-2022学年高一下学期期中阶段测试化学试题(已下线)第四章 非金属及其化合物 第23练 硝酸 含氮化合物的转化关系
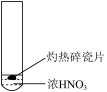
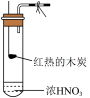
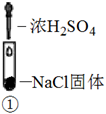
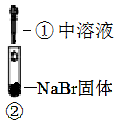
4 . 为探究木炭与浓硝酸的反应原理,某同学设计如下四组实验,发现所有实验过程均有红棕色气体产生,不考虑空气对反应的影响,下列说法错误的是
|
|
|
|
| ① | ② | ③ | ④ |
| A.所有实验产生的气体均为混合物 |
| B.③和④中生成的气体成分可能相同 |
| C.②中红棕色气体全部为木炭与浓硝酸反应产生 |
| D.①说明浓硝酸不稳定受热易分解 |
您最近一年使用:0次
2023-05-27更新
|
385次组卷
|
2卷引用:山西省大同市2022-2023学年高一下学期5月期中考试化学试题
5 . 探究金属与过量浓硫酸反应的装置(固定装置已略去)如下图所示。关于实验操作或叙述错误的是
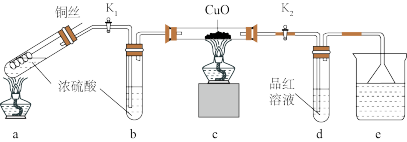

| A.上下抽动铜丝,可控制反应随时发生或停止 |
| B.e中可以选用NaOH溶液或酸性KMnO4溶液 |
| C.其他条件不变,用铁丝代替铜丝,c、d中两次实验现象相同 |
| D.为确定a中白色固体是否是硫酸铜,可向冷却后的试管中注入水,振荡后观察现象 |
您最近一年使用:0次
2020-06-20更新
|
1928次组卷
|
11卷引用:山西师范大学实验中学2021-2022学年高一下学期第二次月考化学试题
山西师范大学实验中学2021-2022学年高一下学期第二次月考化学试题湖北省武汉市2020届高三毕业生六月供题(二)理科综合化学试题湖南省衡阳市第一中学2021届高三上学期第二次月考化学试题(已下线)小题必刷19 硫及其化合物——2021年高考化学一轮复习小题必刷(通用版)山东省济宁市邹城二中2020-2021学年高一下学期6月月考化学试题(已下线)课时22 硫及其化合物-2022年高考化学一轮复习小题多维练(全国通用)湖北省公安县第三中学2020-2021学年高三上学期11月月考化学试题广东省梅州兴宁市沐彬中学2021-2022学年高一下学期 3月月考化学试题福建省厦门市翔安第一中学2023-2024学年高三上学期10月月考化学试题上海市吴淞中学2023-2024学年高一上学期期末质量检测 化学试题广东省揭阳市惠来同仁北实高级中学2023-2024学年高三上学期期中考试化学试题
名校
6 . 研究铜和铁与浓硫酸的反应,实验如下:
下列说法正确的是
| ① | ② |
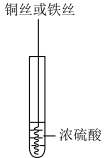 | 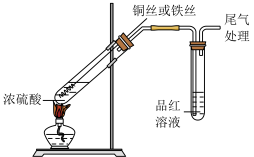 |
| 铜丝表面无明显现象 铁丝表面迅速变黑,之后无明显现象 | 铜丝或铁丝逐渐溶解,产生大量气体, 品红溶液褪色 |
| A.常温下不能用铁制容器盛放浓硫酸,可用铜制容器盛放浓硫酸 |
| B.②中铜丝或铁丝均有剩余时,产生气体的物质的量相等 |
| C.依据②,可推断出铜和铁与浓硫酸反应可生成SO2 |
| D.①②中现象的差异仅是由于温度改变了化学反应速率 |
您最近一年使用:0次
2019-05-28更新
|
2425次组卷
|
18卷引用:山西省实验中学2021届高三9月月考化学试题
山西省实验中学2021届高三9月月考化学试题山西省实验中学2020-2021学年高三上学期第一次月考化学试题【区级联考】北京市通州区2019届高三下学期第三次模拟考试理科综合化学试题(已下线)第4章 非金属及其化合物 单元测试(测)——2020年高考化学一轮复习讲练测(已下线)小题必刷15 铁、铜及其化合物——2021年高考化学一轮复习小题必刷(通用版)(已下线)小题必刷19 硫及其化合物——2021年高考化学一轮复习小题必刷(通用版)(已下线)易错19 实验装置类选择题-备战2021年高考化学一轮复习易错题(人教版2019)必修第二册 第五章 化工生产中的重要非金属元素 第一节 硫及其化合物四川省成都龙泉二中2021届高三下学期3月月考理综化学试题(已下线)第10讲 金属材料及金属矿物的开发利用(精练)-2022年高考化学一轮复习讲练测(已下线)考点11 硫及其化合物-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点11 硫及其化合物-备战2022年高考化学一轮复习考点帮(浙江专用)(已下线)考点10 硫及其化合物-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)专题七实验装置图(讲)北京市朝阳区2023届高三下学期三模化学试题(已下线)第5讲 金属材料与金属的冶炼(已下线)考点10 硫及其化合物(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)山东省青岛第五十八中学2023-2024学年高一上学期1月月考化学试题
名校
7 . 向乙醛溶液中加入含 的物质的量为1
的物质的量为1 的溴水,观察到溴水褪色。对产生该现象的原因有如下3种猜想:①溴水与乙醛发生取代反应;②由于乙醛具有还原性,溴水将乙醛氧化为乙酸;③由于乙醛分子中有不饱和键,溴水与乙醛发生加成反应。
的溴水,观察到溴水褪色。对产生该现象的原因有如下3种猜想:①溴水与乙醛发生取代反应;②由于乙醛具有还原性,溴水将乙醛氧化为乙酸;③由于乙醛分子中有不饱和键,溴水与乙醛发生加成反应。
为探究哪一种猜想正确,某研究性学习小组设计了如下2种实验方案。
方案1:检验褪色后溶液的酸碱性。方案2:测定反应后溶液中的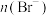 。
。
下列说法正确的是
 的物质的量为1
的物质的量为1 的溴水,观察到溴水褪色。对产生该现象的原因有如下3种猜想:①溴水与乙醛发生取代反应;②由于乙醛具有还原性,溴水将乙醛氧化为乙酸;③由于乙醛分子中有不饱和键,溴水与乙醛发生加成反应。
的溴水,观察到溴水褪色。对产生该现象的原因有如下3种猜想:①溴水与乙醛发生取代反应;②由于乙醛具有还原性,溴水将乙醛氧化为乙酸;③由于乙醛分子中有不饱和键,溴水与乙醛发生加成反应。为探究哪一种猜想正确,某研究性学习小组设计了如下2种实验方案。
方案1:检验褪色后溶液的酸碱性。方案2:测定反应后溶液中的
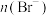 。
。下列说法正确的是
| A.若检验褪色后的溶液显酸性,说明溴水将乙醛氧化成乙酸 |
B.若测得反应后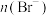 为0 为0 ,说明溴水与乙醛发生加成反应 ,说明溴水与乙醛发生加成反应 |
C.若测得反应后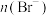 为2 为2 ,说明溴水与乙醛发生取代反应 ,说明溴水与乙醛发生取代反应 |
D.若溴水能将乙醛氧化为乙酸,反应的离子方程式为: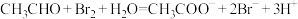 |
您最近一年使用:0次
2023-07-18更新
|
339次组卷
|
4卷引用:山西省名校联合测评2022-2023学年高二下学期7月期末化学试题
名校
8 . 亚硫酰氯( )又名氯化亚砜,是一种无色或淡黄色发烟液体,有强烈刺激性气味,其熔点-105℃,沸点79℃,140℃以上时易分解。遇水剧烈反应,常用作脱水剂,主要用于制造酰基氯化物,还用于医药、农药、染料等的生产。某实验小组设计实验制备氯化亚砜并探究其性质。
)又名氯化亚砜,是一种无色或淡黄色发烟液体,有强烈刺激性气味,其熔点-105℃,沸点79℃,140℃以上时易分解。遇水剧烈反应,常用作脱水剂,主要用于制造酰基氯化物,还用于医药、农药、染料等的生产。某实验小组设计实验制备氯化亚砜并探究其性质。
【资料】①实验室制备原理:在活性炭催化下,
②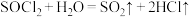 。
。
③ 是一种重要的化工试剂,遇水易分解。
是一种重要的化工试剂,遇水易分解。
实验一:制备产品并探究 的性质
的性质
根据图1所示装置设计实验(装置可以重复使用)。
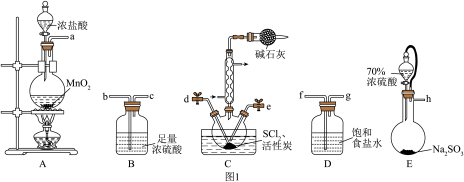
(1)装置接口连接顺序为a→_______ →d、e→_______ →h。
(2)实验室用亚硫酸钠固体与70%硫酸制备 ,不用稀硫酸的原因为
,不用稀硫酸的原因为_______ 。
(3)A装置中发生反应的离子方程式为_______ 。
(4)实验室常用过量NaOH溶液吸收 ,写出反应的离子方程式:
,写出反应的离子方程式:_______ 。
(5)甲同学认为 还可用作由
还可用作由 制取无水
制取无水 的脱水剂,但乙同学认为该实验可能发生副反应使产品不纯。所以乙同学设计如下实验判断副反应的可能性:取少量
的脱水剂,但乙同学认为该实验可能发生副反应使产品不纯。所以乙同学设计如下实验判断副反应的可能性:取少量 于试管中,加入足量
于试管中,加入足量 ,充分反应后向试管中加水溶解,取溶解后的溶液少许于四支试管中,分别进行下列实验,能验证发生副反应的是_______(填选项字母)。
,充分反应后向试管中加水溶解,取溶解后的溶液少许于四支试管中,分别进行下列实验,能验证发生副反应的是_______(填选项字母)。
实验二:测定产品纯度。
利用图2装置测定产品纯度。
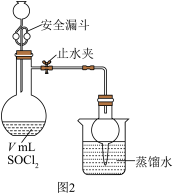
打开止水夹,向安全漏斗中加入足量蒸馏水,待反应完全后,将烧杯中的溶液和烧瓶中的溶液合并,在合并后的溶液中加入足量的 固体,振荡后静置,过滤,将滤液配制成250mL溶液,取25.00mL配制的溶液于锥形瓶,滴几滴
固体,振荡后静置,过滤,将滤液配制成250mL溶液,取25.00mL配制的溶液于锥形瓶,滴几滴 溶液作指示剂,用
溶液作指示剂,用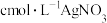 溶液滴定至终点,消耗VmL
溶液滴定至终点,消耗VmL 溶液[已知:常温下,
溶液[已知:常温下, ,
,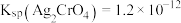 ]。
]。
(6)VmL产品中含_______ mol 。下列情况会使测定结果偏高的是
。下列情况会使测定结果偏高的是_______ (填序号)。
①产品含少量 ②滴定管没有用
②滴定管没有用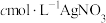 溶液润洗
溶液润洗
③滴加 指示剂过多 ④合并溶液时,烧瓶中有少量残余液体
指示剂过多 ④合并溶液时,烧瓶中有少量残余液体
 )又名氯化亚砜,是一种无色或淡黄色发烟液体,有强烈刺激性气味,其熔点-105℃,沸点79℃,140℃以上时易分解。遇水剧烈反应,常用作脱水剂,主要用于制造酰基氯化物,还用于医药、农药、染料等的生产。某实验小组设计实验制备氯化亚砜并探究其性质。
)又名氯化亚砜,是一种无色或淡黄色发烟液体,有强烈刺激性气味,其熔点-105℃,沸点79℃,140℃以上时易分解。遇水剧烈反应,常用作脱水剂,主要用于制造酰基氯化物,还用于医药、农药、染料等的生产。某实验小组设计实验制备氯化亚砜并探究其性质。【资料】①实验室制备原理:在活性炭催化下,

②
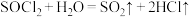 。
。③
 是一种重要的化工试剂,遇水易分解。
是一种重要的化工试剂,遇水易分解。实验一:制备产品并探究
 的性质
的性质根据图1所示装置设计实验(装置可以重复使用)。

(1)装置接口连接顺序为a→
(2)实验室用亚硫酸钠固体与70%硫酸制备
 ,不用稀硫酸的原因为
,不用稀硫酸的原因为(3)A装置中发生反应的离子方程式为
(4)实验室常用过量NaOH溶液吸收
 ,写出反应的离子方程式:
,写出反应的离子方程式:(5)甲同学认为
 还可用作由
还可用作由 制取无水
制取无水 的脱水剂,但乙同学认为该实验可能发生副反应使产品不纯。所以乙同学设计如下实验判断副反应的可能性:取少量
的脱水剂,但乙同学认为该实验可能发生副反应使产品不纯。所以乙同学设计如下实验判断副反应的可能性:取少量 于试管中,加入足量
于试管中,加入足量 ,充分反应后向试管中加水溶解,取溶解后的溶液少许于四支试管中,分别进行下列实验,能验证发生副反应的是_______(填选项字母)。
,充分反应后向试管中加水溶解,取溶解后的溶液少许于四支试管中,分别进行下列实验,能验证发生副反应的是_______(填选项字母)。A.滴加 溶液 溶液 | B.滴加 溶液 溶液 |
C.滴加酸性 溶液 溶液 | D.先滴加稀 ,再滴加 ,再滴加 溶液 溶液 |
实验二:测定产品纯度。
利用图2装置测定产品纯度。

打开止水夹,向安全漏斗中加入足量蒸馏水,待反应完全后,将烧杯中的溶液和烧瓶中的溶液合并,在合并后的溶液中加入足量的
 固体,振荡后静置,过滤,将滤液配制成250mL溶液,取25.00mL配制的溶液于锥形瓶,滴几滴
固体,振荡后静置,过滤,将滤液配制成250mL溶液,取25.00mL配制的溶液于锥形瓶,滴几滴 溶液作指示剂,用
溶液作指示剂,用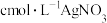 溶液滴定至终点,消耗VmL
溶液滴定至终点,消耗VmL 溶液[已知:常温下,
溶液[已知:常温下, ,
,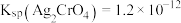 ]。
]。(6)VmL产品中含
 。下列情况会使测定结果偏高的是
。下列情况会使测定结果偏高的是①产品含少量
 ②滴定管没有用
②滴定管没有用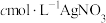 溶液润洗
溶液润洗③滴加
 指示剂过多 ④合并溶液时,烧瓶中有少量残余液体
指示剂过多 ④合并溶液时,烧瓶中有少量残余液体
您最近一年使用:0次
9 . 物质的类别和核心元素的化合价是研究物质性质的两个重要角度。“价类二维图”是研究物质性质的重要手段。下图所示是氮及其部分化合物的“价类二维图”,根据图示回答下列问题。
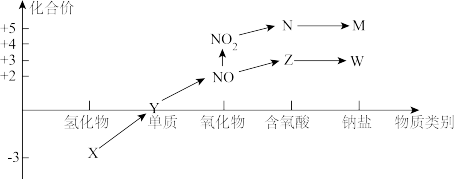
某化学兴趣小组利用如图装置制备X并探究其相关性质。

(1)从物质的性质分析,B中盛放的试剂名称为:_______ 。
(2)将D与a相连,在E中产生白色沉淀,其沉淀的化学式为:_______ ,若向a处分别通入_______ (填标号),在E中也会产生白色沉淀。
A. B.
B. C.
C. D.
D.
(3)实验发现C中粉末完全变红,D中无水硫酘铜变蓝,还产生单质Y。若C中红色固体为单质,实验后将C中固体与稀硝酸混合,充分反应后红色固体有剩余,再加入下列的_______(填标号)试剂,固体又可以继续溶解。
(4)人体正常的血红蛋白含有 ,但若误食W,会导致血红蛋白含有的
,但若误食W,会导致血红蛋白含有的 转化为
转化为 而中毒,服用维生素C可解毒。解毒时维生素C的作用是
而中毒,服用维生素C可解毒。解毒时维生素C的作用是_______ (填“还原性”或“氧化性”)。

某化学兴趣小组利用如图装置制备X并探究其相关性质。

(1)从物质的性质分析,B中盛放的试剂名称为:
(2)将D与a相连,在E中产生白色沉淀,其沉淀的化学式为:
A.
 B.
B. C.
C. D.
D.
(3)实验发现C中粉末完全变红,D中无水硫酘铜变蓝,还产生单质Y。若C中红色固体为单质,实验后将C中固体与稀硝酸混合,充分反应后红色固体有剩余,再加入下列的_______(填标号)试剂,固体又可以继续溶解。
A. 溶液 溶液 | B. 溶液 溶液 | C.稀 | D. 溶液 溶液 |
(4)人体正常的血红蛋白含有
 ,但若误食W,会导致血红蛋白含有的
,但若误食W,会导致血红蛋白含有的 转化为
转化为 而中毒,服用维生素C可解毒。解毒时维生素C的作用是
而中毒,服用维生素C可解毒。解毒时维生素C的作用是
您最近一年使用:0次
名校
10 . 某小组比较Cl-、Br-、I- 的还原性,实验如下:
下列对实验的分析不合理 的是
实验1 | 实验2 | 实验3 | |
| 装置 |
|
|
|
现象 | 溶液颜色无明显变化;把蘸浓氨水的玻璃棒靠近试管口,产生白烟 | 溶液变黄;把湿KI淀粉试纸靠近试管口,变蓝 | 溶液变深紫色;经检验溶液含单质碘 |
| A.实验1中,白烟是NH4Cl | B.根据实验1和实验2判断还原性:Br->Cl- |
| C.根据实验3判断还原性:I->Br- | D.上述实验利用了浓H2SO4的强氧化性、难挥发性等性质 |
您最近一年使用:0次
2018-10-15更新
|
1491次组卷
|
14卷引用:山西省山西大学附属中学2021-2022学年高三上学期10月模块诊断考试化学试题
山西省山西大学附属中学2021-2022学年高三上学期10月模块诊断考试化学试题【全国区级联考】北京市朝阳区2018届高三二模理综化学试题(已下线)【全国区级联考】北京市朝阳区2018届高三第二次综合练习(二模)理综化学试题【全国百强校】湖北省荆州中学2018届高三全真模拟考试(二)理综化学试题【全国百强校】北京市中央民族大学附属中学(朝阳分校)2019届高三上学期10月月考化学试题浙江省杭州市2018-2019学年高二下学前期末考试化学试题浙江省杭州市长征中学2019-2020学年高二上学期期中考试化学试题(已下线)《2020年新高考政策解读与配套资源》模拟试题04-2020年北京新高考化学模拟试题(已下线)小题必刷18 氯及其化合物——2021年高考化学一轮复习小题必刷(通用版)江西省高安中学2020-2021学年高一上学期期中考试化学试题安徽省六安中学2021届高三上学期第三次月考化学试题(已下线)押新高考卷10题 氧化还原反应-备战2022年高考化学临考题号押题(新高考通版)(已下线)第四章 非金属及其化合物 第19练 卤素的性质及提取北京市大兴一中2023-2024学年高一下学期3月月考化学试题