20. 某化学课外小组的同学通过实验探究认识化学反应速率和化学反应限度
(1)实验一:通过实验室制备
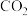
的反应探究外界条件对化学反应速率的影响,下表是实验过程中的数据及相关信息:
| 序号 | 反应温度/℃ | 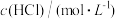 | 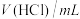 | 10g 的形状 的形状 | t/min |
| ① | 20 | 2 | 10 | 块状 | t1 |
| ② | 20 | 4 | 10 | 块状 | t2 |
| ③ | 20 | 2 | 10 | 粉末 | t3 |
| ④ | 40 | 2 | 10 | 粉末 | t4 |
| ⑤ | 40 | 4 | 10 | 粉末 | t5 |
t表示收集CO
2体积为a mL所需的时间,(注:气体体积均在相同条件下测得),分析表格中的信息可知,影响该化学反应速率的因素有
___。
(2)实验二:已知2KMnO
4+5H
2C
2O
4+3H
2SO
4=K
2SO
4+2MnSO
4+10CO
2↑+8H
2O。在酸性高锰酸钾溶液与草酸(H
2C
2O
4)溶液反应时,发现开始一段时间,反应速率较慢,溶液褪色不明显,但不久突然褪色,反应速率明显加快。
①针对上述实验现象,小组同学认为KMnO
4与H
2C
2O
4反应放热,导致溶液温度升高,反应速率加快。从影响化学反应速率的因素看,你认为还可能是
__________的影响。
②若用实验证明你的猜想,除酸性高锰酸钾溶液、草酸溶液外,还需要的试剂最合理的是
_____(填字母)。
A.硫酸钾
B.硫酸锰
C.二氧化锰
D.水
(3)实验三:探究KI和FeCl
3混合时生成KCl、I
2和FeCl
2的反应存在一定的限度。
Ⅰ、向5 mL 0.1 mol/LKI溶液中滴加5~6滴0.1 molL FeCl
3溶液,充分反应后,将所得溶液分成甲、乙两等份;
Ⅱ、向甲中滴加CCl
4,充分振荡;Ⅲ、向乙中滴加试剂X。
请回答下列问题:
①步骤Ⅲ中,试剂X是
________;
②步骤Ⅱ和Ⅲ中的实验现象说明KI和FeCl
3混合时生成KCl、I
2和FeCl
2的反应存在一定的限度,该实验现象是
__________。