某化学课外小组的同学通过实验探究认识化学反应速率和化学反应限度
(1)实验一:通过实验室制备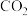 的反应探究外界条件对化学反应速率的影响,下表是实验过程中的数据及相关信息:
的反应探究外界条件对化学反应速率的影响,下表是实验过程中的数据及相关信息:
t表示收集CO2体积为a mL所需的时间,(注:气体体积均在相同条件下测得),分析表格中的信息可知,影响该化学反应速率的因素有___ 。
(2)实验二:已知2KMnO4+5H2C2O4+3H2SO4=K2SO4+2MnSO4+10CO2↑+8H2O。在酸性高锰酸钾溶液与草酸(H2C2O4)溶液反应时,发现开始一段时间,反应速率较慢,溶液褪色不明显,但不久突然褪色,反应速率明显加快。
①针对上述实验现象,小组同学认为KMnO4与H2C2O4反应放热,导致溶液温度升高,反应速率加快。从影响化学反应速率的因素看,你认为还可能是__________ 的影响。
②若用实验证明你的猜想,除酸性高锰酸钾溶液、草酸溶液外,还需要的试剂最合理的是_____ (填字母)。
A.硫酸钾 B.硫酸锰 C.二氧化锰 D.水
(3)实验三:探究KI和FeCl3混合时生成KCl、I2和FeCl2的反应存在一定的限度。
Ⅰ、向5 mL 0.1 mol/LKI溶液中滴加5~6滴0.1 molL FeCl3溶液,充分反应后,将所得溶液分成甲、乙两等份;
Ⅱ、向甲中滴加CCl4,充分振荡;Ⅲ、向乙中滴加试剂X。
请回答下列问题:
①步骤Ⅲ中,试剂X是________ ;
②步骤Ⅱ和Ⅲ中的实验现象说明KI和FeCl3混合时生成KCl、I2和FeCl2的反应存在一定的限度,该实验现象是__________ 。
(1)实验一:通过实验室制备
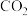 的反应探究外界条件对化学反应速率的影响,下表是实验过程中的数据及相关信息:
的反应探究外界条件对化学反应速率的影响,下表是实验过程中的数据及相关信息:| 序号 | 反应温度/℃ | 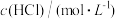 | 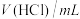 | 10g 的形状 的形状 | t/min |
| ① | 20 | 2 | 10 | 块状 | t1 |
| ② | 20 | 4 | 10 | 块状 | t2 |
| ③ | 20 | 2 | 10 | 粉末 | t3 |
| ④ | 40 | 2 | 10 | 粉末 | t4 |
| ⑤ | 40 | 4 | 10 | 粉末 | t5 |
(2)实验二:已知2KMnO4+5H2C2O4+3H2SO4=K2SO4+2MnSO4+10CO2↑+8H2O。在酸性高锰酸钾溶液与草酸(H2C2O4)溶液反应时,发现开始一段时间,反应速率较慢,溶液褪色不明显,但不久突然褪色,反应速率明显加快。
①针对上述实验现象,小组同学认为KMnO4与H2C2O4反应放热,导致溶液温度升高,反应速率加快。从影响化学反应速率的因素看,你认为还可能是
②若用实验证明你的猜想,除酸性高锰酸钾溶液、草酸溶液外,还需要的试剂最合理的是
A.硫酸钾 B.硫酸锰 C.二氧化锰 D.水
(3)实验三:探究KI和FeCl3混合时生成KCl、I2和FeCl2的反应存在一定的限度。
Ⅰ、向5 mL 0.1 mol/LKI溶液中滴加5~6滴0.1 molL FeCl3溶液,充分反应后,将所得溶液分成甲、乙两等份;
Ⅱ、向甲中滴加CCl4,充分振荡;Ⅲ、向乙中滴加试剂X。
请回答下列问题:
①步骤Ⅲ中,试剂X是
②步骤Ⅱ和Ⅲ中的实验现象说明KI和FeCl3混合时生成KCl、I2和FeCl2的反应存在一定的限度,该实验现象是
更新时间:2020-11-13 18:37:16
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
名校
【推荐1】按要求回答下列问题
(1)某蓄电池的正负极标志难以辨别,请设计实验方案,将蓄电池的正负极辨别出来____________________ 。
(2)解释下列化学反应的反应速率变化关系曲线
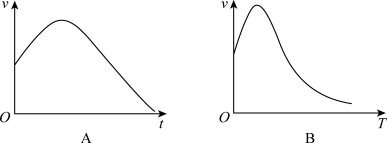
①将除去氧化膜的镁条投入盛有稀盐酸的试管中,产生氢气的速率随时间的变化关系如图A所示,试解释原因:_________________________________________________________ 。
②过氧化氢在酶的催化作用下的分解速率随温度的变化关系如图B所示,试解释原因:______________________ 。
(3)氢能源是最具应用前景的能源之一,高纯氢的制备是目前的研究热点。可利用太阳能光伏电池电解水制高纯氢,工作示意图如下。通过控制开关连接K1或K2,可交替得到H2和O2。

①制H2时,连接_______________ 。
②改变开关连接方式,可得O2,电极反应式为___________________________ 。
③结合①和②中电极3的电极反应式,说明电极3的作用:______________________________ 。
(4)甲醇燃料电池DMFC可作电脑、汽车的能量来源。在实验室完成一个实验,用DMFC电解NaClO3溶液可制取NaClO4溶液,装置如图所示(其中DMFC以KOH作电解质)。

①写出电源负极电极反应式:______________________________ 。
②写出电解的总反应化学方程式:__________________________ 。
(1)某蓄电池的正负极标志难以辨别,请设计实验方案,将蓄电池的正负极辨别出来
(2)解释下列化学反应的反应速率变化关系曲线

①将除去氧化膜的镁条投入盛有稀盐酸的试管中,产生氢气的速率随时间的变化关系如图A所示,试解释原因:
②过氧化氢在酶的催化作用下的分解速率随温度的变化关系如图B所示,试解释原因:
(3)氢能源是最具应用前景的能源之一,高纯氢的制备是目前的研究热点。可利用太阳能光伏电池电解水制高纯氢,工作示意图如下。通过控制开关连接K1或K2,可交替得到H2和O2。

①制H2时,连接
②改变开关连接方式,可得O2,电极反应式为
③结合①和②中电极3的电极反应式,说明电极3的作用:
(4)甲醇燃料电池DMFC可作电脑、汽车的能量来源。在实验室完成一个实验,用DMFC电解NaClO3溶液可制取NaClO4溶液,装置如图所示(其中DMFC以KOH作电解质)。

①写出电源负极电极反应式:
②写出电解的总反应化学方程式:
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】I.(1)25℃、101kPa时,使1.0 g乙烯与足量的氧气反应,生成CO2和液态H2O并放出50 KJ的热量,表示乙烯燃烧热的热化学方程式为_________________________ 。
(2)比较下列热化学方程式中ΔH的大小关系。
CH4 (g)+2O2 (g)===CO2 (g)+2H2O (l) ΔH1
CH4 (g)+2O2 (g)===CO2 (g)+2H2O (g) ΔH2
则ΔH1________ ΔH2
(3)依据盖斯定律可以对某些难以通过实验直接测定的化学反应的焓变进行推算。
已知:C (s,石墨) + O2 (g) = CO2 (g) ΔH1
2H2 (g) + O2 (g ) = 2H2O (l) ΔH2
2C2H2 (g) + 5 O2 (g ) = 4 CO2 (g) +2 H2O (1) ΔH3
则2C (s,石墨)+ H2 (g)= C2H2 (g) 反应的ΔH的表达式为:ΔH =_____ 。
II. 草酸与高锰酸钾在酸性条件下能够发生如下反应:2MnO4- + 5H2C2O4 + 6H+ = 2 Mn2++ 10CO2↑ + 8H2O。现用4 mL 0.001 mol/L KMnO4溶液与2 mL 0.01 mol/L H2C2O4溶液,研究不同条件对化学反应速率的影响。改变的条件如下:
(4)如果研究催化剂对化学反应速率的影响,使用实验_______ 和____ (用I~IV表示,下同);如果研究温度对化学反应速率的影响,使用实验_____ 和______ 。
(5)对比实验I和IV,可以研究_________________ 对化学反应速率的影响,实验IV中加入1 mL蒸馏水的目的是 _______________________ 。
(2)比较下列热化学方程式中ΔH的大小关系。
CH4 (g)+2O2 (g)===CO2 (g)+2H2O (l) ΔH1
CH4 (g)+2O2 (g)===CO2 (g)+2H2O (g) ΔH2
则ΔH1
(3)依据盖斯定律可以对某些难以通过实验直接测定的化学反应的焓变进行推算。
已知:C (s,石墨) + O2 (g) = CO2 (g) ΔH1
2H2 (g) + O2 (g ) = 2H2O (l) ΔH2
2C2H2 (g) + 5 O2 (g ) = 4 CO2 (g) +2 H2O (1) ΔH3
则2C (s,石墨)+ H2 (g)= C2H2 (g) 反应的ΔH的表达式为:ΔH =
II. 草酸与高锰酸钾在酸性条件下能够发生如下反应:2MnO4- + 5H2C2O4 + 6H+ = 2 Mn2++ 10CO2↑ + 8H2O。现用4 mL 0.001 mol/L KMnO4溶液与2 mL 0.01 mol/L H2C2O4溶液,研究不同条件对化学反应速率的影响。改变的条件如下:
| 组别 | 10%硫酸体积/mL | 温度/℃ | 其他物质 |
| I | 2 mL | 20 | / |
| II | 2 mL | 20 | MnSO4固体 |
| III | 2 mL | 30 | / |
| IV | 1 mL | 20 | 1 mL蒸馏水 |
(5)对比实验I和IV,可以研究
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】 溶液和
溶液和 溶液可发生反应:
溶液可发生反应: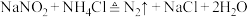 。为探究反应速率与
。为探究反应速率与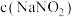 的关系,利用图装置(夹持仪器略去)进行实验。
的关系,利用图装置(夹持仪器略去)进行实验。
实验步骤:往A中加入VmL的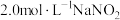 溶液、
溶液、 溶液和水,充分搅拌。控制体系温度,通过分液漏斗往A中加入
溶液和水,充分搅拌。控制体系温度,通过分液漏斗往A中加入 醋酸。当导管口气泡均匀稳定冒出时,开始用排水法收集气体。用秒表测量收集
醋酸。当导管口气泡均匀稳定冒出时,开始用排水法收集气体。用秒表测量收集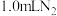 所需的时间,重复多次取平均值(t)。
所需的时间,重复多次取平均值(t)。
回答下列问题:

(1)仪器A的名称为_______ 。
(2)检验装置气密性的方法:关闭止水夹K,_______ 。
(3)若需控制体系的温度为36℃,采取的合理加热方式为_______ 。
(4)每组实验过程中,反应物浓度变化很小,忽路其对反应速率测定的影响。实验数据如表所示。
①
_______ ,
_______ 。
②该反应的速率方程为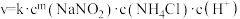 、k为反应速率常数,利用实验数据计算得m=
、k为反应速率常数,利用实验数据计算得m=_______ (填整数)。
③醋酸的作用是_______ 。
 溶液和
溶液和 溶液可发生反应:
溶液可发生反应: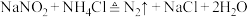 。为探究反应速率与
。为探究反应速率与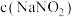 的关系,利用图装置(夹持仪器略去)进行实验。
的关系,利用图装置(夹持仪器略去)进行实验。实验步骤:往A中加入VmL的
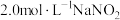 溶液、
溶液、 溶液和水,充分搅拌。控制体系温度,通过分液漏斗往A中加入
溶液和水,充分搅拌。控制体系温度,通过分液漏斗往A中加入 醋酸。当导管口气泡均匀稳定冒出时,开始用排水法收集气体。用秒表测量收集
醋酸。当导管口气泡均匀稳定冒出时,开始用排水法收集气体。用秒表测量收集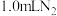 所需的时间,重复多次取平均值(t)。
所需的时间,重复多次取平均值(t)。回答下列问题:

(1)仪器A的名称为
(2)检验装置气密性的方法:关闭止水夹K,
(3)若需控制体系的温度为36℃,采取的合理加热方式为
(4)每组实验过程中,反应物浓度变化很小,忽路其对反应速率测定的影响。实验数据如表所示。
| 实验编号 | V/mL | t/s | |||
 溶液 溶液 |  溶液 溶液 | 醋酸 | 水 | ||
| 1 | 12.0 | 4.0 | 4.0 | 0.0 | 38 |
| 2 | 8.0 |  | 4.0 | 4.0 | 83 |
| 3 |  | 4.0 | 4.0 |  | 150 |
| 4 | 4.0 | 4.0 |  | 8.0 | 334 |


②该反应的速率方程为
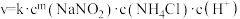 、k为反应速率常数,利用实验数据计算得m=
、k为反应速率常数,利用实验数据计算得m=③醋酸的作用是
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】某化学课外小组的同学通过实验探究认识化学反应速率和化学反应限度。
(1)实验一:探究固体的表面积和温度对反应速率的影响
实验方案:用相同质量的锌和相同浓度的足量的稀盐酸反应得到实验数据如下表所示:
①实验Ⅰ和Ⅱ表明_______ ,化学反应速率越大;
②能表明固体的表面积对反应速率有影响的实验编号是_______ 和_______ ;
③请设计一个实验方案证明盐酸的浓度对该反应速率的影响:_______ 。
(2)实验二:探究 和
和 混合时生成
混合时生成 、
、 和
和 的反应存在一定的限度。实验步骤:
的反应存在一定的限度。实验步骤:
i.向 溶液中滴加5~6滴
溶液中滴加5~6滴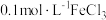 溶液,充分反应后,将所得溶液分成甲、乙、丙三等份;
溶液,充分反应后,将所得溶液分成甲、乙、丙三等份;
ii.向甲中滴加 ,充分振荡;
,充分振荡;
iii.向乙中滴加试剂X。
①将 和
和 反应的离子方程式补充完整:
反应的离子方程式补充完整:_______ 。
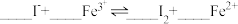
②步骤ⅲ中,试剂X是_______ 。
③步骤ⅱ和ⅲ中的实验现象说明 和
和 混合时生成
混合时生成 、
、 和
和 的反应存在一定的限度,该实验现象是
的反应存在一定的限度,该实验现象是_______ 。
(1)实验一:探究固体的表面积和温度对反应速率的影响
实验方案:用相同质量的锌和相同浓度的足量的稀盐酸反应得到实验数据如下表所示:
| 实验编号 | 锌的状态 | 反应温度/ | 收集 氢气所需时间/s 氢气所需时间/s |
| Ⅰ | 薄片 | 15 | 200 |
| II | 薄片 | 25 | 90 |
| Ⅲ | 粉末 | 25 | 10 |
②能表明固体的表面积对反应速率有影响的实验编号是
③请设计一个实验方案证明盐酸的浓度对该反应速率的影响:
(2)实验二:探究
 和
和 混合时生成
混合时生成 、
、 和
和 的反应存在一定的限度。实验步骤:
的反应存在一定的限度。实验步骤:i.向
 溶液中滴加5~6滴
溶液中滴加5~6滴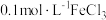 溶液,充分反应后,将所得溶液分成甲、乙、丙三等份;
溶液,充分反应后,将所得溶液分成甲、乙、丙三等份;ii.向甲中滴加
 ,充分振荡;
,充分振荡;iii.向乙中滴加试剂X。
①将
 和
和 反应的离子方程式补充完整:
反应的离子方程式补充完整: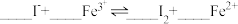
②步骤ⅲ中,试剂X是
③步骤ⅱ和ⅲ中的实验现象说明
 和
和 混合时生成
混合时生成 、
、 和
和 的反应存在一定的限度,该实验现象是
的反应存在一定的限度,该实验现象是
您最近半年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐2】在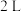 密闭容器中,800℃时反应
密闭容器中,800℃时反应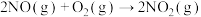 体系中,
体系中,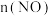 随时间的变化如表:
随时间的变化如表:
(1)上述反应___________ (填“是”或“不是”)可逆反应。
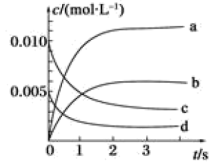
(2)如图所示,表示 变化曲线的是
变化曲线的是______ 。用 表示从
表示从 内该反应的平均速率v=
内该反应的平均速率v=_______ 。
(3)能说明该反应已达到平衡状态的是___________ (填序号)。
a. b.容器内压强保持不变
b.容器内压强保持不变
c.体系颜色不再改变d.容器内密度保持不变
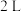 密闭容器中,800℃时反应
密闭容器中,800℃时反应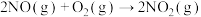 体系中,
体系中,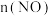 随时间的变化如表:
随时间的变化如表:| 时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
 | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
(1)上述反应
(2)如图所示,表示
 变化曲线的是
变化曲线的是 表示从
表示从 内该反应的平均速率v=
内该反应的平均速率v=
(3)能说明该反应已达到平衡状态的是
a.
 b.容器内压强保持不变
b.容器内压强保持不变c.体系颜色不再改变d.容器内密度保持不变
您最近半年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐3】工业制硫酸中的一步重要反应是SO2的催化氧化。在2L密闭容器中,充入SO2和O2,在催化剂、500℃的条件下发生反应。SO2与SO3的物质的量随时间变化的曲线如图所示,请回答下列问题。

(1)反应开始至2min末,以O2的浓度变化表示该反应的平均反应速率是_______ ;表示SO3的物质的量随时间变化的曲线是_______ (填相应的字母编号)。
(2)由图象可知SO2与O2的反应是可逆反应,证据是_______ 。
(3)下列说法不正确的是_______ 。
a.催化剂可以加快化学反应速率,缩短达到化学平衡所需的时间
b.恒容条件下,通入氮气使压强增大,该反应速率加快
c.通过调控反应条件,可以改变该反应的限度
d.若仅增大容器容积,则该化学反应速率增大
(4)下列情况,能说明该反应一定达到化学平衡状态的是_______ 。
a.单位时间内消耗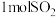 ,同时生成
,同时生成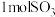
b.SO2的物质的量保持不变
c.混合气体的密度不变
d.SO2的浓度与SO3的浓度相等

(1)反应开始至2min末,以O2的浓度变化表示该反应的平均反应速率是
(2)由图象可知SO2与O2的反应是可逆反应,证据是
(3)下列说法不正确的是
a.催化剂可以加快化学反应速率,缩短达到化学平衡所需的时间
b.恒容条件下,通入氮气使压强增大,该反应速率加快
c.通过调控反应条件,可以改变该反应的限度
d.若仅增大容器容积,则该化学反应速率增大
(4)下列情况,能说明该反应一定达到化学平衡状态的是
a.单位时间内消耗
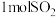 ,同时生成
,同时生成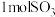
b.SO2的物质的量保持不变
c.混合气体的密度不变
d.SO2的浓度与SO3的浓度相等
您最近半年使用:0次



