21. (1)以CO
2为碳源制取低碳有机物一直是化学领域的研究热点,CO
2加氢制取低碳醇的反应如下:
反应I:CO
2(g)+3H
2(g)=CH
3OH(g)+H
2O(g) △H=-49.0kJ/mol
反应II:2CO
2(g)+6H
2(g)=CH
3CH
2OH(g)+3H
2O(g) △H=-173.6kJ/mol
写出由CH
3OH(g)合成CH
3CH
2OH(g)的反应的热化学方程式
_______________________________(2)高铁酸钾(K
2FeO
4)是铁的一种重要化合物,具有极强的氧化性
①电解法是工业上制备K
2FeO
4的一种方法。以铁为阳极电解氢氧化钠溶液,然后在阳极溶液中加入KOH。电解时阳极发生反应生成FeO
42-,该电极反应式为
______________________________②与MnO
2—Zn电池类似,K
2FeO
4—Zn也可以组成碱性电池,K
2FeO
4在电池中作正极材料,其电极反应式为FeO
42-+3e
-+4H
2O=Fe(OH)
3+5OH
-,则该电池总反应的离子方程式为
__________________(3)可燃冰的主要成分是甲烷,甲烷既是清洁燃料,也是重要的化工原料。甲烷和二氧化碳重整制合成气对温室气体的治理具有重大意义。
已知:CH
4(g)+CO
2(g)==2CO(g)+2H
2(g)
Δ
H=+247.3 kJ·mol
-1CH
4(g)==C(s)+2H
2(g) Δ
H=+75 kJ·mol
-1则反应2CO(g)===C(s)+CO
2(g)在
________(填“高温”或“低温”)下能自发进行。
(4)以甲烷为燃料的新型电池的成本大大低于以氢为燃料的传统燃料电池,下图是目前研究较多的一类固体氧化物燃料电池的工作原理示意图。
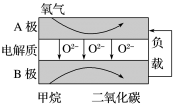
①B极为电池的
________极,该电极的反应式为
____________________________。
②若用该燃料电池作电源,用石墨作电极电解100 mL 1 mol·L
-1的硫酸铜溶液,当两极收集到的气体体积相等时,理论上消耗甲烷的体积为
___________(标况下)。