1 . 某化学兴趣小组利用铜跟浓硫酸反应,探究 的部分性质。
的部分性质。___________ 。
(2)装置B的作用是贮存多余的气体,B中广口瓶内应盛放的液体是___________ (填序号);
①水 ②饱和的 溶液 ③饱和的
溶液 ③饱和的 溶液 ④酸性
溶液 ④酸性 溶液
溶液
(3)装置C和D中产生的现象相同,但原因却不同。C中是由于 与溶液中的
与溶液中的 反应使碱性减弱,而D中则是由于
反应使碱性减弱,而D中则是由于 具有
具有___________ 性。
(4)若实验中用一定质量的铜片和
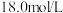 的浓硫酸在加热条件充分反应,最终铜片与硫酸均有剩余。假定反应前后溶液的体积不变,设剩余硫酸的浓度为
的浓硫酸在加热条件充分反应,最终铜片与硫酸均有剩余。假定反应前后溶液的体积不变,设剩余硫酸的浓度为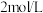 ,现向反应后溶液中缓慢加入硝酸钾固体,充分搅拌直到剩余铜片恰好完全反应,反应消耗硝酸钾
,现向反应后溶液中缓慢加入硝酸钾固体,充分搅拌直到剩余铜片恰好完全反应,反应消耗硝酸钾___________ mol。
 的部分性质。
的部分性质。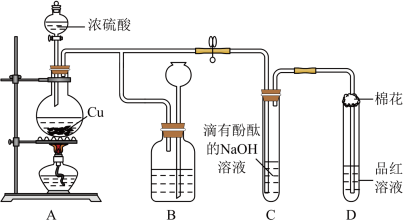
(2)装置B的作用是贮存多余的气体,B中广口瓶内应盛放的液体是
①水 ②饱和的
 溶液 ③饱和的
溶液 ③饱和的 溶液 ④酸性
溶液 ④酸性 溶液
溶液(3)装置C和D中产生的现象相同,但原因却不同。C中是由于
 与溶液中的
与溶液中的 反应使碱性减弱,而D中则是由于
反应使碱性减弱,而D中则是由于 具有
具有(4)若实验中用一定质量的铜片和

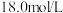 的浓硫酸在加热条件充分反应,最终铜片与硫酸均有剩余。假定反应前后溶液的体积不变,设剩余硫酸的浓度为
的浓硫酸在加热条件充分反应,最终铜片与硫酸均有剩余。假定反应前后溶液的体积不变,设剩余硫酸的浓度为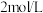 ,现向反应后溶液中缓慢加入硝酸钾固体,充分搅拌直到剩余铜片恰好完全反应,反应消耗硝酸钾
,现向反应后溶液中缓慢加入硝酸钾固体,充分搅拌直到剩余铜片恰好完全反应,反应消耗硝酸钾
您最近一年使用:0次
2 . 某化学自主实验小组利用如图所示装置(K1、K2为止水夹,夹持装置已略去)探究NO2能否被NH3还原。
(1)a仪器名称为_______ 。
(2)甲中盛放的试剂的名称是_______ ,乙中盛放的试剂的化学式为_______ 。
(3)C中铜与浓硝酸反应时,体现的浓硝酸的性质为_______ ,C中实验现象为_______ 。
(4)实验过程中观察到B中红棕色气体逐渐变淡至无色,经检测发现尾气中的有害气体只有未完全反应的反应物,则B中发生反应的化学方程式为_______ ,其中n(还原产物):n(氧化产物)=_______ 。
(5)NaOH溶液可吸收过量的NO2,二者反应生成两种钠盐,则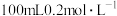 NaOH溶液最多能吸收
NaOH溶液最多能吸收_______ mol NO2.(忽略气体在水中的溶解及气体与水的反应)

(1)a仪器名称为
(2)甲中盛放的试剂的名称是
(3)C中铜与浓硝酸反应时,体现的浓硝酸的性质为
(4)实验过程中观察到B中红棕色气体逐渐变淡至无色,经检测发现尾气中的有害气体只有未完全反应的反应物,则B中发生反应的化学方程式为
(5)NaOH溶液可吸收过量的NO2,二者反应生成两种钠盐,则
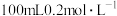 NaOH溶液最多能吸收
NaOH溶液最多能吸收
您最近一年使用:0次
名校
3 . 实验室可用如图装置(略去部分夹持仪器)制取SO2并验证其性质。_______ ,仪器组装完成后,关闭两端活塞,向装置B的长颈漏斗内注入液体至形成段液柱,若_______ 则整个装置气密性良好。
(2)A中如果用浓硫酸和铜反应,也可制得 进行实验,反应的化学方程式为
进行实验,反应的化学方程式为_______ 。
(3)C试管中的试剂可以验证二氧化硫的氧化性,现象为_______ 。
(4)为验证二氧化硫的还原性,充分反应后,取试管D中的溶液分成三份,分别进行实验:
方案Ⅰ:向第一份溶液中加入 溶液,有白色沉淀生成;
溶液,有白色沉淀生成;
方案Ⅱ:向第二份溶液中加入品红溶液,红色褪去;
方案Ⅲ:向第三份溶液中加入 溶液,产生白色沉淀
溶液,产生白色沉淀
上述方案合理的是方案_______ (填“Ⅰ”“Ⅱ”或“Ⅲ”); 通入KMnO4溶液中发生的主要反应的离子方程式为
通入KMnO4溶液中发生的主要反应的离子方程式为_______ 。
(5)装置E的作用是做安全瓶,防止F中的液体倒吸入D中,装置F中为_______ 溶液。

(2)A中如果用浓硫酸和铜反应,也可制得
 进行实验,反应的化学方程式为
进行实验,反应的化学方程式为(3)C试管中的试剂可以验证二氧化硫的氧化性,现象为
(4)为验证二氧化硫的还原性,充分反应后,取试管D中的溶液分成三份,分别进行实验:
方案Ⅰ:向第一份溶液中加入
 溶液,有白色沉淀生成;
溶液,有白色沉淀生成;方案Ⅱ:向第二份溶液中加入品红溶液,红色褪去;
方案Ⅲ:向第三份溶液中加入
 溶液,产生白色沉淀
溶液,产生白色沉淀上述方案合理的是方案
 通入KMnO4溶液中发生的主要反应的离子方程式为
通入KMnO4溶液中发生的主要反应的离子方程式为(5)装置E的作用是做安全瓶,防止F中的液体倒吸入D中,装置F中为
您最近一年使用:0次
4 . 如图所示,夹子开始处于关闭状态,将液体A滴入试管②与气体B充分反应,打开夹子,可发现试管①内的水立刻沸腾了.则液体A和气体B的组合不可能是

| A.水、氨气 | B.水、 与 与 | C. 溶液、 溶液、 | D. 溶液、 溶液、 |
您最近一年使用:0次
名校
解题方法
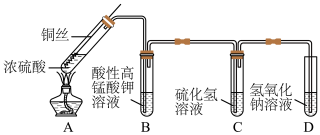
5 . 某化学实验小组的同学利用铜与浓硫酸反应制取二氧化硫并研究其性质,所用实验装置如图。回答下列问题:________________ 。
(2)装置A中反应的化学方程式是__________________ 。
(3)装置B的现象为__________ ,体现了SO2的__________ 性。
(4)装置C中反应的化学方程式是____________________________ 。
(5)探究SO2与钡盐的反应
在下图装置中先后三次加入相同浓度、相同体积、不同条件下的钡盐溶液,控制食用油油层厚度一致,打开开关K,通入SO2流速一致。三次实验现象如下表:
三次实验分别得到如下pH-t图:_____________________________ 。
②pH-t图中,曲线a呈缓慢下降趋势,这是因为__________ ;曲线b出现骤降,这是因为SO2与BaCl2溶液中溶解的__________ 发生反应生成了H+。
③写出实验c中反应的离子方程式:_____________________
______Ba2++_______SO2+______ +_____=______BaSO4↓+_______NO+_______。
+_____=______BaSO4↓+_______NO+_______。
(2)装置A中反应的化学方程式是
(3)装置B的现象为
(4)装置C中反应的化学方程式是
(5)探究SO2与钡盐的反应
在下图装置中先后三次加入相同浓度、相同体积、不同条件下的钡盐溶液,控制食用油油层厚度一致,打开开关K,通入SO2流速一致。三次实验现象如下表:
实验a | 实验b | 实验c |
|
已煮沸的 BaCl2溶液 | 未煮沸的 BaCl2溶液 | 已煮沸的 Ba(NO3)2溶液 | |
无白色沉淀生成 | 有白色沉淀生成 | 有白色沉淀生成 |

②pH-t图中,曲线a呈缓慢下降趋势,这是因为
③写出实验c中反应的离子方程式:
______Ba2++_______SO2+______
 +_____=______BaSO4↓+_______NO+_______。
+_____=______BaSO4↓+_______NO+_______。
您最近一年使用:0次
6 . 甲、乙两同学欲验证乙醇的性质,现做如下实验:
Ⅰ.甲同学做乙醇的催化氧化实验并考查催化剂的催化机理,现设计了如下图所示的装置(夹持装置仪器已省略):
(1)M处乙醇参与反应的化学方程式为_______ 。
(2)从M管中可观察到红、黑交替现象。从中可认识到该实验过程中催化剂_______ (填“参加”或“不参加”)化学反应,还可以认识到催化剂起催化作用需要一定的_______ 。
(3)用银氨溶液可以检验F中的产物,写出配置银氨溶液的过程:_______ (必须用到的试剂:2%的 溶液,2%的稀氨水)
溶液,2%的稀氨水)
Ⅱ.乙同学采用如图装置以乙醇为原料制备乙烯并研究乙烯与溴水的反应。_______ 。
(5)除杂试剂A为_______ 。
(6)实验观察到溴水褪色,得到无色透明的溶液。进一步分析发现反应产物主要为 ,含少量
,含少量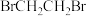 。乙烯与溴水反应后的溶液呈
。乙烯与溴水反应后的溶液呈_______ (填“中性”、“碱性”或“酸性”)。
Ⅰ.甲同学做乙醇的催化氧化实验并考查催化剂的催化机理,现设计了如下图所示的装置(夹持装置仪器已省略):

(1)M处乙醇参与反应的化学方程式为
(2)从M管中可观察到红、黑交替现象。从中可认识到该实验过程中催化剂
(3)用银氨溶液可以检验F中的产物,写出配置银氨溶液的过程:
 溶液,2%的稀氨水)
溶液,2%的稀氨水) Ⅱ.乙同学采用如图装置以乙醇为原料制备乙烯并研究乙烯与溴水的反应。

(5)除杂试剂A为
(6)实验观察到溴水褪色,得到无色透明的溶液。进一步分析发现反应产物主要为
 ,含少量
,含少量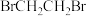 。乙烯与溴水反应后的溶液呈
。乙烯与溴水反应后的溶液呈
您最近一年使用:0次
名校
7 . 用如图所示的装置进行实验,将稀硫酸全部加入装置 I的试管中,关闭活塞。 下列说法错误的是
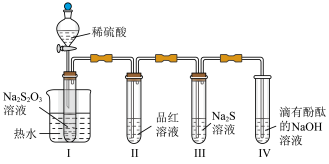
| A.Ⅳ的作用是吸收尾气 SO2,防止污染空气 |
| B.降低稀硫酸浓度,装置 I中试管内出现浑浊所需的时间会变长 |
| C.装置 Ⅱ中品红溶液褪色,与氯水使品红溶液褪色原理相同 |
| D.装置 Ⅲ试管中出现浑浊,说明 SO2 具有氧化性 |
您最近一年使用:0次
名校
8 . 微型实验因其试剂用量少、产生的污染物少(或废弃物少)在实验室被广泛采用。如图是研究二氧化硫性质的微型实验装置。下列说法中错误的是
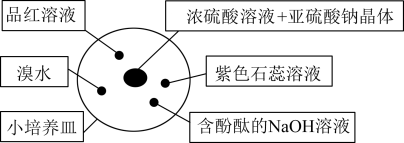
| A.紫色石蕊溶液先变红色后褪色 | B.品红溶液褪色,加热可以恢复 |
C.溴水的黄色褪去,体现 的还原性 的还原性 | D.含酚酞的NaOH溶液红色变浅或褪色 |
您最近一年使用:0次
7日内更新
|
50次组卷
|
2卷引用:河南省开封市五县联考2023-2024学年高一下学期4月期中考试化学试题
9 . 根据下列实验操作和现象所得出的结论或解释正确的是
| 选项 | 实验操作和现象 | 结论或解释 |
| A | 检验SO2气体中是否混有SO3(g):将气体通入Ba(NO3)2溶液,有白色沉淀生成 | 混有SO3(g) |
| B | 淀粉﹣KI溶液中通入少量Cl2,再通入SO2,溶液先出现蓝色,后蓝色褪去 | 还原性:SO2>I﹣>Cl﹣ |
| C | 用蘸有浓氨水的玻璃棒靠近某有色气体X,出现白烟 | 该气体只能是HCl |
| D | 用大理石和盐酸反应制取CO2气体,将气体立即通入一定浓度的Na2SiO3溶液中,出现白色沉淀 | H2CO3的酸性比H2SiO3的酸性强 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
10 . 如图所示,某同学利用 和70%的
和70%的 溶液制取
溶液制取 并探究其性质。
并探究其性质。___________ ;装置B中发生反应的现象为___________ 。
(2)装置C中的实验现象是___________ ,该实验现象说明 具有
具有___________ (填“氧化”或“还原”)性。
(3)装置D的实验现象是___________ 。
(4)装置E的目的是探究 与品红作用的可逆性,请写出实验操作及现象:
与品红作用的可逆性,请写出实验操作及现象:___________ 。
 和70%的
和70%的 溶液制取
溶液制取 并探究其性质。
并探究其性质。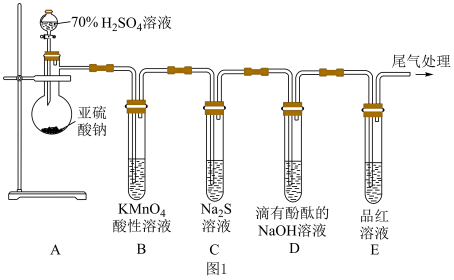
(2)装置C中的实验现象是
 具有
具有(3)装置D的实验现象是
(4)装置E的目的是探究
 与品红作用的可逆性,请写出实验操作及现象:
与品红作用的可逆性,请写出实验操作及现象:
您最近一年使用:0次
2024-06-07更新
|
110次组卷
|
2卷引用:湖南省长沙市实验中学2023-2024学年高一下学期期中考试化学试题




