解题方法
1 . Ⅰ.实验小组利用传感器探究Na2CO3和NaHCO3的性质。
【查阅资料】pH越小,OH-浓度越小,溶液碱性越弱。
【实验过程】
【分析与解释】
(1)实验①中,溶解时吸收热量的物质是___________ 。
(2)实验②中,Na2CO3溶液和澄清石灰水反应的离子方程式为___________ ,OH-未参与该反应的实验证据是___________ 。
(3)实验②中,滴加NaHCO3溶液的pH变化与滴加Na2CO3溶液的有明显差异,原因是滴加NaHCO3溶液的烧杯中,参与反应的离子有___________ 。
(4)工业上制得的纯碱中常含有一定量的NaHCO3,取质量为a g的纯碱样品,充分加热后,质量减少b g,此样品中Na2CO3的质量分数___________ 。
Ⅱ.可用Cl2和Ca(OH)2制备漂粉精,漂粉精常用于游泳池的消毒,起消毒作用的是HClO,池水的酸碱性对漂粉精的消毒效果影响明显。
(5)写出制备漂粉精的化学方程式___________ 。
(6)若池水碱性过强,消毒作用会___________ (填“增强”或“减弱”)。
(7)若池水酸性过强,会刺激眼睛和皮肤。有时加入Na2CO3、NaHCO3以降低酸性,起到降低酸性作用的离子分别是___________ (填离子符号)。
【查阅资料】pH越小,OH-浓度越小,溶液碱性越弱。
【实验过程】
| 编号 | 实验操作 | 实验数据 |
| 实验① | 测量下述实验过程的温度变化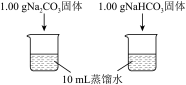 |  |
| 实验② | 测量下述实验过程的pH变化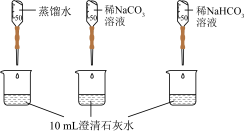 | 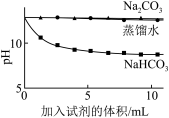 |
(1)实验①中,溶解时吸收热量的物质是
(2)实验②中,Na2CO3溶液和澄清石灰水反应的离子方程式为
(3)实验②中,滴加NaHCO3溶液的pH变化与滴加Na2CO3溶液的有明显差异,原因是滴加NaHCO3溶液的烧杯中,参与反应的离子有
(4)工业上制得的纯碱中常含有一定量的NaHCO3,取质量为a g的纯碱样品,充分加热后,质量减少b g,此样品中Na2CO3的质量分数
Ⅱ.可用Cl2和Ca(OH)2制备漂粉精,漂粉精常用于游泳池的消毒,起消毒作用的是HClO,池水的酸碱性对漂粉精的消毒效果影响明显。
(5)写出制备漂粉精的化学方程式
(6)若池水碱性过强,消毒作用会
(7)若池水酸性过强,会刺激眼睛和皮肤。有时加入Na2CO3、NaHCO3以降低酸性,起到降低酸性作用的离子分别是
您最近一年使用:0次
名校
解题方法
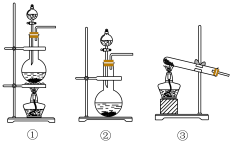
2 . 为了探究Cl2、SO2同时通入水中所发生的反应,某校化学兴趣小组同学设计了如图所示的实验装置。
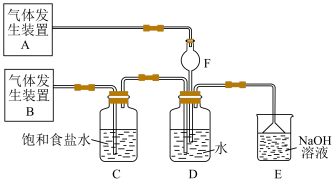
(1)该化学兴趣小组的同学采用Na2SO3与质量分数为70%的硫酸为原料制取SO2,采用MnO2与浓盐酸为原料制取Cl2。在此实验中,仪器 的作用是
的作用是______ ;气体发生装置B应选择下列装置中的____________ (填序号)。
(2)为验证通入D装置中的气体是Cl2过量还是SO2过量,该化学兴趣小组的同学准备了以下试剂:
①氯化铁溶液 ②氯化亚铁溶液 ③硫氰化钾溶液 ④酸性高锰酸钾溶液
若Cl2过量,取适量D中溶液滴加至盛有______ (填序号)的试管中,再加入______ (填序号),产生的现象是______ 。
若SO2过量,取适量D中溶液滴加至盛有______ (填序号)的试管中,产生的现象是______ 。

(1)该化学兴趣小组的同学采用Na2SO3与质量分数为70%的硫酸为原料制取SO2,采用MnO2与浓盐酸为原料制取Cl2。在此实验中,仪器
 的作用是
的作用是
(2)为验证通入D装置中的气体是Cl2过量还是SO2过量,该化学兴趣小组的同学准备了以下试剂:
①氯化铁溶液 ②氯化亚铁溶液 ③硫氰化钾溶液 ④酸性高锰酸钾溶液
若Cl2过量,取适量D中溶液滴加至盛有
若SO2过量,取适量D中溶液滴加至盛有
您最近一年使用:0次
2020-03-04更新
|
638次组卷
|
4卷引用:山东省济南外国语学校2022-2023学年高一上学期期末考试化学试题
名校
解题方法
3 . 为探究H2O2、SO2、Br2的性质,某小组同学设计如下实验(夹持及尾气处理装置已略去,气密性已检验)。

(1)在滴入浓硫酸之前要通入N2一段时间的目的是__________________________ 。
(2)该实验可以证明SO2具有_________ 性;H2O2的氧化性_________ Br2(填“强于”“弱于”)。
(3)B中红棕色褪去的原因_______________________________ ,B中重新变成红棕色的原因____________________________________ (均用离子方程式表示)。
(4)C中产生的白色沉淀是______ 。
(5)甲同学通过C中产生白色沉淀,得出结论:SO2能与BaCl2反应产生沉淀。乙同学认为不能得出此结论,并对实验进行了改进:在B和C之间增加盛放_________ 的洗气瓶。再次进行实验时,则C中未产生沉淀。
(6)为进一步研究SO2的性质,分别用煮沸和未煮沸过的蒸馏水配制Ba(NO3)2和BaCl2溶液,进行如下实验:
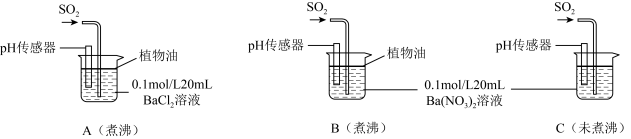
①实验A中,没有观察到白色沉淀,但pH传感器显示溶液呈酸性,原因是__________________ 。(用化学方程式表示)
②实验C中出现白色沉淀比实验B快很多。由此得出的结论是__________________ 。若实验B、C中通入足量的SO2后,溶液酸性:B_________ C(填“强于”“弱于”“等于”)。
(7)Na2SO3固体因贮放不慎发生变质。现取样品1.8克溶于水得溶液A,在A中加入足量BaCl2溶液,过滤得沉淀B,将沉淀B加入足量的稀硫酸后,沉淀不仅不消失,反而增加了0.16g(假如沉淀完全转化)。样品中Na2SO3的质量分数是___________________ 。

| 实验操作 | 实验现象 |
| i.打开弹簧夹,通入N2一段时间,关闭弹簧夹,打开A中分液漏斗活塞,滴加浓硫酸 | A中有气泡产生,B中红棕色溴水褪色,C中有白色沉淀 |
| ⅱ.取C中沉淀加入盐酸 | C中白色沉淀不溶解 |
| ⅲ.打开B中分液漏斗活塞,逐滴滴加H2O2 | 开始时颜色无明显变化;继续滴加H2O2溶液,一段时间后,混合液逐渐变成红棕色 |
(2)该实验可以证明SO2具有
(3)B中红棕色褪去的原因
(4)C中产生的白色沉淀是
(5)甲同学通过C中产生白色沉淀,得出结论:SO2能与BaCl2反应产生沉淀。乙同学认为不能得出此结论,并对实验进行了改进:在B和C之间增加盛放
(6)为进一步研究SO2的性质,分别用煮沸和未煮沸过的蒸馏水配制Ba(NO3)2和BaCl2溶液,进行如下实验:

①实验A中,没有观察到白色沉淀,但pH传感器显示溶液呈酸性,原因是
②实验C中出现白色沉淀比实验B快很多。由此得出的结论是
(7)Na2SO3固体因贮放不慎发生变质。现取样品1.8克溶于水得溶液A,在A中加入足量BaCl2溶液,过滤得沉淀B,将沉淀B加入足量的稀硫酸后,沉淀不仅不消失,反而增加了0.16g(假如沉淀完全转化)。样品中Na2SO3的质量分数是
您最近一年使用:0次
2020-01-18更新
|
646次组卷
|
3卷引用:广东省汕头市金山中学2019-2020学年高一上学期期末考试化学试题
4 . 山东省率先实现空气质量自动监测四级数据覆盖与共享。某科研小组测定空气中SO2含量的过程如下:
已知:品红能溶于乙醇等溶剂。
回答下列问题:
(1)向品红水溶液中通入足量SO2,现象是___ 。经查阅资料知,不是SO2导致上述现象,验证该结论可使用的试剂是___ 。
(2)用如图所示装置检测空气中SO2的含量。
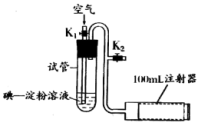
①配制1000mL5×10-3mol•L-1的碘溶液,需要的玻璃仪器有烧杯、玻璃棒、胶头滴管、量筒、__ 。
②将配制的溶液稀释10倍,量取5mL注入试管,加入2-3滴淀粉溶液,慢慢抽气,观察到溶液中___ (填实验现象)时,停止抽气,记录抽气次数n。该过程中发生反应的离子方程式为__ 。
③空气中二氧化硫的最大允许含量为0.02mg•L-1。若每次抽空气100mL(标准状况),则n至少为__ 次,才符合标准。抽气时应慢慢抽拉活塞,若抽拉过快,会造成测定结果__ (偏大、偏小、无影响)。
已知:品红能溶于乙醇等溶剂。
回答下列问题:
(1)向品红水溶液中通入足量SO2,现象是
(2)用如图所示装置检测空气中SO2的含量。

①配制1000mL5×10-3mol•L-1的碘溶液,需要的玻璃仪器有烧杯、玻璃棒、胶头滴管、量筒、
②将配制的溶液稀释10倍,量取5mL注入试管,加入2-3滴淀粉溶液,慢慢抽气,观察到溶液中
③空气中二氧化硫的最大允许含量为0.02mg•L-1。若每次抽空气100mL(标准状况),则n至少为
您最近一年使用:0次
2021-01-28更新
|
368次组卷
|
2卷引用:山东省潍坊市2020-2021学年高一上学期期末统考化学试题
5 . 某学习小组探究浓、稀硝酸氧化性的相对强弱,按下图装置进行实验(夹持仪器已略去)。实验表明浓硝酸能将NO氧化成NO2,而稀硝酸不能氧化NO。由此得出的结论是浓硝酸的氧化性强于稀硝酸。
可选药品:浓硝酸、3mo/L稀硝酸、蒸馏水、浓硫酸、氢氧化钠溶液及二氧化碳
已知:氢氧化钠溶液不与NO反应,能与NO2反应,2NO2+2NaOH=NaNO3+NaNO2+H2O。
(1)实验应避免有害气体排放到空气中,装置③、④、⑥中盛放的药品依次是________
(2)滴加浓硝酸之前的操作时检验装置的气密性,加入药品,打开弹簧夹后________
(3)装置①中发生反应的化学方程式是_________
(4)装置②的作用是________ ,发生反应的化学方程式是__________
(5)该小组得出的结论依据的实验现象是___________
(6)实验结束后,同学们发现装置①中溶液呈绿色,而不显蓝色。甲同学认为是该溶液中硝酸铜的质量分数较高所致,而乙同学认为是该溶液中溶解了生成的气体。同学们分别设计了以下4个实验来判断两种看法是否正确。这些方案中可行的是(选填序号字母)( )
a.加热该绿色溶液,观察颜色变化
b.加水稀释绿色溶液,观察颜色变化
c.向该绿色溶液中通入氮气,观察颜色变化
d.向饱和硝酸铜溶液中通入浓硝酸与铜反应产生的气体,观察颜色变化

可选药品:浓硝酸、3mo/L稀硝酸、蒸馏水、浓硫酸、氢氧化钠溶液及二氧化碳
已知:氢氧化钠溶液不与NO反应,能与NO2反应,2NO2+2NaOH=NaNO3+NaNO2+H2O。
(1)实验应避免有害气体排放到空气中,装置③、④、⑥中盛放的药品依次是
(2)滴加浓硝酸之前的操作时检验装置的气密性,加入药品,打开弹簧夹后
(3)装置①中发生反应的化学方程式是
(4)装置②的作用是
(5)该小组得出的结论依据的实验现象是
(6)实验结束后,同学们发现装置①中溶液呈绿色,而不显蓝色。甲同学认为是该溶液中硝酸铜的质量分数较高所致,而乙同学认为是该溶液中溶解了生成的气体。同学们分别设计了以下4个实验来判断两种看法是否正确。这些方案中可行的是(选填序号字母)
a.加热该绿色溶液,观察颜色变化
b.加水稀释绿色溶液,观察颜色变化
c.向该绿色溶液中通入氮气,观察颜色变化
d.向饱和硝酸铜溶液中通入浓硝酸与铜反应产生的气体,观察颜色变化
您最近一年使用:0次
2019-01-30更新
|
3163次组卷
|
21卷引用:浙江省杭州学军中学2023-2024学年高一上学期期末模拟考试化学试卷
浙江省杭州学军中学2023-2024学年高一上学期期末模拟考试化学试卷 2009年普通高等学校招生统一考试理综试题化学部分(北京卷)09高考真题汇编—实验设计与评价 综合性实验2009年高考真题汇编-氮族元素(已下线)2010年天津市天津一中高三第五次月考(理综)化学部分(已下线)2010—2011学年浙江省杭州学军中学高一下学期期中考试化学试卷2016届贵州省务川民族中学高三上学期期中考试化学试卷2015-2016学年江苏省盐城市建湖二中高一下学期期中考试化学试卷2017届河北省邯郸市大名一中高三上学期第一次月考化学试卷宁夏青铜峡市高级中学2018届高三上学期期中考试化学试题内蒙古集宁一中2017-2018学年高一下学期第二次月考理科综合化学试题人教版化学必修一.4.4氨 硝酸 硫酸同步测试卷(已下线)【走进新高考】(人教版必修一)4.4.2氨、硝酸、硫酸——硝酸 同步练习02【全国百强校】北京四中2018-2019学年高一下学期期中测试化学试题江西省宜春市奉新县第一中学2019-2020学年高一下学期第二次月考化学试题福建省福州市2020届高三模拟考试化学试题专题7 第二单元 第2课时 硝酸-高中化学必修第二册苏教版2019人教版2019必修第二册 第五章 第二节 第3课时 硝酸 酸雨及防治第四章 非金属及其化合物 第23讲 硝酸 含氮化合物的转化关系北京市顺义牛栏山第一中学2022-2023学年高一下学期3月月考化学试题(已下线)专题03 硫酸和硝酸专讲(专题过关)-2022-2023学年高一化学下学期期中期末考点大串讲(人教版2019必修第二册)
6 . 小明很喜欢化学实验课,今天要学习“探究铁及其化合物的氧化性或还原性”。
(1)实验前小明预测Fe2+既有还原性又有氧化性。你认为他预测的依据是_______________ 。
(2)小明欲用实验证明他的预测。实验室提供了下列试剂:3%的过氧化氢溶液、锌粒、铜片、0.1 mol·L-1氯化亚铁溶液、硫氰化钾溶液、新制氯水。
①若小明计划在0.1 mol·L-1氯化亚铁溶液滴入新制氯水,探究Fe2+的还原性,你预计可能发生的反应的离子方程式是______________________________ ,可能观察到的现象是溶液由浅绿色变为________ 色。
②实验中,小明发现现象不太明显,老师分析可能是产物的含量太低,建议可以通过检验Fe2+被氧化的产物Fe3+的存在以获取证据。你认为可选_________ 滴入小明所得的混合液中,并通过溶液出现______ 色的现象,证明小明的观点和实验方案都是正确的。
③对于证明Fe2+具有氧化性,小明认为金属单质都具有还原性,并分别将铜片、锌粒投入氯化亚铁溶液中,结果铜片没变化,锌粒逐渐变小。由此说明三种金属的还原性由强至弱的顺序为__________ (填化学式)。
④实际上Fe2+的还原性较强,实验室的氯化亚铁溶液常因氧化而变质,除去杂质的方法是______ ,相关反应的离子方程式是_____________ 。
(1)实验前小明预测Fe2+既有还原性又有氧化性。你认为他预测的依据是
(2)小明欲用实验证明他的预测。实验室提供了下列试剂:3%的过氧化氢溶液、锌粒、铜片、0.1 mol·L-1氯化亚铁溶液、硫氰化钾溶液、新制氯水。
①若小明计划在0.1 mol·L-1氯化亚铁溶液滴入新制氯水,探究Fe2+的还原性,你预计可能发生的反应的离子方程式是
②实验中,小明发现现象不太明显,老师分析可能是产物的含量太低,建议可以通过检验Fe2+被氧化的产物Fe3+的存在以获取证据。你认为可选
③对于证明Fe2+具有氧化性,小明认为金属单质都具有还原性,并分别将铜片、锌粒投入氯化亚铁溶液中,结果铜片没变化,锌粒逐渐变小。由此说明三种金属的还原性由强至弱的顺序为
④实际上Fe2+的还原性较强,实验室的氯化亚铁溶液常因氧化而变质,除去杂质的方法是
您最近一年使用:0次
2018-05-06更新
|
432次组卷
|
7卷引用:陕西省铜川市耀州中学2022-2023学年高一上学期期末考试化学试题
陕西省铜川市耀州中学2022-2023学年高一上学期期末考试化学试题贵州省遵义航天高级中学2017-2018学年高一下学期期中考试理科综合化学试题云南省彝良县民中2018-2019学年高一上学期12月份考试化学试题(已下线)专题10 性质探究类综合实验-2022年高考化学毕业班二轮热点题型归纳与变式演练(全国通用)陕西省渭南市华州区咸林中学2021-2022学年高一上学期第三阶段质量检测化学试题作业(十八) 铁盐和亚铁盐河南省南阳市六校2023-2024学年高一上学期12月月考化学试题



