1 . 铜丝与稀硝酸反应的实验现象叙述错误的是
| A.铜丝逐渐变细 | B.铜丝表面有无色气体产生 |
| C.溶液变蓝 | D.产生的气体遇到空气无明显变化 |
您最近一年使用:0次
2023-06-26更新
|
286次组卷
|
5卷引用:黑龙江省哈尔滨市第三中学2022-2023学年高一下学期学业水平强化模拟考试化学试题
黑龙江省哈尔滨市第三中学2022-2023学年高一下学期学业水平强化模拟考试化学试题黑龙江省哈尔滨市第三中学校2022-2023学年高一下学期6月考试化学试题(已下线)专题十三 氮及其化合物(已下线)合格考真题汇编12氮元素及其化合物(已下线)合格考真题汇编21化学实验基础一
2 . 某实验小组探究 和
和 的反应。实验操作及现象如下。
的反应。实验操作及现象如下。
(1)取实验2后的溶液,进行如下实验:
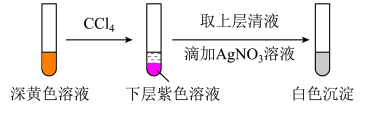
①根据______ 现象,判断实验2中有I2生成,因此反应后溶液显黄色。
②经检验,上述白色沉淀是AgCl。补全实验2中发生反应的离子方程式:_____ 。
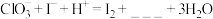
(2)查阅资料:一定条件下, 和I2都可以被氧化成
和I2都可以被氧化成 。
。
作出假设:NaClO3溶液用量增加导致溶液褪色的原因是______ 。
进行实验:
取少量实验4中的无色溶液进行以下实验,证实假设成立。
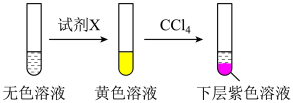
其中试剂X可以是______ (填字母)。
a.碘水 b.KMnO4溶液 c.NaHSO3溶液
 和
和 的反应。实验操作及现象如下。
的反应。实验操作及现象如下。实验及试剂 | 编号 | 无色NaClO3溶液用量 | 试管中溶液颜色 |
| 1 | 0.05mL | 浅黄色 |
2 | 0.02mL | 深黄色 | |
3 | 0.25mL | 浅黄色 | |
4 | 0.30mL | 无色 |

①根据
②经检验,上述白色沉淀是AgCl。补全实验2中发生反应的离子方程式:
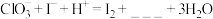
(2)查阅资料:一定条件下,
 和I2都可以被氧化成
和I2都可以被氧化成 。
。作出假设:NaClO3溶液用量增加导致溶液褪色的原因是
进行实验:
取少量实验4中的无色溶液进行以下实验,证实假设成立。

其中试剂X可以是
a.碘水 b.KMnO4溶液 c.NaHSO3溶液
您最近一年使用:0次
3 . 某化学实验小组同学利用以下实验装置制备氨气,并探究氨气的性质(部分仪器已略去)。请回答:

(1)实验室制备氨气的化学方程式为______ 。
(2)用装置B收集氨气时,应选择氨气的进气口是_______ (选填“a”或“b”)。
(3)打开装置B中的止水夹c,若观察到烧瓶内产生了红色喷泉,则说明氨气具有的性质是______ ,请用方程式表示:_______ ;氨气催化氧化可用于制硝酸,请写出氨气催化氧化的化学方程式_______ 。
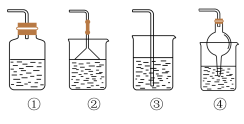
(4)为防止环境污染,以下装置(盛放的液体均为水)可用于吸收多余氨气的是______ (填序号)。

(1)实验室制备氨气的化学方程式为
(2)用装置B收集氨气时,应选择氨气的进气口是
(3)打开装置B中的止水夹c,若观察到烧瓶内产生了红色喷泉,则说明氨气具有的性质是
(4)为防止环境污染,以下装置(盛放的液体均为水)可用于吸收多余氨气的是

您最近一年使用:0次
2023-04-18更新
|
342次组卷
|
4卷引用:浙江省宁波市2022—2023学年高一下学期学业水平考试模拟化学试题
解题方法
4 . 某校化学兴趣小组用下图所示装置探究 的性质。请回答:
的性质。请回答:
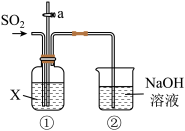
(1)装置②中发生反应的化学方程式是_______ 。
(2)若X为品红溶液,可观察到装置①中溶液_______ ,说明 具有
具有_______ 性。
(3)若X为紫色石蕊溶液,可观察到装置①中溶液_______ ,说明 的水溶液显
的水溶液显_______ (填“酸性”或“碱性”)。
(4)若X为 溶液,可观察到装置①中
溶液,可观察到装置①中_______ (填“有”或“无”)明显现象。打开活塞a,通入氧气,有白色沉淀生成,说明 最终被氧化为
最终被氧化为 ,由此可知
,由此可知 具有
具有_______ (填“氧化性”或“还原性”)。
(5)若X为 溶液,可观察到装置①中产生浅黄色沉淀(单质硫),说明
溶液,可观察到装置①中产生浅黄色沉淀(单质硫),说明 具有
具有_______ (填“氧化性”或“还原性”)。写出相应的化学方程式:_______ 。
 的性质。请回答:
的性质。请回答:
(1)装置②中发生反应的化学方程式是
(2)若X为品红溶液,可观察到装置①中溶液
 具有
具有(3)若X为紫色石蕊溶液,可观察到装置①中溶液
 的水溶液显
的水溶液显(4)若X为
 溶液,可观察到装置①中
溶液,可观察到装置①中 最终被氧化为
最终被氧化为 ,由此可知
,由此可知 具有
具有(5)若X为
 溶液,可观察到装置①中产生浅黄色沉淀(单质硫),说明
溶液,可观察到装置①中产生浅黄色沉淀(单质硫),说明 具有
具有
您最近一年使用:0次
名校
解题方法
5 . 某小组研究钠与不同浓度盐酸的反应。
【实验操作】
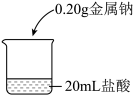
取5块质量均为0.20 g且形状相似的金属钠,分别放入20 mL不同浓度的盐酸中,如图。
【实验现象与数据】
经检验,⑤中出现的白色浑浊中的固体为NaCl。
【问题与讨论】
(1)补全钠与盐酸反应的化学方程式:
_______ :
(2)小组得出结论:钠的密度小于盐酸的密度,依据的实验现象是_______ 。
(3)在上述实验中,盐酸浓度越大,钠完全消失所用的时间_______ 。
(4)在上述实验中,钠完全消失所用的时间不同。原因可能是:盐酸浓度越大,化学反应越快,但是生成的氯化钠改变了盐酸与钠的_______ ,该因素影响了化学反应速率,进而影响了钠完全消失所用的时间。
【实验操作】
取5块质量均为0.20 g且形状相似的金属钠,分别放入20 mL不同浓度的盐酸中,如图。

【实验现象与数据】
| 编号 | ① | ② | ③ | ④ | ⑤ |
| c(HCl)/(mol·L-1) | 0.5 | 1.0 | 1.5 | 3.0 | 6.0 |
| 主要现象 | 钠浮在液面上,四处游动 | ||||
| 钠燃烧。溶液澄清 | 钠短时燃烧。溶液澄清 | 钠的表面有火花。溶液澄清 | 钠的表面。有少量火花。溶液澄清 | 钠的周围出现白色浑浊,一段时间后变澄清 | |
| 钠完全消失所用的时间/s | 11 | 21 | 37 | 65 | 114 |
【问题与讨论】
(1)补全钠与盐酸反应的化学方程式:

(2)小组得出结论:钠的密度小于盐酸的密度,依据的实验现象是
(3)在上述实验中,盐酸浓度越大,钠完全消失所用的时间
(4)在上述实验中,钠完全消失所用的时间不同。原因可能是:盐酸浓度越大,化学反应越快,但是生成的氯化钠改变了盐酸与钠的
您最近一年使用:0次
2023-03-15更新
|
505次组卷
|
3卷引用:2023年北京市第一次普通高中学业水平合格性考试化学试题
6 . 已知反应: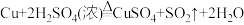 ,某化学兴趣小组用如图所示装置制取SO2,并进行相关性质实验。
,某化学兴趣小组用如图所示装置制取SO2,并进行相关性质实验。
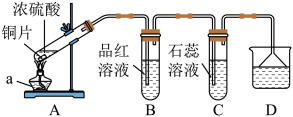
请回答下列问题:
(1)仪器a的名称是_______ ;
(2)B中品红溶液褪色,说明SO2具有_______ (填“漂白性”或“还原性”);
(3)C中石蕊溶液变为_______ (填“蓝色”或“红色”);
(4)为防止SO2污染环境,D中可选用_______ (填“NaOH”或“H2SO4”)溶液;
(5)酸性条件下,SO2与 发生如下反应:
发生如下反应: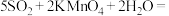
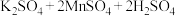 ,使溶液褪色。当
,使溶液褪色。当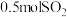 参加反应时,转移电子的物质的量是
参加反应时,转移电子的物质的量是_______ mol。
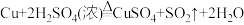 ,某化学兴趣小组用如图所示装置制取SO2,并进行相关性质实验。
,某化学兴趣小组用如图所示装置制取SO2,并进行相关性质实验。
请回答下列问题:
(1)仪器a的名称是
(2)B中品红溶液褪色,说明SO2具有
(3)C中石蕊溶液变为
(4)为防止SO2污染环境,D中可选用
(5)酸性条件下,SO2与
 发生如下反应:
发生如下反应: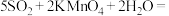
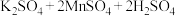 ,使溶液褪色。当
,使溶液褪色。当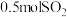 参加反应时,转移电子的物质的量是
参加反应时,转移电子的物质的量是
您最近一年使用:0次
2022-06-17更新
|
749次组卷
|
2卷引用:陕西省2022-2023学年高二下学期化学学业水平模拟测试(一)
解题方法
7 . 浓硫酸与木炭在加热条件下可发生化学反应,为检验反应的产物,某同学设计了如下图所示的实验。请据此回答下列问题。
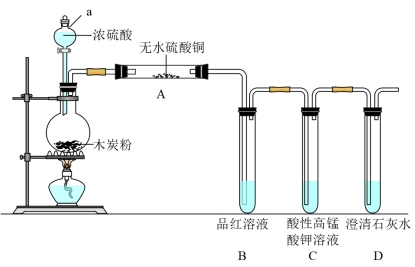
(1)写出浓硫酸和木炭粉在加热条件下发生反应的化学方程式_______ 。
(2)仪器a的名称是_______ 。
(3)装置A中出现_______ 现象,证明气体产物中有 。
。
(4)C装置作用是_______ 。

(1)写出浓硫酸和木炭粉在加热条件下发生反应的化学方程式
(2)仪器a的名称是
(3)装置A中出现
 。
。(4)C装置作用是
您最近一年使用:0次
2022-04-15更新
|
973次组卷
|
4卷引用:陕西省2022-2023学年高二下学期化学学业水平模拟测试(二)




