1 . 过二硫酸钠( )也叫高硫酸钠,可用于废气处理及有害物质的氧化降解。用
)也叫高硫酸钠,可用于废气处理及有害物质的氧化降解。用 溶液和一定浓度的NaOH溶液混合可制得
溶液和一定浓度的NaOH溶液混合可制得 晶体。实验室制备
晶体。实验室制备 晶体的装置如下图所示:
晶体的装置如下图所示: 。
。
(1)写出装置中生成 的反应的化学方程式:
的反应的化学方程式:___________ 。
(2)盛装NaOH溶液的仪器名称为___________ ,持续通入氮气的目的是___________ 。
(3)装置中硫酸的作用是___________ 。
(4)某兴趣小组设计实验探究不同环境下 氧化性的强弱。将
氧化性的强弱。将 (1.69g)与过量
(1.69g)与过量 (10g)溶于水中形成的混合溶液煮沸3min,观察并记录加入试剂时和加热过程中的现象(如下表所示)。
(10g)溶于水中形成的混合溶液煮沸3min,观察并记录加入试剂时和加热过程中的现象(如下表所示)。
①在___________ (填“中性”“酸性”或“碱性”)条件下, 的氧化能力最强。
的氧化能力最强。
②若用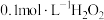 溶液滴定碱性氧化反应后的溶液(先将溶液调至酸性再滴定),滴定终点时的现象为
溶液滴定碱性氧化反应后的溶液(先将溶液调至酸性再滴定),滴定终点时的现象为___________ ;达到滴定终点时,消耗 溶液的体积为
溶液的体积为 。则碱性氧化后的溶液中
。则碱性氧化后的溶液中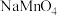 的质量为
的质量为___________ g(用含 的代数式表示,
的代数式表示,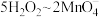 )
)
 )也叫高硫酸钠,可用于废气处理及有害物质的氧化降解。用
)也叫高硫酸钠,可用于废气处理及有害物质的氧化降解。用 溶液和一定浓度的NaOH溶液混合可制得
溶液和一定浓度的NaOH溶液混合可制得 晶体。实验室制备
晶体。实验室制备 晶体的装置如下图所示:
晶体的装置如下图所示: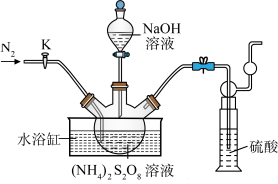
 。
。(1)写出装置中生成
 的反应的化学方程式:
的反应的化学方程式:(2)盛装NaOH溶液的仪器名称为
(3)装置中硫酸的作用是
(4)某兴趣小组设计实验探究不同环境下
 氧化性的强弱。将
氧化性的强弱。将 (1.69g)与过量
(1.69g)与过量 (10g)溶于水中形成的混合溶液煮沸3min,观察并记录加入试剂时和加热过程中的现象(如下表所示)。
(10g)溶于水中形成的混合溶液煮沸3min,观察并记录加入试剂时和加热过程中的现象(如下表所示)。| 环境 | 调节溶液氧化环境时的现象 | 加热煮沸3min期间产生的现象 |
| 中性 | 加入VmL蒸馏水,无明显现象 | 30s时开始有大量气泡冒出,3min后溶液变为深棕色,溶液中有悬浮小颗粒 |
| 碱性 | 加入VmL某浓度的NaOH溶液,瞬间变为棕色( ) ) | 10s后溶液逐渐变为深紫色( ),没有明显冒气泡现象 ),没有明显冒气泡现象 |
| 酸性 | 加入VmL稀硫酸无明显现象 | 煮沸3min后,有气泡冒出 |
 的氧化能力最强。
的氧化能力最强。②若用
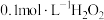 溶液滴定碱性氧化反应后的溶液(先将溶液调至酸性再滴定),滴定终点时的现象为
溶液滴定碱性氧化反应后的溶液(先将溶液调至酸性再滴定),滴定终点时的现象为 溶液的体积为
溶液的体积为 。则碱性氧化后的溶液中
。则碱性氧化后的溶液中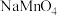 的质量为
的质量为 的代数式表示,
的代数式表示,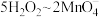 )
)
您最近半年使用:0次
2 . 拟用如图装置设计实验来探究纯净、干燥的氯气与氨气的反应。___________ 。
(2)如图中的装置连接顺序为A→___________ (用大写字母表示)。若按照正确顺序连接实验装置后,整套实验装置存在的主要缺点___________ 。
(3)写出F装置中的反应的一种工业用途:___________ 。
(4)在工业上利用反应N2+3H2 2NH3制备氨气。现在实验室模拟该反应探究影响反应速率的因素,在四个相同的容器中,在不同的温度下(其他条件相同)进行合成氨的反应,根据下列在相同时间内测得的结果判断,该反应所处的温度最高的是
2NH3制备氨气。现在实验室模拟该反应探究影响反应速率的因素,在四个相同的容器中,在不同的温度下(其他条件相同)进行合成氨的反应,根据下列在相同时间内测得的结果判断,该反应所处的温度最高的是___________ (填字母)。
A.v(NH3)=0.1mol/(L·min) B.v(H2)=0.6mol/(L·min) C.v(N2)=0.3mol/(L·min)

(2)如图中的装置连接顺序为A→
(3)写出F装置中的反应的一种工业用途:
(4)在工业上利用反应N2+3H2
 2NH3制备氨气。现在实验室模拟该反应探究影响反应速率的因素,在四个相同的容器中,在不同的温度下(其他条件相同)进行合成氨的反应,根据下列在相同时间内测得的结果判断,该反应所处的温度最高的是
2NH3制备氨气。现在实验室模拟该反应探究影响反应速率的因素,在四个相同的容器中,在不同的温度下(其他条件相同)进行合成氨的反应,根据下列在相同时间内测得的结果判断,该反应所处的温度最高的是A.v(NH3)=0.1mol/(L·min) B.v(H2)=0.6mol/(L·min) C.v(N2)=0.3mol/(L·min)
您最近半年使用:0次
解题方法
3 . I.如图所示,在一个带导管的胶塞侧面挖一个凹槽,并嵌入下端卷成螺旋状的铜丝;在A试管里加入 2 mL 浓H2SO4,盖好胶塞,使铜丝与浓H2SO4接触,加热进行反应,将生成的气体导入B试管的品红溶液中。请回答下列问题:
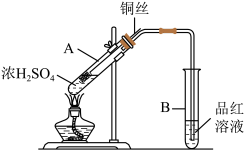
(1)铜与浓H2SO4反应,铜作
(2)B试管中的现象是
(3)本实验中将铜丝嵌入胶塞侧面的凹槽中,使铜丝可以自由抽动,该设计的特点是
Ⅱ.请回答:
(4)已知稀硫酸能与硫代硫酸钠发生如下反应:Na2S2O3+H2SO4=Na2SO4+SO2↑+H2O+S↓,下列各组实验中溶液最先变浑浊的是___________(填字母)。
| A.0.1 mol/L Na2S2O3和H2SO4各5 mL,加水5 mL,反应温度10℃ |
| B.0.1 mol/L Na2S2O3和H2SO4各5 mL,加水10 mL,反应温度10℃ |
| C.0.1 mol/L Na2S2O3和H2SO4各5 mL,加水5 mL,反应温度30℃ |
| D.0.2 mol/L Na2S2O3和H2SO4各5 mL,加水10 mL,反应温度30℃ |
您最近半年使用:0次
解题方法
4 . 戴口罩是新冠肺炎疫情常态化防控的措施之一。一次性医用口罩绒布的主要成分是聚丙烯[(C3H6)n],随意丢弃易引起白色污染。某兴趣小组尝试用焚烧法对口罩绒布进行处理,并将燃烧产物用氢氧化钠溶液吸收。
(1)聚丙烯完全燃烧的化学方程式为:2(C3H6)n+9nO2 6nCO2+6nX,X的化学式为
6nCO2+6nX,X的化学式为________ 。
(2)为“看见”CO2与NaOH的反应,甲同学设计了如图所示的实验方案,当观察到______ 现象时,说明两者发生反应。
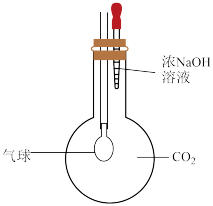
(3)将完全燃烧后的产物全部通入一定量的氢氧化钠溶液中,得到吸收液。乙同学对吸收液的成分产生兴趣,进行如下探究:
【提出问题】
吸收液中溶质的成分是什么?
【查阅资料】
①Na2CO3、NaHCO3的溶液均呈碱性;CaCl2溶液呈中性。
②NaOH与NaHCO3能反应
③Na2CO3+CaCl2=CaCO3↓+2NaCl
2NaHCO3+CaCl2=CaCO3↓+2NaCl+H2O+CO2↑
【猜想假设】
猜想一:NaOH、Na2CO3
猜想二:________
猜想三:Na2CO3、NaHCO3
猜想四:NaHCO3
【实验探究】
【交流反思】
实验结束后,为了对吸收液进行无害化处理,丙同学向吸收液中加入稀盐酸至不再产生气泡为止。写出其中一个反应的化学方程式:________ 。
(1)聚丙烯完全燃烧的化学方程式为:2(C3H6)n+9nO2
 6nCO2+6nX,X的化学式为
6nCO2+6nX,X的化学式为(2)为“看见”CO2与NaOH的反应,甲同学设计了如图所示的实验方案,当观察到

(3)将完全燃烧后的产物全部通入一定量的氢氧化钠溶液中,得到吸收液。乙同学对吸收液的成分产生兴趣,进行如下探究:
【提出问题】
吸收液中溶质的成分是什么?
【查阅资料】
①Na2CO3、NaHCO3的溶液均呈碱性;CaCl2溶液呈中性。
②NaOH与NaHCO3能反应
③Na2CO3+CaCl2=CaCO3↓+2NaCl
2NaHCO3+CaCl2=CaCO3↓+2NaCl+H2O+CO2↑
【猜想假设】
猜想一:NaOH、Na2CO3
猜想二:
猜想三:Na2CO3、NaHCO3
猜想四:NaHCO3
【实验探究】
| 步骤 | 实验操作 | 实验现象 | 实验结论 |
| 1 | 取吸收液少许于试管中,滴加2~3滴无色酚酞溶液 | 溶液呈碱性 | |
| 2 | 向步骤1所得溶液中加入过量的CaCl2溶液 | 产生白色沉淀,溶液为红色 | 猜想 |
实验结束后,为了对吸收液进行无害化处理,丙同学向吸收液中加入稀盐酸至不再产生气泡为止。写出其中一个反应的化学方程式:
您最近半年使用:0次
5 . 铜丝与稀硝酸反应的实验现象叙述错误的是
| A.铜丝逐渐变细 | B.铜丝表面有无色气体产生 |
| C.溶液变蓝 | D.产生的气体遇到空气无明显变化 |
您最近半年使用:0次
2023-06-26更新
|
251次组卷
|
5卷引用:黑龙江省哈尔滨市第三中学2022-2023学年高一下学期学业水平强化模拟考试化学试题
黑龙江省哈尔滨市第三中学2022-2023学年高一下学期学业水平强化模拟考试化学试题黑龙江省哈尔滨市第三中学校2022-2023学年高一下学期6月考试化学试题(已下线)专题十三 氮及其化合物(已下线)合格考真题汇编12氮元素及其化合物(已下线)合格考真题汇编21化学实验基础一
6 . 某实验小组探究 和
和 的反应。实验操作及现象如下。
的反应。实验操作及现象如下。
(1)取实验2后的溶液,进行如下实验:
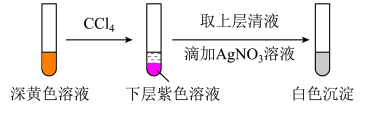
①根据______ 现象,判断实验2中有I2生成,因此反应后溶液显黄色。
②经检验,上述白色沉淀是AgCl。补全实验2中发生反应的离子方程式:_____ 。
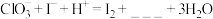
(2)查阅资料:一定条件下, 和I2都可以被氧化成
和I2都可以被氧化成 。
。
作出假设:NaClO3溶液用量增加导致溶液褪色的原因是______ 。
进行实验:
取少量实验4中的无色溶液进行以下实验,证实假设成立。
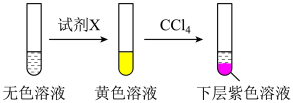
其中试剂X可以是______ (填字母)。
a.碘水 b.KMnO4溶液 c.NaHSO3溶液
 和
和 的反应。实验操作及现象如下。
的反应。实验操作及现象如下。实验及试剂 | 编号 | 无色NaClO3溶液用量 | 试管中溶液颜色 |
| 1 | 0.05mL | 浅黄色 |
2 | 0.02mL | 深黄色 | |
3 | 0.25mL | 浅黄色 | |
4 | 0.30mL | 无色 |

①根据
②经检验,上述白色沉淀是AgCl。补全实验2中发生反应的离子方程式:
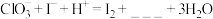
(2)查阅资料:一定条件下,
 和I2都可以被氧化成
和I2都可以被氧化成 。
。作出假设:NaClO3溶液用量增加导致溶液褪色的原因是
进行实验:
取少量实验4中的无色溶液进行以下实验,证实假设成立。

其中试剂X可以是
a.碘水 b.KMnO4溶液 c.NaHSO3溶液
您最近半年使用:0次
7 . 某化学实验小组同学利用以下实验装置制备氨气,并探究氨气的性质(部分仪器已略去)。请回答:

(1)实验室制备氨气的化学方程式为______ 。
(2)用装置B收集氨气时,应选择氨气的进气口是_______ (选填“a”或“b”)。
(3)打开装置B中的止水夹c,若观察到烧瓶内产生了红色喷泉,则说明氨气具有的性质是______ ,请用方程式表示:_______ ;氨气催化氧化可用于制硝酸,请写出氨气催化氧化的化学方程式_______ 。
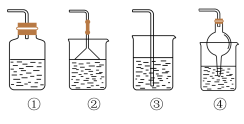
(4)为防止环境污染,以下装置(盛放的液体均为水)可用于吸收多余氨气的是______ (填序号)。

(1)实验室制备氨气的化学方程式为
(2)用装置B收集氨气时,应选择氨气的进气口是
(3)打开装置B中的止水夹c,若观察到烧瓶内产生了红色喷泉,则说明氨气具有的性质是
(4)为防止环境污染,以下装置(盛放的液体均为水)可用于吸收多余氨气的是

您最近半年使用:0次
2023-04-18更新
|
323次组卷
|
4卷引用:浙江省宁波市2022—2023学年高一下学期学业水平考试模拟化学试题
解题方法
8 . 某校化学兴趣小组用下图所示装置探究 的性质。请回答:
的性质。请回答:
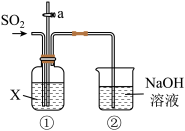
(1)装置②中发生反应的化学方程式是_______ 。
(2)若X为品红溶液,可观察到装置①中溶液_______ ,说明 具有
具有_______ 性。
(3)若X为紫色石蕊溶液,可观察到装置①中溶液_______ ,说明 的水溶液显
的水溶液显_______ (填“酸性”或“碱性”)。
(4)若X为 溶液,可观察到装置①中
溶液,可观察到装置①中_______ (填“有”或“无”)明显现象。打开活塞a,通入氧气,有白色沉淀生成,说明 最终被氧化为
最终被氧化为 ,由此可知
,由此可知 具有
具有_______ (填“氧化性”或“还原性”)。
(5)若X为 溶液,可观察到装置①中产生浅黄色沉淀(单质硫),说明
溶液,可观察到装置①中产生浅黄色沉淀(单质硫),说明 具有
具有_______ (填“氧化性”或“还原性”)。写出相应的化学方程式:_______ 。
 的性质。请回答:
的性质。请回答:
(1)装置②中发生反应的化学方程式是
(2)若X为品红溶液,可观察到装置①中溶液
 具有
具有(3)若X为紫色石蕊溶液,可观察到装置①中溶液
 的水溶液显
的水溶液显(4)若X为
 溶液,可观察到装置①中
溶液,可观察到装置①中 最终被氧化为
最终被氧化为 ,由此可知
,由此可知 具有
具有(5)若X为
 溶液,可观察到装置①中产生浅黄色沉淀(单质硫),说明
溶液,可观察到装置①中产生浅黄色沉淀(单质硫),说明 具有
具有
您最近半年使用:0次
名校
解题方法
9 . 某小组研究钠与不同浓度盐酸的反应。
【实验操作】
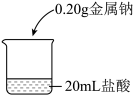
取5块质量均为0.20 g且形状相似的金属钠,分别放入20 mL不同浓度的盐酸中,如图。
【实验现象与数据】
经检验,⑤中出现的白色浑浊中的固体为NaCl。
【问题与讨论】
(1)补全钠与盐酸反应的化学方程式:
_______ :
(2)小组得出结论:钠的密度小于盐酸的密度,依据的实验现象是_______ 。
(3)在上述实验中,盐酸浓度越大,钠完全消失所用的时间_______ 。
(4)在上述实验中,钠完全消失所用的时间不同。原因可能是:盐酸浓度越大,化学反应越快,但是生成的氯化钠改变了盐酸与钠的_______ ,该因素影响了化学反应速率,进而影响了钠完全消失所用的时间。
【实验操作】
取5块质量均为0.20 g且形状相似的金属钠,分别放入20 mL不同浓度的盐酸中,如图。

【实验现象与数据】
| 编号 | ① | ② | ③ | ④ | ⑤ |
| c(HCl)/(mol·L-1) | 0.5 | 1.0 | 1.5 | 3.0 | 6.0 |
| 主要现象 | 钠浮在液面上,四处游动 | ||||
| 钠燃烧。溶液澄清 | 钠短时燃烧。溶液澄清 | 钠的表面有火花。溶液澄清 | 钠的表面。有少量火花。溶液澄清 | 钠的周围出现白色浑浊,一段时间后变澄清 | |
| 钠完全消失所用的时间/s | 11 | 21 | 37 | 65 | 114 |
【问题与讨论】
(1)补全钠与盐酸反应的化学方程式:

(2)小组得出结论:钠的密度小于盐酸的密度,依据的实验现象是
(3)在上述实验中,盐酸浓度越大,钠完全消失所用的时间
(4)在上述实验中,钠完全消失所用的时间不同。原因可能是:盐酸浓度越大,化学反应越快,但是生成的氯化钠改变了盐酸与钠的
您最近半年使用:0次
2023-03-15更新
|
480次组卷
|
3卷引用:2023年北京市第一次普通高中学业水平合格性考试化学试题
解题方法
10 . 某同学研究铜与稀硝酸的反应,实验如下(夹持装置已略去,气密性良好)。
(1)HNO3中的氮元素为+5价,是氮元素的最高价态,HNO3具有_______ (填“氧化”或“还原”)性。
(2)步骤III中分液漏斗内的红棕色气体是_______ 。
(3)补全铜与稀硝酸反应的化学方程式:_______ 。
3Cu+8HNO3(稀)=3Cu(NO3)2+ _______↑+4H2O
_______↑+4H2O
(4)上述实验过程中,有利于减少环境污染的措施有_______ (写出一条即可)。
| 步骤I | 步骤II | 步骤III |
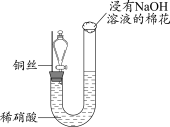 | 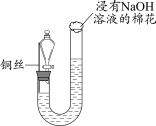 | 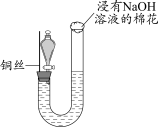 |
| 如图组装仪器并加入药品,分液漏斗旋塞关闭,U型管左侧无气体 | 将铜丝下移,一段时间后,U型管左侧产生无色气体,溶液逐渐变蓝,当液面低于铜丝时,反应逐渐停止 | 将铜丝上移,打开分液漏斗旋塞,U型管内气体进入分液漏斗立即变为红棕色,待气体全部进入分液漏斗后关闭旋塞 |
(2)步骤III中分液漏斗内的红棕色气体是
(3)补全铜与稀硝酸反应的化学方程式:
3Cu+8HNO3(稀)=3Cu(NO3)2+
 _______↑+4H2O
_______↑+4H2O(4)上述实验过程中,有利于减少环境污染的措施有
您最近半年使用:0次




